题目内容
12.为制取含HClO浓度较高的溶液,下列图示装置和原理均正确,且能达到实验目的是( )| A. | 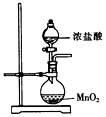 制取氯气 | B. | 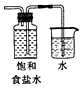 制取氯水 | C. | 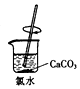 提高HClO浓度 | D. | 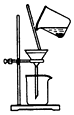 过滤 |
分析 A.实验室用浓盐酸与二氧化锰加热反应生成氯气,装置中缺少酒精灯;
B.氯气易溶于水,吸收氯气的导管不能插入溶液;
C.氯气与水发生反应Cl2+H2O?HCl+HClO,碳酸钙与HCl反应,不与次氯酸反应;
D.过滤时漏掉下端必须紧靠烧杯内壁.
解答 解:A.用浓盐酸与二氧化锰制取氯气时应该加热,该装置中缺少加热仪器,故A错误;
B.氯气易溶于水,吸收氯气时需要防止倒吸,图示装置会发生倒吸现象,故B错误;
C.加入碳酸钙固体,HCl与碳酸钙反应,而HClO不反应,溶液中氢离子浓度减小,平衡向正反应方向移动,HClO浓度增加,故C正确;
D.该装置中,漏掉下端没有紧靠烧杯内壁,操作不合理,故D错误;
故选C.
点评 本题考查化学实验方案的评价,题目难度不大,涉及氯气制备及性质、过滤操作、化学平衡及其影响等知识,明确制备原理为解答关键,试题培养了学生的化学实验能力.

练习册系列答案
相关题目
2.下列不是化石能源的是( )
| A. | 天然气 | B. | 潮汐 | C. | 煤 | D. | 石油 |
3.下列说法正确的是( )
| A. | 铅蓄电池充电时,阳极固体质量增大 | |
| B. | 0.1mol•L-1CH3COONa溶液加热后,溶液的pH减小 | |
| C. | 标准状况下,11.2L苯中含有的碳原子数为3×6.02×1023个 | |
| D. | 室温下,稀释0.1mol•L-1氨水c(H+).c(NH3•H2O)减小 |
20.下列化学用语中书写正确的是( )
| A. | 原子核内有10 个中子的氧原子:${\;}_{8}^{18}$O | |
| B. | 次氯酸的结构式:H-Cl-O | |
| C. | CO2的比例模型: | |
| D. | 溴化铵的电子式: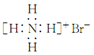 |
7.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,56g由N2和CO组成的混合气体含有的原子数目为4 NA | |
| B. | 高温下,0.2 molFe与足量水蒸气反应,生成的H2分子数为0.3NA | |
| C. | 1 L 1.0mol•L-1的NaAlO2水溶液中含有的总原子数为2NA | |
| D. | 1 mol羟基中含有的电子数为10NA |
17.硫酸、亚硫酸和氢硫酸是含硫的三种酸.下列说法不正确的是( )
| A. | 若向Na2S溶液中通入SO2则产生淡黄色沉淀 | |
| B. | 这三种酸都是二元酸,都能与氢氧化钠反应生成酸式盐和正盐 | |
| C. | 这三种酸的水溶液久置空气中都会变质 | |
| D. | 向氢硫酸、亚硫酸溶液中滴加氯水都会发生氧化还原反应 |
4.根据下列实验操作,预测的实验现象和实验结论或解释正确的是( )
| 实验操作 | 预测的实验现象 | 实验结论或解释 | |
| A | 向饱和Na2CO3 溶液中滴加少量稀盐酸 | 立即有气体逸出 | CO32-+2H+═H2O+CO2↑ |
| B | 将浓硫酸滴加到盛有铜片的试管中,并将 蘸有品红溶液的试纸置于试管口 | 品红试纸褪色 | SO2具有漂白性 |
| C | 铝箔在酒精灯火焰上加热 | 铝熔化但不会滴下 | A12O3的熔点比铝高 |
| D | 向淀粉的酸性水解液中滴入少量新制 Cu (OH)2悬浊液并加热 | 有砖红色沉淀生成 | 葡萄糖具有还原性 |
| A. | A | B. | B | C. | C | D. | D |
1.新型锌-空气电池的储存电量是锂电池的三倍,成本是锂电池的一半.这种电池使用特殊材料吸附空气中的氧,电池放电时总反应:2Zn+O2+4OH-+2H2O═2Zn(OH)42-,电解液是KOH溶液.下列有关该电池的说法正确的是( )
| A. | 锌是负极,发生还原反应 | |
| B. | O2在正极发生氧化反应 | |
| C. | 工作一段时间后,电解质溶液的碱性会减弱 | |
| D. | 该电池能将化学能全部转化为电能 |
2.一定条件下,下列金属中能与水发生置换反应并产生金属氧化物的是( )
| A. | 钾 | B. | 镁 | C. | 铁 | D. | 铜 |