2.下列说法中不正确的是( )
| A. | 化学反应除了生成新物质外,还伴随着能量的变化 | |
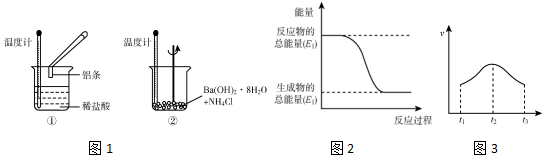
| B. | 物质燃烧和酸碱中和均放出热量 | |
| C. | 需要加热的反应肯定是吸热反应 | |
| D. | 化学反应是吸热的还是放热的取决于生成物具有的总能量和反应物具有的总能量的相对大小 |
20.科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O$?_{TiO_{2}}^{激光}$2H2↑+O2↑.制得的氢气可用于燃料电池.
(1)分解海水时,实现了从太阳能转变为化学能.生成的氢气用于燃料电池时,实现化学能转变为电能.
通常把拆开1mol 某化学键所吸收的能量或形成1mol某化学键所放出的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热,化学反应的反应热等于反应中断裂旧化学键的之和与反应中形成新化学键的键能之和的差.
(2)估算1mol N和 3mol H结合生成1mol NH3放出热量为45.4KJ.在一定条件下,N2和H2合成NH3,该反应为放热反应(填“放热”或“吸热”),每生成2mol NH3反应的热值为90.8KJ.
(1)分解海水时,实现了从太阳能转变为化学能.生成的氢气用于燃料电池时,实现化学能转变为电能.
通常把拆开1mol 某化学键所吸收的能量或形成1mol某化学键所放出的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热,化学反应的反应热等于反应中断裂旧化学键的之和与反应中形成新化学键的键能之和的差.
| 化学键 | H-H | N≡N | N-H |
| 键能/KJ•mol-1 | 436 | 946 | 390.8 |
19.A、B、C、D、E五种元素为同周期从左向右按原子序数递增(原子序数为5个连续的自然数)的顺序排列如下:下列说法中正确的是( )
| A | B | C | D | E |
| A. | HnDOm为强酸时,E的非金属性一定很强 | |
| B. | A(OH)n为强碱时,B(OH)m也一定为强碱 | |
| C. | E元素的最高化合价为+7时,D元素的负化合价可为-2价 | |
| D. | HnCOm为强酸时,E的单质可能有强还原性 |
18.表是元素周期表的一部分,针对表中的①~⑧种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:氩.
(2)在这些元素中,属于金属的是:Na、Al.
(3)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4.
(4)最高价氧化物的水化物显两性的是氢氧化铝;写出它与盐酸反应的离子方程式Al(OH)3+3H+=Al3++3H2O.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(2)在这些元素中,属于金属的是:Na、Al.
(3)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4.
(4)最高价氧化物的水化物显两性的是氢氧化铝;写出它与盐酸反应的离子方程式Al(OH)3+3H+=Al3++3H2O.
17.短周期元素X、Y、Z、W在周期表中的相对位置如图所示,其中W元素的原子结构示意图为 .请回答下列问题:
.请回答下列问题:
(1)Z元素位于元素周期表中第三周期VA族.
(2)X元素的最简单气态氢化物能与其最高价氧化物对应的水化物反应,得到的化合物属于离子化合物 (填“离子化合物”或“共价化合物”).
(3)X、Y、Z三种元素的原子半径由大到小的顺序为P>N>O(用元素符号表示).
(4)写出W单质与X的最高价氧化物对应水化物的浓溶液反应的化学方程式:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
 .请回答下列问题:
.请回答下列问题:| W | X | Y |
| Z |
(2)X元素的最简单气态氢化物能与其最高价氧化物对应的水化物反应,得到的化合物属于离子化合物 (填“离子化合物”或“共价化合物”).
(3)X、Y、Z三种元素的原子半径由大到小的顺序为P>N>O(用元素符号表示).
(4)写出W单质与X的最高价氧化物对应水化物的浓溶液反应的化学方程式:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
16.表为元素周期表的一部分.
(1)表中元素F的非金属性最强;元素K的金属性最强;元素Br的单质室温下呈液态(填写元素符号);
(2)表中元素⑦的原子结构示意图为
(3)表中元素⑥⑩氢化物的稳定性顺序为HF>HCl(填写化学式,下同);
(4)表中元素⑩和⑬最高价氧化物对应水化物的酸性:HClO4>HBrO4.
(5)表中元素②和⑦最高价氧化物对应水化物的碱性NaOH>LiOH.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ⑥ | |||
| 三 | ⑦ | ⑧ | ⑨ | ⑩ | ||||
| 四 | ⑪ | ⑫ | ⑬ | |||||
(2)表中元素⑦的原子结构示意图为

(3)表中元素⑥⑩氢化物的稳定性顺序为HF>HCl(填写化学式,下同);
(4)表中元素⑩和⑬最高价氧化物对应水化物的酸性:HClO4>HBrO4.
(5)表中元素②和⑦最高价氧化物对应水化物的碱性NaOH>LiOH.
13. 如图是NaCl晶体的一个晶胞结构棋型,KO2的晶体结构与NaCl的相似,KO2可以看做是Na+的位置被K+代替,Cl-的位置被O2-代替代替.则下列关于KO2晶体结构的叙述中正确的是( )
如图是NaCl晶体的一个晶胞结构棋型,KO2的晶体结构与NaCl的相似,KO2可以看做是Na+的位置被K+代替,Cl-的位置被O2-代替代替.则下列关于KO2晶体结构的叙述中正确的是( )
0 162671 162679 162685 162689 162695 162697 162701 162707 162709 162715 162721 162725 162727 162731 162737 162739 162745 162749 162751 162755 162757 162761 162763 162765 162766 162767 162769 162770 162771 162773 162775 162779 162781 162785 162787 162791 162797 162799 162805 162809 162811 162815 162821 162827 162829 162835 162839 162841 162847 162851 162857 162865 203614
 如图是NaCl晶体的一个晶胞结构棋型,KO2的晶体结构与NaCl的相似,KO2可以看做是Na+的位置被K+代替,Cl-的位置被O2-代替代替.则下列关于KO2晶体结构的叙述中正确的是( )
如图是NaCl晶体的一个晶胞结构棋型,KO2的晶体结构与NaCl的相似,KO2可以看做是Na+的位置被K+代替,Cl-的位置被O2-代替代替.则下列关于KO2晶体结构的叙述中正确的是( )| A. | 与K+距离相等且最近的O2-有8个 | |
| B. | 与K+距离相等且最近的O2-构成的多面体是六面体 | |
| C. | 一个KO2晶胞中的K+和O2-的粒子数都是4个 | |
| D. | 与K+距离相等且最近的K+有8个 |
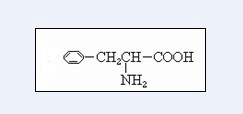 .
.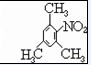 .
.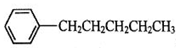 、
、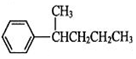 、
、
 、
、 、
、 、
、 .
.
 .
.