��Ŀ����
15����ѧ��Ӧ�����������仯�ǻ�ѧ��Ӧ�Ļ�������֮һ��ijͬѧ������ͼ1ʵ�飬�Լ��黯ѧ��Ӧ�е������仯��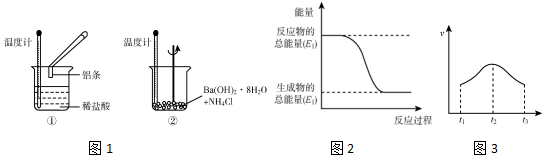
��ش��������⣺
��1��ʵ���з��֣���Ӧ����е��¶����ߣ����е��¶Ƚ��ͣ��ɴ��ж�����������ķ�Ӧ�Ƿ��ȷ�Ӧ��Ba��OH��2•8H2O��NH4Cl�ķ�Ӧ�����ȷ�Ӧ����Ӧ���̢٣���١��ڡ����������仯����ͼ2��ʾ��
��2������ʵ���ò��������������ʱ��Ĺ�ϵ��ͼ3��ʾ����t1-t2ʱ�����������������ҪӰ��������A��t2-t3������С����ҪӰ��������B��
A���¶� B��Ũ�� C��ѹǿ
��3����֪����ʢ��20mL 2mol/L��ϡ���ᣬ������������Һ��2min���ռ�����״����H2�����Ϊ224mL�����ʱ����ڷ�Ӧ����v��HCl��=0.5moL•-1•min-1��
���� ��1����ѧ��Ӧ�У��¶����ߣ���Ӧ���ȣ��¶Ƚ�����Ӧ���ȣ�ͼ2�з�Ӧ���������������������������÷�ӦΪ���ȷ�Ӧ���ݴ˽��н��
��2���¶ȡ���Һ��������Ũ�ȶ�Ӱ�췴Ӧ���ʣ���ͽ������û���Ӧ�Ƿ��ȷ�Ӧ���൱����Һ�¶����ߣ������¶ȷ�Ӧ����������Ũ�Ⱥ��¶ȶԷ�Ӧ����Ӱ����Դ�С������
��3������Hԭ���غ���㷴Ӧ���������ʵ������ٸ���v=$\frac{\frac{��n}{V}}{��t}$�������ᷴӦ���ʣ�
��� �⣺��1��Al��HCl��Ӧ���¶����ߣ���˵����Ӧ���ȣ�Ba��OH��2•8H2O��NH4Cl�ķ�Ӧ�¶Ƚ��ͣ�˵����ӦΪ���ȷ�Ӧ��
��Ӧ��Ϊ���ȷ�Ӧ����Ӧ�������������������������������Ԣٵ������仯����ͼ2��ʾ��
�ʴ�Ϊ���ţ������٣�
��2���¶ȡ���Һ��������Ũ�ȶ�Ӱ�췴Ӧ���ʣ���ͽ������û���Ӧ�Ƿ��ȷ�Ӧ���൱����Һ�¶����ߣ������¶ȷ�Ӧ��������t1-t2ʱ���ڣ��¶������߶�������Ũ�����ͣ�������������˵����Ӧ���ʵ���ҪӰ���������¶ȣ�t2-t3������С��˵����Ӧ���ʵ���ҪӰ��������������Ũ�ȣ�
�ʴ�Ϊ��A��B��
��3��n��H2��=$\frac{0.224L}{22.4L/mol}$=0.01mol������Hԭ���غ�òμӷ�Ӧ��n��HCl��=2n��H2��=0.02mol�����ʱ����ڷ�Ӧ����v��HCl��=$\frac{\frac{0.02mol}{0.02L}}{2min}$=0.5mol/��L•min����
�ʴ�Ϊ��0.5��
���� ����������������ķ�ӦΪ���忼������ʵ�鷽����ƣ��漰��Ӧ���ʼ��㡢��Ӧ����Ӱ�����ص�֪ʶ�㣬Ϊ��Ƶ���㣬�ѵ��ǣ�2���������Ҫ�����¶ȡ�Ũ�ȶԷ�Ӧ�����ۺ�Ӱ�죬��Ŀ�ѶȲ���

 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�| A�� | ��Na2S��ȥ��ˮ�е�Hg2+ | B�� | ���ȵ�Na2CO3��Һȥ���� | ||
| C�� | ������֬��������Ӧ������� | D�� | ����CuSO4��Һʱ������ϡH2SO4 |
 �о����֣�NOx��SO2����������Ҫ�ɷ֣���֪��
�о����֣�NOx��SO2����������Ҫ�ɷ֣���֪��2CO��g��+O2��g��?CO2��g����H1=-566.00kJ•mol-1
2SO2��g��+O2��g��?2SO3��g����H2=-196.6kJ•mol-1
2NO��g��+O2��g��?2NO2��g����H3=-113.0kJ•mol-1
��Ӧ2NO2��g��+SO2��g��+CO��g��?SO3��g��+2NO��g��+CO2��g���ġ�H=-268.3kJ•mol-1��NOx��Ҫ��Դ������β����
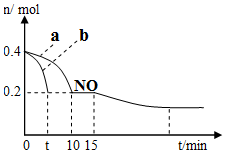
��1��T��ʱ��ģ������β����ת����2NO+2CO?2CO2+N2���������ʵ�����NO��CO�����ݻ�Ϊ2L���ܱ������У������¶Ⱥ�������䣬��Ӧ���̣�0��15min����NO�����ʵ�����ʱ��仯��ͼ��ʾ��
��T��ʱ�û�ѧ��Ӧ��ƽ�ⳣ��K=5��mol/L��-1��ƽ��ʱ�������¶Ȳ��䣬���������г���0.2mol CO��0.4mol N2��ƽ�⽫�����ƶ���������������ҡ�������
��ͼ1��a��b�ֱ��ʾʹ��ͬ�ִ���ʱ���ﵽƽ�������n��NO���ı仯���ߣ����б�ʾ����������ϴ��������b���a����b������
��15minʱ�����ı���練Ӧ����������n��NO��������ͼ��ʾ�ı仯����ı����������������CO�����ʵ���Ũ�Ȼ�����ѹǿ��
������SO2��Ҫ��Դ��ú��ȼ�գ�
25��ʱ������ƽ�ⳣ����
| ��ѧʽ | H2CO3 | H2SO3 |
| ����ƽ�ⳣ�� | K1=4.30��10-7 K2=5.61��10-11 | K1=1.54��10-2 K2=1.02��10-7 |
��2���ٳ����£�pH��ͬ��������Һ��I��Na2CO3��II��NaHCO3��III��Na2SO3�����ʵ���Ũ���ɴ�С������˳��Ϊ������ű�ʾ��
���ô�����Һ����SO2�ɽ���ת��ΪHSO3-���÷�Ӧ�����ӷ���ʽ�ǣ�H2O+2SO2+CO32-�T2HSO3-+CO2����
��3����֪NaHSO3��Һ�����ԣ�����˵����ȷ����D��
A��c��Na+��=2c��SO32-��+2c��HSO3-��+2c��H2SO3��
B��c��Na+��+c��H+��=c��OH����+c��HSO3����+c��SO32-��
C��c��HSO3-����c��H+����c��H2SO3����c��SO32-��
D��c��H+��+c��H2SO3��=c��SO32-��+c��OH-��
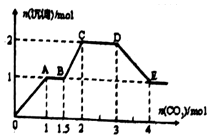 ��������ǿ����ʵĻ����Һ10L�����п��ܺ�K+��Ba2+��Na+��NH4+��Cl-��SO42-��AlO2-��OH-�еļ��֣�������ͨ��CO2���壬������������������CO2����֮�ʵĹ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
��������ǿ����ʵĻ����Һ10L�����п��ܺ�K+��Ba2+��Na+��NH4+��Cl-��SO42-��AlO2-��OH-�еļ��֣�������ͨ��CO2���壬������������������CO2����֮�ʵĹ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ����Һ����ȷ�����ڵ�������Ba2+��Na+��Cl-��NH4+ | |
| B�� | �϶������ڵ�������Cl-��OH- | |
| C�� | ������ȷ�������������ٻ�����һ�������ӣ�������ӵ���СŨ��Ϊ��0.2mol/L | |
| D�� | OA�η�Ӧ�����ӷ���ʽ����2AlO2-+CO2+3H2O�T2Al��OH��3��+CO32- |
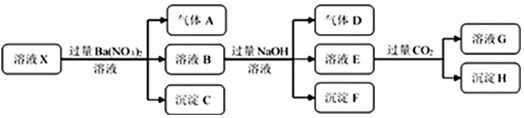
�����й��ƶϺ������ǣ�������
| A�� | ��Ҫȷ����ҺX���Ƿ���Fe3+�������Ϊȡ����ԭ��Һ���Թ��У���������KSCN��Һ����Һ��Ѫ��ɫ������Fe3+ | |
| B�� | ����CΪBaSO4������HΪBaCO3 | |
| C�� | ��Һ��һ������H+��Al3+��NH4+��Fe2+��SO42-��Cl- | |
| D�� | ����ҺXΪ100mL������������AΪ112mL�����������X��c��Fe2+��=0.05mol•L-1 |
��1���ֽ⺣ˮʱ��ʵ���˴�̫����ת��Ϊ��ѧ�ܣ����ɵ���������ȼ�ϵ��ʱ��ʵ�ֻ�ѧ��ת��Ϊ���ܣ�
ͨ���Ѳ�1mol ij��ѧ�������յ��������γ�1molij��ѧ�����ų����������ɸû�ѧ���ļ��ܣ����ܵĴ�С���Ժ�����ѧ����ǿ����Ҳ�����ڹ��㻯ѧ��Ӧ�ķ�Ӧ�ȣ���ѧ��Ӧ�ķ�Ӧ�ȵ��ڷ�Ӧ�ж��Ѿɻ�ѧ����֮���뷴Ӧ���γ��»�ѧ���ļ���֮�͵IJ
| ��ѧ�� | H-H | N��N | N-H |
| ����/KJ•mol-1 | 436 | 946 | 390.8 |
��������
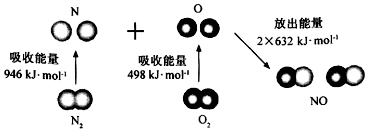
| A�� | ֱ�ۿ����÷�Ӧ�з�Ӧ�������е����������������������е������� | |
| B�� | 2 mol��̬��ԭ�ӽ������O2��g��ʱ���ܷų�498 KJ���� | |
| C�� | ����1 mol NO�����еĻ�ѧ������Ҫ����632KJ���� | |
| D�� | �÷�Ӧ���Ȼ�ѧ����ʽΪ��N2+O2�T2NO��H=+180KJ/mol�� |
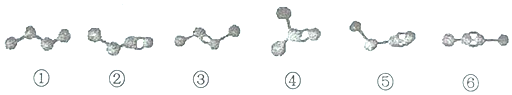
| A�� | ���ڡ��ۡ��ܵķ���ʽ��ΪC4H8������Ϊͬ���칹�� | |
| B�� | ���ݺ͢ķ���ʽ��ΪC4H6������Ϊͬ���칹�� | |
| C�� | ���ڡ��ۡ��ݡ��ֱ����������������ӳɷ�Ӧ�����ɵõ����� | |
| D�� | �����ʵ��������ں͢ݷֱ�����������ȫȼ�գ��������ĵ������� |
| A�� | ������Ϊ8�ĵ�ԭ�ӣ�${\;}_{8}^{15}$N | |
| B�� | ������ĵ���ʽ��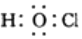 | |
| C�� | PCl5���ӵ�ÿ��ԭ�Ӷ�����8�����ȶ��ṹ | |
| D�� | �õ���ʽ��ʾNaCl���γɹ��̣�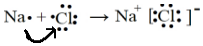 |