13.短周期元素的性质递变规律如图所示,下列说法正确的是( )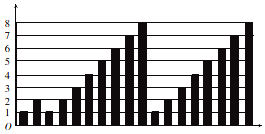

| A. | 横坐标为质子数,纵坐标为元素的最高正价 | |
| B. | 横坐标为原子序数,纵坐标为元素原子的最外层电子数 | |
| C. | 横坐标为核电荷数,纵坐标为元素原子的半径 | |
| D. | 横坐标为中子数,纵坐标为元素的非金属性 |
12.人类社会的进步离不开创新的发展.下列行为不符合绿色发展宗旨的是( )
| A. | 研发煤炭的洁净、高效利用技术,保护生态环境 | |
| B. | 推广CO2的再利用技术,将其合成有价值的化学品 | |
| C. | 利用工业废水灌溉农作物,提高水资源的利用率 | |
| D. | 提高风能、水能、太阳能等可再生清洁能源的使用比例 |
11.反应4NH3(g)+5O2(g)═4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的速率可表示为( )
| A. | v(NH3)=0.01 mol•L-1•s-1 | B. | v(O2)=0.001 mol•L-1•s-1 | ||
| C. | v(NO)=0.001 mol•L-1•s-1 | D. | v(H2O)=0.045 mol•L-1•s-1 |
10. 在如图所示的装置中,a的金属活泼性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是( )
在如图所示的装置中,a的金属活泼性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是( )
 在如图所示的装置中,a的金属活泼性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是( )
在如图所示的装置中,a的金属活泼性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是( )| A. | 碳棒上有气体放出,溶液c(H+)减小 | |
| B. | a是正极,b是负极 | |
| C. | 导线中有电子流动,电子从a极到b极 | |
| D. | a极上发生了氧化反应 |
9.下列关于元素周期律和元素周期表的论述中正确的是( )
| A. | 同一主族的元素从上到下金属性逐渐减弱 | |
| B. | 元素周期表是元素周期律的具体表现形式 | |
| C. | 同一周期从左到右,元素原子半径逐渐增大 | |
| D. | 非金属元素的最高正化合价等于它的负化合价的绝对值 |
7.下列转化需要加入氧化剂才能实现的是( )
| A. | H2S SO2 | B. | H2SO4 SO2 | C. | SO2 SO32- | D. | SO32- SO2 |
5.下列属于共价化合物的是( )
| A. | NaOH | B. | MgCl2 | C. | N2 | D. | H2O |
4.下列现象与氢键有关的是( )
①NH3的熔、沸点比VA族其他元素氢化物的高
②小分子的醇、羧酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④尿素的熔、沸点比醋酸的高
⑤液态氟化氢的化学式有时可以写成(HF)n 的形式
⑥H2O比H2S稳定.
0 162618 162626 162632 162636 162642 162644 162648 162654 162656 162662 162668 162672 162674 162678 162684 162686 162692 162696 162698 162702 162704 162708 162710 162712 162713 162714 162716 162717 162718 162720 162722 162726 162728 162732 162734 162738 162744 162746 162752 162756 162758 162762 162768 162774 162776 162782 162786 162788 162794 162798 162804 162812 203614
①NH3的熔、沸点比VA族其他元素氢化物的高
②小分子的醇、羧酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④尿素的熔、沸点比醋酸的高
⑤液态氟化氢的化学式有时可以写成(HF)n 的形式
⑥H2O比H2S稳定.
| A. | ①②③④⑤⑥ | B. | ①②③④⑤ | C. | ①②③④ | D. | ①②③ |
