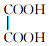题目内容
11.反应4NH3(g)+5O2(g)═4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的速率可表示为( )| A. | v(NH3)=0.01 mol•L-1•s-1 | B. | v(O2)=0.001 mol•L-1•s-1 | ||
| C. | v(NO)=0.001 mol•L-1•s-1 | D. | v(H2O)=0.045 mol•L-1•s-1 |
分析 根据v=$\frac{△c}{△t}$计算v(H2O),再利用速率之比等于化学计量数之比计算各物质表示的反应速率.进行判断.
解答 解:在体积10L的密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol.
则v(H2O)=$\frac{\frac{0.45mol}{10L}}{30s}$=0.0015mol•L-1•s-1,
A.速率之比等于化学计量数之比,所以v(NH3)=$\frac{2}{3}$×0.0015mol•L-1•s-1=0.0010mol•L-1•s-1,故A错误;
B.速率之比等于化学计量数之比,所以v(O2)=$\frac{5}{6}$×0.0015mol•L-1•s-1=0.00125mol•L-1•s-1,故B错误;
C.速率之比等于化学计量数之比,所以v(NO)=$\frac{2}{3}$×0.0015mol•L-1•s-1=0.0010mol•L-1•s-1,故C正确;
D.v(H2O)=$\frac{\frac{0.45mol}{10L}}{30s}$=0.0015mol•L-1•s-1,故D错误.
故选:C.
点评 本题考查化学反应速率的计算,难度不大,注意公式的运用,化学反应速率的计算通常利用定义法与速率规律计算,根据题目选择合适的计算方法.

练习册系列答案
相关题目
1.有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同.下列事实不能说明上述观点的是( )
| A. | 苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应 | |
| B. | 苯在50℃~60℃时发生硝化反应而甲苯在30℃时即可 | |
| C. | 甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色 | |
| D. | 乙烯能发生加成反应,乙烷不能发生加成反应 |
2.下列装置或操作能达到实验目的(必要的夹持装置及石棉网已省略)的是( )
| A. | 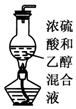 实验室制乙烯 | |
| B. | 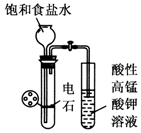 实验室制乙炔并验证乙炔能发生氧化反应 | |
| C. | 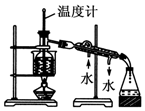 实验室中分馏石油 | |
| D. | 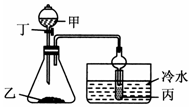 若甲为硫酸,乙为贝壳粉,丙为苯酚钠溶液,验证硫酸、碳酸、苯酚酸性的强弱 |
16.某有机物A的结构简式如下: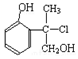 .下列叙述正确的是( )
.下列叙述正确的是( )
 .下列叙述正确的是( )
.下列叙述正确的是( )| A. | 有机物A属于芳香烃 | |
| B. | 有机物A可以和Br2的CCl4溶液发生加成反应 | |
| C. | 有机物A和浓硫酸混合加热170℃时,可以发生消去反应 | |
| D. | 1mol A和足量的NaOH溶液反应,可以消耗2mol NaOH |
3.下列实验中不能观察到明显变化的是( )
| A. | 把溴水滴加到淀粉KI溶液中 | |
| B. | 把Cl2通入FeCl2溶液中 | |
| C. | 把绿豆大的钾投入少量水中 | |
| D. | 把一段打磨过的镁带放入少量冷水中 |
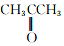
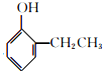 和
和 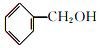
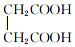 与
与