12.甲醇是一种重要化工原料,又是一种可再生能源,具有开发和应用的广阔前景.
(1)已知:CH3OH(g)═HCHO(g)+H2(g)△H=+84kJ•mol-1
2H2(g)+O2(g)═2H2O(g)△H=-484kJ•mol-1
工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式:2CH3OH(g)+O2(g)=2HCHO(g)+2H2O(g)△H=-316kJ•mol-1.
(2)工业上可用如下方法合成甲醇,化学方程式为CO(g)+2H2(g)?CH3OH(g),已知某些化学键的键能数据如表:
请回答下列问题:
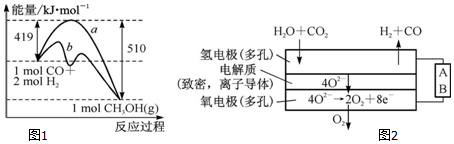
①该反应的△S<(填“>”或“<”)0.图1中曲线a到曲线b的措施是加入催化剂.
②已知CO中的C与O之间为三键,其键能为x kJ•mol-1,则x=1097.
(3)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电.
①该电池负极的电极反应式为CH3OH+8OH--6e-=CO32-+6H2O.
②若以该电池为电源,用石墨作电极电解200mL含有如表离子的溶液.
电解一段时间后,当两极收集到相同体积(相同条件下)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的质量为3.2g.
(4)电解水蒸气和CO2产生合成气(H2+CO).较高温度下(700~1 000℃),在SOEC两侧电极上施加一定的直流电压,H2O和CO2在氢电极发生还原反应产生O2-,O2-穿过致密的固体氧化物电解质层到达氧电极,在氧电极发生氧化反应得到纯O2.由图2可知A为直流电源的负极(填“正极”或“负极”),请写出以H2O为原料生成H2的电极反应式:H2O+2e-=H2↑+O2-.
(1)已知:CH3OH(g)═HCHO(g)+H2(g)△H=+84kJ•mol-1
2H2(g)+O2(g)═2H2O(g)△H=-484kJ•mol-1
工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式:2CH3OH(g)+O2(g)=2HCHO(g)+2H2O(g)△H=-316kJ•mol-1.
(2)工业上可用如下方法合成甲醇,化学方程式为CO(g)+2H2(g)?CH3OH(g),已知某些化学键的键能数据如表:
| 化学键 | C-C | C-H | H-H | C-O | C≡O | O-H |
| 键能/kJ•mol-1 | 348 | 413 | 436 | 358 | x | 463 |

①该反应的△S<(填“>”或“<”)0.图1中曲线a到曲线b的措施是加入催化剂.
②已知CO中的C与O之间为三键,其键能为x kJ•mol-1,则x=1097.
(3)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电.
①该电池负极的电极反应式为CH3OH+8OH--6e-=CO32-+6H2O.
②若以该电池为电源,用石墨作电极电解200mL含有如表离子的溶液.
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/mol•L-1 | 0.5 | 2 | 2 | 0.5 |
(4)电解水蒸气和CO2产生合成气(H2+CO).较高温度下(700~1 000℃),在SOEC两侧电极上施加一定的直流电压,H2O和CO2在氢电极发生还原反应产生O2-,O2-穿过致密的固体氧化物电解质层到达氧电极,在氧电极发生氧化反应得到纯O2.由图2可知A为直流电源的负极(填“正极”或“负极”),请写出以H2O为原料生成H2的电极反应式:H2O+2e-=H2↑+O2-.
11. 回答下列问题:
回答下列问题:
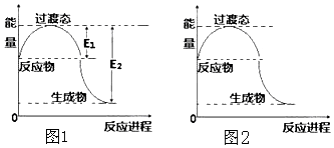
(1)2molCH4(g)和4mol O2(g)反应生成CO2(g)和H2O(g)过程中的能量变化如图1所示.已知E1=134KJ,E2=368KJ.则热化学方程式为2CH4(g)+4O2(g)=2CO2(g)+4H2O(g)△H=-234 kJ•mol-1生成18g H2O(l)放出或吸收的能量(范围)>58.5KJ
请在图2中画出加入催化剂后,反应过程中的能量变化曲线.
(2)在一定条件下,已知下列反应的热化学反应式:
C(石墨,s)+O2(g)=CO2(g)△H1; 2H2(g)+O2(g)=2H2O(l)△H2
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H3
由C(石墨,s)和气态H2反应合成气态1mol C2H2的热化学方程式2C (s,石墨)+H2(g)=C2H2(g))△H=2△H1+$\frac{1}{2}$△H2-$\frac{1}{2}$△H3;
(3)工业上可通过CO(C≡O)和H2化合制得CH3OH(气态),各键能数据如表所示
写出合成1mol CH3OH(气态)的热化学方程式CO(g)+2H2(g)?CH3OH (g)△H=-116 kJ•mol-1.
 回答下列问题:
回答下列问题:(1)2molCH4(g)和4mol O2(g)反应生成CO2(g)和H2O(g)过程中的能量变化如图1所示.已知E1=134KJ,E2=368KJ.则热化学方程式为2CH4(g)+4O2(g)=2CO2(g)+4H2O(g)△H=-234 kJ•mol-1生成18g H2O(l)放出或吸收的能量(范围)>58.5KJ
请在图2中画出加入催化剂后,反应过程中的能量变化曲线.
(2)在一定条件下,已知下列反应的热化学反应式:
C(石墨,s)+O2(g)=CO2(g)△H1; 2H2(g)+O2(g)=2H2O(l)△H2
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H3
由C(石墨,s)和气态H2反应合成气态1mol C2H2的热化学方程式2C (s,石墨)+H2(g)=C2H2(g))△H=2△H1+$\frac{1}{2}$△H2-$\frac{1}{2}$△H3;
(3)工业上可通过CO(C≡O)和H2化合制得CH3OH(气态),各键能数据如表所示
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能(kJ/mol) | 348 | 413 | 436 | 358 | 1072 | 463 |
7.500mL NaNO3和Cu(NO3)2的混合溶液中c(NO3-)=6mol/L,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到气体22.4L(标准状况下),假定电解后溶液体积仍为500mL,下列说法正确的是( )
0 162606 162614 162620 162624 162630 162632 162636 162642 162644 162650 162656 162660 162662 162666 162672 162674 162680 162684 162686 162690 162692 162696 162698 162700 162701 162702 162704 162705 162706 162708 162710 162714 162716 162720 162722 162726 162732 162734 162740 162744 162746 162750 162756 162762 162764 162770 162774 162776 162782 162786 162792 162800 203614
| A. | 原混合溶液中c(Na+)=6 mol | |
| B. | 电解后得到的Cu的物质的量为2 mol | |
| C. | 上述电解过程中共转移8 mol电子 | |
| D. | 电解后溶液中c(H+)=4 mol/L |

 废旧印刷电路板的回收利用可实现资源再生,并减少污染.废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末.
废旧印刷电路板的回收利用可实现资源再生,并减少污染.废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末.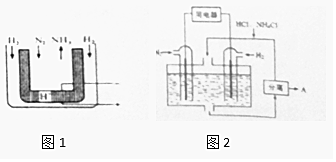 氮及其化合物与人类的生产、生活息息相关.
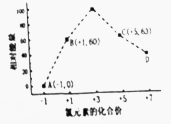
氮及其化合物与人类的生产、生活息息相关.