题目内容
4.在一定条件下,A和B反应可生成C和D,其能量变化如下:
①(多选)下列关于反应A+B═C+D的说法正确的是AD
A.反应前后原子的种类和数目一定不变
B.该反应若有热量变化,则一定是氧化还原反应
C.若该反应为放热反应,则不需加热反应就一定能发生
D.反应物的总质量与生成物的总质量一定相等,且该反应遵循能量守恒
②若E1<E2,则该反应为吸热 (填“吸热”或“放热”)反应,该反应的反应热为△H=(E2-E1)kJ•mol-1.
分析 ①A、根据反应前后原子守恒分析;
B、化学反应中的能量变化与反应类型无关,决定于反应物和生成物的能量的相对高低;
C、反应放热还是吸热与反应条件无关,决定于反应物和生成物的能量的相对高低;
D、根据质量守恒定律分析,任何化学反应都遵循能量守恒,也都有能量变化;
②当反应物的总能量小于生成物的总能量,则该反应为吸热反应,根据吸热为正结合两者的能量差计算反应热.
解答 解:①A、化学反应的过程是原子的重新组合过程,遵循原子守恒,所以反应前后原子的种类和数目一定不变,故A正确;
B、中和反应有热量放出,不是氧化还原反应,故B错误;
C、燃烧都是放热反应,需要加热到着火点,故C错误;
D、反应前后质量守恒,所以反应物的总质量与生成物的总质量一定相等,化学反应过程是旧键断裂新键形成的过程,有能量变化,遵循能量守恒定律,故D正确;
故选:AD;
②若E1<E2,即反应物的总能量小于生成物的总能量,则该反应为吸热反应,该反应的反应热△H=(E2-E1)kJ•mol-1;
故答案为:吸热;△H=(E2-E1)kJ•mol-1.
点评 本题考查化学反应过程的实质是原子的重新组合过程,是旧键断裂新键形成的过程,遵循原子守恒和能量守恒,难度不大.

练习册系列答案
 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
5.下列各组物质,不能按图(“→”表示反应一步完成)关系转化的是( )
| 选项 | a | b | c | 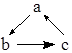 |
| A | Cu | CuO | Cu(OH)2 | |
| B | SiO2 | Na2SiO3 | H2SiO3 | |
| C | AlCl3 | NaAlO2 | Al(OH)3 | |
| D | CaO | Ca(OH)2 | CaCO3 |
| A. | A | B. | B | C. | C | D. | D |
6.下列化学用语的书写,正确的是( )
| A. | H2S的电子式: | B. | 硫原子的结构示意图: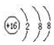 | ||
| C. | 氮气的电子式: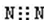 | D. | 水分子的结构式: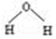 |
3.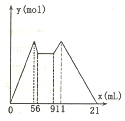 如图是向MgCl2、A1C13混合溶液中先滴加试剂A,然后改滴试剂B,所得沉淀的物质
如图是向MgCl2、A1C13混合溶液中先滴加试剂A,然后改滴试剂B,所得沉淀的物质
的量y(mol)与试剂体积V(mL)间的关系,以下结论不正确的是( )
 如图是向MgCl2、A1C13混合溶液中先滴加试剂A,然后改滴试剂B,所得沉淀的物质
如图是向MgCl2、A1C13混合溶液中先滴加试剂A,然后改滴试剂B,所得沉淀的物质的量y(mol)与试剂体积V(mL)间的关系,以下结论不正确的是( )
| A. | 原混合液中,c(A13+):c(Mg2+):c(C1)=1:1:5 | |
| B. | 若A和B为一元强碱和一元强酸,则滴加7.5mL剂A后改滴试剂B | |
| C. | 若A是NaOH,B是盐酸,则c(NaOH):c(HC1)=2:1 | |
| D. | 从6到9,相应离子反应方程式H++OH-═H2O |
10.下列实验方案不能达到实验目的是( )
| 实验目的 | 实验方案 | |
| A | 证明溴乙烷发生消去反应有乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反产生的气体通入溴的四氯化碳溶液 |
| B | 检验卤代烃中卤原子的种类 | 将溴乙烷与氢氧化钠溶液共热,取冷却后反应液 滴加硝酸酸化后滴加硝酸银溶液 |
| C | 验证乙炔能被酸性高锰酸钾溶液氧化 | 将电石与饱和食盐水反应生成的气体通入酸性高锰酸钾溶液,观察溶液是否褪色 |
| D | 验证苯和液溴在FeBr3的催化下发生取代反应 | 将反应产生的混合气体先通入溴的四氯化碳溶液再通入AgNO3溶液中,观察是否有淡黄色沉淀生成 |
| A. | A | B. | B | C. | C | D. | D |
16.已知X、Y、Z、W、R是元素周期表中前四周期的常见元素,相关信息如表所述:
(1)R在元素周期表中的位置为第四周期第VIII族,X的基态原子的价电子排布图为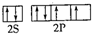 ,Z的基态原子的电子排布式为1s22s22p63s23p5.
,Z的基态原子的电子排布式为1s22s22p63s23p5.
(2)用“>”、“<”或“=”填空:
(3)用方程式表示下列过程:
①Y的气态氢化物的水溶液遇酚酞变红的原因NH3•H2O?NH4++OH-,
②W的最高价氧化物的水化物在水中发生电离H++AlO2-+H2O?Al(OH)3?Al3++3OH-.
| 元素 | 相关信息 |
| X | 地壳中含量最多的元素 |
| Y | 元素的气态氢化物极易溶于水,水溶液遇酚酞变红 |
| Z | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物是自来水生产过程中常用的消毒剂 |
| W | 与Z同周期,第一电离能至第四电离能分别是:I1=578kJ•mol-1,I2=1817kJ•mol-1,I3=2745kJ•mol-1,I4=11575kJ•mol-1 |
| R | 有多种化合价,水溶液中其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
 ,Z的基态原子的电子排布式为1s22s22p63s23p5.
,Z的基态原子的电子排布式为1s22s22p63s23p5.(2)用“>”、“<”或“=”填空:
| 简单离子半径 | 第一电离能 | 电负性 | 气态氢化物稳定性 |
| X<Y | X<Y | X>Z | H2X>YH3 |
①Y的气态氢化物的水溶液遇酚酞变红的原因NH3•H2O?NH4++OH-,
②W的最高价氧化物的水化物在水中发生电离H++AlO2-+H2O?Al(OH)3?Al3++3OH-.
13.在恒温、恒容的条件下,可逆反应H2(g)+I2(g)?2HI(g) 达到化学平衡状态的标志是( )
| A. | 混合气体的压强不再变化 | B. | 混合气体的密度不再变化 | ||
| C. | 混合气体的颜色不再变化 | D. | 混合气体中c(H2):c(I2):c(HI)=1:1:2 |
14.下列过程发生化学变化的是( )
| A. | 蒸馏 | B. | 将固体碘单质升华 | ||
| C. | 用液氨做制冷剂 | D. | 加热硫酸铜晶体失水 |