1.亚硫酰氯(SOCl2)是一种液态化合物,沸点770C.是一种重要的化工产品.加热可发生反应4SOCl2$\frac{\underline{\;200℃左右\;}}{\;}$2SO2+S2Cl2+3Cl2(S2Cl2的沸点为138X:).工业上合成亚硫酰氯方法之一是:
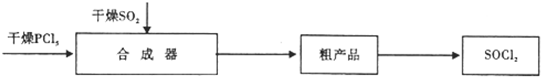
已知:合成器中发生的反应为:PCl5(熔融)+SO2$\frac{\underline{\;一定温度\;}}{\;}$SOCl2+POCl3△H<0 (POCl3 的沸点为105.3℃)
请回答下列问题:
(1)要得到干燥的SO2气体,可将潮湿的SO2通过装有AD的干燥装置(填写字母番号,多选).
A.浓硫酸B.生石灰C.氢氧化钠D.硅胶
(2)工业上从粗产品中,可采用分馏(或蒸馏)的方法(填写操作方法)获得较纯的SOCl2.
(3)合成器的内层,最好选用耐高温、耐氧化、耐腐蚀(工程陶瓷或耐高温陶瓷)材料制成.
(4)已知SOCl2与H2OI发生剧烈反应,有白雾形成并逸出有剌激性气味的气体,请写出该 反应的化学方程式SOCl2+H2O=SO2↑+HCl↑.
(5)SOCl2已Li-SOCl2电池,其电极材料分别为锂和碳,电解液是LiAlCl-SOCl2.电池的总反应可表示为:Li+SOCl2═4LiCl+S+SO2.该电池的负极的电极反应式为Li-e-=Li+
(6)某学习小组用刚吸收过少量SO2的NaOH溶液吸收SOOl2加热分解并冷却至室温后 的气体.吸收一段时间后,吸收液(强碱性)中肯定存在Cl-、OH-和SO${\;}_{4}^{2-}$.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气中的CO2的影响).
①提出合理假设.
假设1:只存在SO${\;}_{3}^{2-}$;假设2:既不存在SO${\;}_{3}^{2-}$也不存在ClO-;假设3:只存在ClO-.
②设计实验方案,进行实验.请写出实验步骤以及预期现象和结论.限选实验试剂:3moL.L-1H2SO4溶液、1moL.L-1NaOH溶液、0.1moL.L-1KMnO4溶液、淀粉一KI溶液、紫色石蕊试液.

已知:合成器中发生的反应为:PCl5(熔融)+SO2$\frac{\underline{\;一定温度\;}}{\;}$SOCl2+POCl3△H<0 (POCl3 的沸点为105.3℃)
请回答下列问题:
(1)要得到干燥的SO2气体,可将潮湿的SO2通过装有AD的干燥装置(填写字母番号,多选).
A.浓硫酸B.生石灰C.氢氧化钠D.硅胶
(2)工业上从粗产品中,可采用分馏(或蒸馏)的方法(填写操作方法)获得较纯的SOCl2.
(3)合成器的内层,最好选用耐高温、耐氧化、耐腐蚀(工程陶瓷或耐高温陶瓷)材料制成.
(4)已知SOCl2与H2OI发生剧烈反应,有白雾形成并逸出有剌激性气味的气体,请写出该 反应的化学方程式SOCl2+H2O=SO2↑+HCl↑.
(5)SOCl2已Li-SOCl2电池,其电极材料分别为锂和碳,电解液是LiAlCl-SOCl2.电池的总反应可表示为:Li+SOCl2═4LiCl+S+SO2.该电池的负极的电极反应式为Li-e-=Li+
(6)某学习小组用刚吸收过少量SO2的NaOH溶液吸收SOOl2加热分解并冷却至室温后 的气体.吸收一段时间后,吸收液(强碱性)中肯定存在Cl-、OH-和SO${\;}_{4}^{2-}$.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气中的CO2的影响).
①提出合理假设.
假设1:只存在SO${\;}_{3}^{2-}$;假设2:既不存在SO${\;}_{3}^{2-}$也不存在ClO-;假设3:只存在ClO-.
②设计实验方案,进行实验.请写出实验步骤以及预期现象和结论.限选实验试剂:3moL.L-1H2SO4溶液、1moL.L-1NaOH溶液、0.1moL.L-1KMnO4溶液、淀粉一KI溶液、紫色石蕊试液.
| 实验步骤 | 预期现象和结论 |
| 步骤1取少量吸收液于试管中滴加3moL.L-1H2SO4,至溶液呈酸性,然后将所得溶液分置于A、B试管中. | 无明显现象 |
| 步骤2:在A试管中滴加紫色石蕊试液 | 若先变红后褪色,证明有ClO-,否则无 |
| 步骤3:在B试管中滴加0.01mol•L-1KMnO4溶液 | 若紫红色褪去,证明有SO32-,否则无 |
15.根据下列实验或实验操作和现象,所得结论正确的是( )
| 实验或实验操作 | 现象 | 实验结论 | |
| A | 用大理石和盐酸反应制取CO2 气体,立即通入一定浓度的Na2SiO3 溶液中 | 出现白色沉淀 | 非金属性:Cl>C>Si |
| B | 向某溶液先滴加硝酸酸化,再滴加BaCl2溶液 | 有白色沉淀生成 | 原溶液中含有SO42-、SO32-、HSO3-中的一种或几种 |
| C | 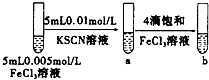 | 试管b比试管a中溶液的红色深 | 增大反应物浓度,平衡向正反应方向移动 |
| D |  | 左边棉球变为橙色,右边棉球变为蓝色 | 氧化性:Cl2>Br2>I2 |
| A. | A | B. | B | C. | C | D. | D |
14.下列实验操作能达到预期实验目的是( )
| 实验目的 | 实验操作 | |
| A | 检验FeCl3溶液的Fe2+ | 向溶液中加入酸性KMnO4溶液 |
| B | 比较CH3COOH和HCN的酸性强弱 | 用pH计分别测定CH3COONa、NaCN饱和溶液的pH |
| C | 制备H2SiO3胶体 | 向Na2SiO3溶液中滴加过量HCl |
| D | 除去乙酸乙酯中的CH3COOH | 加入饱和Na2CO3溶液,振荡后静置,分液 |
| A. | A | B. | B | C. | C | D. | D |
13.已知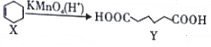 ,下列说法错误的是( )
,下列说法错误的是( )
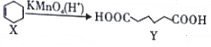 ,下列说法错误的是( )
,下列说法错误的是( )| A. | X分子中所有碳原子一定在同一平面上 | |
| B. | X与乙烯不属于同系物 | |
| C. | Y可发生取代反应、氧化反应 | |
| D. | Y的含有相同官能团的同分异构体有8种(不考虑立体异构) |
12.将一定量的CuS投入足量的HNO3中,收集到标准状况下的气体VL向反应后的溶液中加人足量的NaOH,产生蓝色沉淀,经过滤、洗涤、灼烧,得到CuO16g,若上述气体为NO和NO2的混合物,且体积比为1:1,则V为( )
| A. | 9.0L | B. | 13.44L | C. | 17.92L | D. | 16.8L |
11.下列有关苯的性质说法的是( )
| A. | 苯能使溴水褪色是因为苯与溴水发生了化学反应 | |
| B. | 欲从碘的苯溶液中分离出碘,通常采用萃取法 | |
| C. | 苯和不溶于水且密度比水大的四氯化碳都是无色液体,用试管和水就可以区别它们 | |
| D. | 因为苯通常是无色液体,所以在0℃的环境中可以直接将苯从试剂瓶倒人试管中 |
10.下列物质间的转化需要加入氧化剂才能进行的是( )
| A. | NaOH→NaCl | B. | C→CO2 | C. | Fe2O3→Fe | D. | NaHCO3→Na2CO3 |
9.将40g镁、铁、锌组成的混合物语适量的稀硫酸恰好完全反应,蒸干溶液测得固体质量136g,在上述溶液中加入一定量的氢氧化钠溶液使金属离子全部转化为沉淀,则此沉淀的质量是( )
| A. | 96g | B. | 74g | C. | 82.5g | D. | 无法计算 |
8.在CuO和Cu2O的混合物中,铜元素的质量分数为0.88,则混合物中CuO和Cu2O的物质的量之比为( )
| A. | 1:5 | B. | 1:4 | C. | 3:2 | D. | 5:1 |
7.下列说法不正确的是( )
0 162557 162565 162571 162575 162581 162583 162587 162593 162595 162601 162607 162611 162613 162617 162623 162625 162631 162635 162637 162641 162643 162647 162649 162651 162652 162653 162655 162656 162657 162659 162661 162665 162667 162671 162673 162677 162683 162685 162691 162695 162697 162701 162707 162713 162715 162721 162725 162727 162733 162737 162743 162751 203614
| A. | 通过对苯燃烧和甲烷燃烧现象的对比,可以判断两种物质中含碳量的高低 | |
| B. | 苯不能使酸性高锰酸钾溶液褪色,说明苯分子中没有碳碳双键 | |
| C. | 甲烷分子是空间正四面体形,苯分子是平面形 | |
| D. | 苯不能与Br2(CCl4)发生加成反应,故苯为饱和烃 |