16.7.5g镁铝合金完全溶解于100mL密度为1.40g/mL、质量分数为63%的浓硝酸中得到NO2和NO的混合气体11.2L(标准状况),向反应后的溶液中加入3.0mol/LNaOH溶液,当金属离子恰好完全沉淀时,得到19.4g沉淀,下列说法不正确的是( )
| A. | 该合金中铝与镁的物质的量之比是2:1 | |
| B. | 该浓硝酸中HNO3的物质的量浓度是14.0mol/L | |
| C. | NO2和NO的混合气体中,NO的体积分数是20% | |
| D. | 得到19.4g沉淀时,加入NaOH溶液的体积是300mL |
15.3.87克锌铜合金完全溶解于150mL、密度为1.20g/cm3、质量分数为21%的稀硝酸中,得到NO气体896mL (标准状况),向反应后的溶液中加入适量的1.0mol/LNaOH溶液,恰使溶液中的金属离子全部沉淀.下列说法不正确是( )
| A. | 该稀硝酸中HNO3的物质的量浓度是4.0mol/L | |
| B. | 加入NaOH溶液的体积是560mL | |
| C. | 被还原的硝酸的物质的量为0.04mol | |
| D. | 得到的金属氢氧化物的沉淀为5.81克 |
14.下列有关说法正确的是( )
| A. | 化学平衡向正向移动,反应物浓度一定降低 | |
| B. | 化学平衡向正向移动,生成物的浓度一定增加 | |
| C. | 化学平衡向正向移动,反应物的转化率一定增大 | |
| D. | 化学平衡向正向移动时,正反应速率一定大于逆反应速率 |
13.某温度下,体积一定的密闭容器中发生如下可逆反应X(g)+mY(s)?3Z(g)△H,下列说法正确的是( )
| A. | 气体的密度不变时.说明达到了平衡状态 | |
| B. | 加入少量的X,△H变大 | |
| C. | 加入一定量的惰性气体,平衡向左移动 | |
| D. | 加入少量的Y正反应速率加快 |
8.肼是一种常见的还原剂,不同条件下分解产物不同.60-300℃时,在Cu等金属表面肼分解的机理如图.
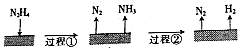
已知:200℃时:
Ⅰ.3N2H4(g)═N2(g)+4NH3(g)△H1=-32.9kJ•mol-1;
Ⅱ.N2H4(g)+H2(g)═2NH3(g)△H2=-41.8kJ•mol-1.
下列说法不正确的是( )
0 162539 162547 162553 162557 162563 162565 162569 162575 162577 162583 162589 162593 162595 162599 162605 162607 162613 162617 162619 162623 162625 162629 162631 162633 162634 162635 162637 162638 162639 162641 162643 162647 162649 162653 162655 162659 162665 162667 162673 162677 162679 162683 162689 162695 162697 162703 162707 162709 162715 162719 162725 162733 203614

已知:200℃时:
Ⅰ.3N2H4(g)═N2(g)+4NH3(g)△H1=-32.9kJ•mol-1;
Ⅱ.N2H4(g)+H2(g)═2NH3(g)△H2=-41.8kJ•mol-1.
下列说法不正确的是( )
| A. | 肼属于共价化合物 | |
| B. | 图示过程①、②都是吸热反应 | |
| C. | 反应Ⅰ中氧化剂与还原剂的物质的量之比为2:1 | |
| D. | 200℃时,肼分解的热化学方程式为:N2H4(g)═N2(g)+2H2(g)△H═+50.7kJ•mol-1 |
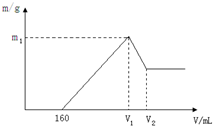 将镁和铝的混合物0.1mol溶于100ml 2mol/L的H2SO4溶液中,然后滴加1mol/L的NaOH溶液,在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示,请回答:
将镁和铝的混合物0.1mol溶于100ml 2mol/L的H2SO4溶液中,然后滴加1mol/L的NaOH溶液,在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示,请回答: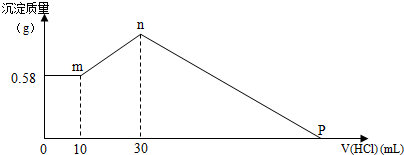
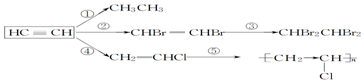
 ,加聚反应.
,加聚反应.