题目内容
14.下列有关说法正确的是( )| A. | 化学平衡向正向移动,反应物浓度一定降低 | |
| B. | 化学平衡向正向移动,生成物的浓度一定增加 | |
| C. | 化学平衡向正向移动,反应物的转化率一定增大 | |
| D. | 化学平衡向正向移动时,正反应速率一定大于逆反应速率 |
分析 A、如增大反应物的浓度,平衡向正方向移动,达到平衡时,反应物的浓度比改变条件前大;
B、如果减少生成物的浓度平衡正向移动,则生成物的浓度减小;
C、两种物质参加的可逆反应,增加其中一种物质的量,另一种物质的转化率增加,而本身的转化率降低;
D、如果正逆反应速率不等,平衡一定移动,正反应速率大于逆反应速率,则平衡正向移动.
解答 解:A、如增大反应物的浓度,平衡向正方向移动,达到平衡时,反应物的浓度比改变条件前大,故A错误;
B、如果减少生成物的浓度平衡正向移动,则生成物的浓度减小,故B错误;
C、两种物质参加的可逆反应,增加其中一种物质的量,另一种物质的转化率增加,而本身的转化率降低,如A+B?C增加A的量,A本身转化率降低,而不是升高,故C错误;
D、如果正逆反应速率不等,平衡一定移动,正反应速率大于逆反应速率,则平衡正向移动,所以化学平衡向正向移动时,正反应速率一定大于逆反应速率,故D正确;
故选D.
点评 本题考查化学平衡的影响因素,题目难度中等,试题灵活性强,注重能力的考查和解决方法的训练.有利于提高学生分析问题、解决问题的能力,注意利用列举反例法进行解答.

练习册系列答案
相关题目
15.下列关于丙烯(CH3-CH=CH2)的说法正确的( )
| A. | 丙烯分子有7个σ键,1个π键 | |
| B. | 丙烯分子中3个碳原子都是sp2杂化 | |
| C. | 丙烯分子中最多有7个原子共平面 | |
| D. | 丙烯分子中3个碳原子在同一直线上 |
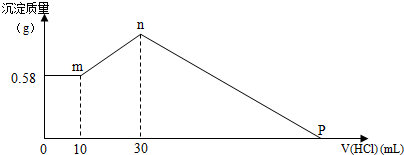
5. 向50mL稀H2SO4与稀HNO3的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如图所示,且每一段只对应一个反应.下列说法正确的是( )
向50mL稀H2SO4与稀HNO3的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如图所示,且每一段只对应一个反应.下列说法正确的是( )
 向50mL稀H2SO4与稀HNO3的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如图所示,且每一段只对应一个反应.下列说法正确的是( )
向50mL稀H2SO4与稀HNO3的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如图所示,且每一段只对应一个反应.下列说法正确的是( )| A. | 开始时产生的气体为H2 | |
| B. | AB段发生的反应为置换反应 | |
| C. | 所用混合溶液中c(HNO3)=0.5 mol•L-1 | |
| D. | 参加反应铁粉的总质量m2=5.6 g |
3.在10℃和2×105 Pa的条件下,反应aA(g)?dD(g)+eE(g)建立平衡后,再逐步增大体系的压强(温度不变).表列出了不同压强下平衡时物质D的浓度.
根据表中数据,回答下列问题:
(1)压强从2×105 Pa增加到5×105 Pa时,平衡移动方向是左,理由是D浓度增大的倍数小于压强增大的倍数.
(2)压强从5×105 Pa增加到1×106 Pa时,平衡移动方向是右,理由是D浓度增大的倍数大于压强增大的倍数,此时压强增大可能使E液化,使生成物的气体体积减小.
| 压强(Pa) | 2×105 | 5×105 | 1×106 |
| 浓度(mol•L-1) | 0.085 | 0.20 | 0.44 |
(1)压强从2×105 Pa增加到5×105 Pa时,平衡移动方向是左,理由是D浓度增大的倍数小于压强增大的倍数.
(2)压强从5×105 Pa增加到1×106 Pa时,平衡移动方向是右,理由是D浓度增大的倍数大于压强增大的倍数,此时压强增大可能使E液化,使生成物的气体体积减小.
4.下列有关物质的性质与用途具有对应关系的是( )
| A. | NH3极易溶于水,可用于工业制冷剂 | |
| B. | HNO3具有酸性,可用于制备硝酸盐原料 | |
| C. | NH4 NO3易溶于水,可用于制造高温材料 | |
| D. | N2难溶于水,可用于合成氨原料 |

 .用电子式表示D2C的形成过程
.用电子式表示D2C的形成过程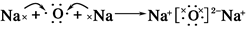 .
.