题目内容
13.某温度下,体积一定的密闭容器中发生如下可逆反应X(g)+mY(s)?3Z(g)△H,下列说法正确的是( )| A. | 气体的密度不变时.说明达到了平衡状态 | |
| B. | 加入少量的X,△H变大 | |
| C. | 加入一定量的惰性气体,平衡向左移动 | |
| D. | 加入少量的Y正反应速率加快 |
分析 A.Y为固体,反应达到平衡时气体的质量不变;
B.反应热与参加反应的反应物的物质的量无关;
C.加入惰性气体,平衡不移动;
D.Y为固体,加固体,平衡不移动.
解答 解:A.Y为固体,反应达到平衡时气体的质量不变,则气体的密度不变时.说明达到了平衡状态,故A正确;
B.加入少量的X,反应放出或吸热的热量增大,但△H不变,故B错误;
C.加入惰性气体,参加反应的气体的浓度不变,则平衡不移动,故C错误;
D.Y为固体,加固体,参加反应气体的浓度不变,则平衡不移动,故D错误.
故选A.
点评 本题考查了化学平衡的影响因素,为高频考点,题目难度中等,注意掌握浓度、压强、温度等影响对化学平衡的影响,试题有利于提高学生的分析、理解能力及灵活应用基础知识的能力.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案
相关题目
14.在一定条件下,分别以高锰酸钾、氯酸钾、过氧化氢为原料制取氧气,当制得同温、同压下相同体积的氧气时,三个反应中转移的电子数之比为( )
| A. | 1:1:l | B. | 2:2:1 | C. | 1:1:2 | D. | 4:3:2 |
1.下列物质的分类合理的是( )
| A. | 酸性氧化物:CO2、SO2、H2O | B. | 碱性氧化物:Na2O、CaO、P2O5 | ||
| C. | 碱:NaOH、KOH、Ba(OH)2 | D. | 铵盐:NH4Cl、NH4NO3、(NH4)2SO4 |
8.肼是一种常见的还原剂,不同条件下分解产物不同.60-300℃时,在Cu等金属表面肼分解的机理如图.
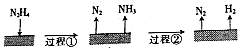
已知:200℃时:
Ⅰ.3N2H4(g)═N2(g)+4NH3(g)△H1=-32.9kJ•mol-1;
Ⅱ.N2H4(g)+H2(g)═2NH3(g)△H2=-41.8kJ•mol-1.
下列说法不正确的是( )

已知:200℃时:
Ⅰ.3N2H4(g)═N2(g)+4NH3(g)△H1=-32.9kJ•mol-1;
Ⅱ.N2H4(g)+H2(g)═2NH3(g)△H2=-41.8kJ•mol-1.
下列说法不正确的是( )
| A. | 肼属于共价化合物 | |
| B. | 图示过程①、②都是吸热反应 | |
| C. | 反应Ⅰ中氧化剂与还原剂的物质的量之比为2:1 | |
| D. | 200℃时,肼分解的热化学方程式为:N2H4(g)═N2(g)+2H2(g)△H═+50.7kJ•mol-1 |
5.根据表信息回答以下问题:
部分短周期元素的原子半径及主要化合价
(1)E、F、G三元素形成的化合物中化学键类型是离子键和共价键.
(2)B、H两元素的最高价氧化物所对应的水化物相互反应的离子方程式是Al(OH)3+3H+═Al3++3H2O.
(3)实验室中制取H单质反应的化学方程式是MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
部分短周期元素的原子半径及主要化合价
| 元素 | A | B | C | D | E | F | G | H |
| 原子半 径(nm) | 0.130 | 0.118 | 0.090 | 0.102 | 0.073 | 0.154 | 0.037 | 0.099 |
| 主要 化合价 | +2 | +3 | +2 | +6,-2 | -2 | +1 | +1 | +7,-1 |
(2)B、H两元素的最高价氧化物所对应的水化物相互反应的离子方程式是Al(OH)3+3H+═Al3++3H2O.
(3)实验室中制取H单质反应的化学方程式是MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
2.短周期元素的性质或原子结构如表:
(1)写出元素X的离子结构示意图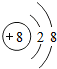 .写出元素Z的气态氢化物的电子式
.写出元素Z的气态氢化物的电子式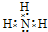 (用元素符号表示)
(用元素符号表示)
(2)写出Y元素最高价氧化物水化物的电离方程式H++AlO2-+H2O?Al(OH)3?Al3++3OH-.
(3)元素T与氯元素相比,非金属性较强的是F(用元素符号表示).
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | L层p电子数比s电子数多2个 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |
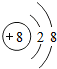 .写出元素Z的气态氢化物的电子式
.写出元素Z的气态氢化物的电子式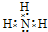 (用元素符号表示)
(用元素符号表示)(2)写出Y元素最高价氧化物水化物的电离方程式H++AlO2-+H2O?Al(OH)3?Al3++3OH-.
(3)元素T与氯元素相比,非金属性较强的是F(用元素符号表示).
3.反应2NO+2CO $\frac{\underline{\;催化剂\;}}{△}$ N2+2CO2是汽车尾气的净化原理.下列判断正确的是( )
| A. | 该反应是置换反应 | B. | 该反应是复分解反应 | ||
| C. | CO发生氧化反应 | D. | NO是还原剂 |
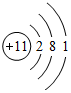 ,B离子的电子式
,B离子的电子式 ,C原子的名称氢原子,D原子的电子式
,C原子的名称氢原子,D原子的电子式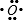 .
.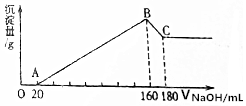 将一定质量的镁、铝合金,投入200mL一定浓度的盐酸中,合金完全溶解,向所得溶液中滴加5mol/L NaOH溶液,生成的沉淀质量与加入NaOH溶液体积如图所示.
将一定质量的镁、铝合金,投入200mL一定浓度的盐酸中,合金完全溶解,向所得溶液中滴加5mol/L NaOH溶液,生成的沉淀质量与加入NaOH溶液体积如图所示.