17.在标准状况下,将a L HCl(气)溶于1L水中(水的密度为1g•cm-3),得到的盐酸的密度为b g•mL-1,质量分数为w,物质的量浓度为c mol•L-1则下列关系式中不正确的是( )
| A. | w=$\frac{36.5a}{(36.5a+22400)}$ | B. | w=$\frac{36.5c}{1000b}$ | ||
| C. | C=$\frac{1000ab}{(36.5a+22400)}$ | D. | b=$\frac{(36.5a+22400)}{(a+1)}$ |
16.氢气、铝、铁都是重要的还原剂.已知下列反应的热化学方程式,下列关于反应的焓变判断正确的是( )
2H2(g)+O2(g)=2H2O(g)△H1
3H2 (g)+Fe2O3 (s)=2Fe (s)+3H2O(g)△H2
2Fe (s)+$\frac{3}{2}$O2 (g)=Fe2O3 (s)△H3
2Al (s)+$\frac{3}{2}$O2 (g)=Al2O3 (s)△H4
2Al (s)+Fe2O3 (s)=Al2O3 (s)+2Fe (s)△H5.
2H2(g)+O2(g)=2H2O(g)△H1
3H2 (g)+Fe2O3 (s)=2Fe (s)+3H2O(g)△H2
2Fe (s)+$\frac{3}{2}$O2 (g)=Fe2O3 (s)△H3
2Al (s)+$\frac{3}{2}$O2 (g)=Al2O3 (s)△H4
2Al (s)+Fe2O3 (s)=Al2O3 (s)+2Fe (s)△H5.
| A. | △H1<0△H3>0 | B. | △H5<0△H4<△H3 | C. | △H1=△H2+△H3 | D. | △H3=△H4+△H5 |
15.根据下列实验操作和现象所得出的结论错误的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | SO2通入酸性高锰酸钾溶液 | 酸性高锰酸钾溶液褪色 | SO2具有还原性 |
| B | 向NaSiO3溶液的试管中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去 | 2min后,试管里出现凝胶 | 非金属性:Cl>Si |
| C | 将盛有铜片的容器中加入浓硝酸 | 产生大量红棕色气体;溶液变为蓝绿色 | 浓硝酸具有强氧化性 |
| D | 浓硫酸滴到湿润的蔗糖中 | 蔗糖变成黑色海绵状 | 浓硫酸具有脱水性和强氧化性 |
| A. | A | B. | B | C. | C | D. | D |
13.25℃时,有关物质的电离平衡常数如表:
(1)电解质由强至弱顺序为H2SO3>CH3COOH>H2CO3(用化学式表示,下同).
(2)常温下,0.02mol•L-1的CH3COOH溶液的电离度约为3%,体积为10mLpH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者<后者(填“>”、“<”或“=”).
(3)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的顺序为CO32->SO32->CH3COO->HSO3-.
(4)NaHSO3溶液显酸性的原因HSO3-?H++SO32-,HSO3-+H2O?H2SO3+OH-,HSO3-的电离程度大于其水解程度,所以NaHSO3溶液显酸性(离子方程式配适当文字叙述),其溶液中离子浓度由大到小的关系是C(Na+)>C(HSO3-)>C(H+)>C(SO32-)>C(OH-).
| 化学式 | CH3COOH | H2CO3 | H2SO3 |
| 电离平衡常数K | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(2)常温下,0.02mol•L-1的CH3COOH溶液的电离度约为3%,体积为10mLpH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者<后者(填“>”、“<”或“=”).
(3)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的顺序为CO32->SO32->CH3COO->HSO3-.
(4)NaHSO3溶液显酸性的原因HSO3-?H++SO32-,HSO3-+H2O?H2SO3+OH-,HSO3-的电离程度大于其水解程度,所以NaHSO3溶液显酸性(离子方程式配适当文字叙述),其溶液中离子浓度由大到小的关系是C(Na+)>C(HSO3-)>C(H+)>C(SO32-)>C(OH-).
9.某学习小组,用稀HNO3与大理石反应过程中质量减小的方法,探究影响反应速率的因素.所用HNO3浓度为1.00mol•L-1、2.00mol•L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298K、308K,每次实验HNO3的用量为25.00mL、大理石用量为10.00g.
实验设计如表:
将相应的实验目的填入下列空格中:
(1)实验①和②探究浓度对该反应速率的影响;
(2)实验①和③探究温度对该反应速率的影响;
(3)实验①和④探究固体颗粒大小对该反应速率的影响.
实验设计如表:
| 编号 | T/K | 大理石规格 | HNO3浓度 |
| ① | 298 | 粗颗粒 | 2.00 mol•L-1 |
| ② | 298 | 粗颗粒 | 1.00 mol•L-1 |
| ③ | 308 | 粗颗粒 | 2.00 mol•L-1 |
| ④ | 298 | 细颗粒 | 2.00 mol•L-1 |
(1)实验①和②探究浓度对该反应速率的影响;
(2)实验①和③探究温度对该反应速率的影响;
(3)实验①和④探究固体颗粒大小对该反应速率的影响.
8.已知:CuS、Cu2S是两种黑色不溶于水的固体,但一定条件下都能与稀HNO3反应,用离子方程式表示为:
①3CuS+8H++8NO3-=3Cu2++3SO42-+8NO↑+4H2O
②3Cu2S+16H++10NO3-=6Cu2++3SO42-+10NO↑+8H2O
现有不同质量的四份CuS、Cu2S的混合物样品分别和100mL物质的量浓度5mol/L稀硝酸充分反应,所取样品质量与产生气体体积(标准状况下测定)如表所示:
试回答下列问题(不考虑硝酸的挥发以及溶液体积变化):
(1)a组实验结束后,溶液中c(NO3-)=2.75mol/L;
(2)b组实验结束后,溶液的pH=0;
(3)通过计算分析实验c组中产生气体的体积(V)范围7L<V<11.2L.
0 162526 162534 162540 162544 162550 162552 162556 162562 162564 162570 162576 162580 162582 162586 162592 162594 162600 162604 162606 162610 162612 162616 162618 162620 162621 162622 162624 162625 162626 162628 162630 162634 162636 162640 162642 162646 162652 162654 162660 162664 162666 162670 162676 162682 162684 162690 162694 162696 162702 162706 162712 162720 203614
①3CuS+8H++8NO3-=3Cu2++3SO42-+8NO↑+4H2O
②3Cu2S+16H++10NO3-=6Cu2++3SO42-+10NO↑+8H2O
现有不同质量的四份CuS、Cu2S的混合物样品分别和100mL物质的量浓度5mol/L稀硝酸充分反应,所取样品质量与产生气体体积(标准状况下测定)如表所示:
| 实验序号 | a | b | c |
| 样品质量(g) | 9.6 | 12.8 | 64.0 |
| 气体体积(L) | 5.04 | 6.72 | V |
(1)a组实验结束后,溶液中c(NO3-)=2.75mol/L;
(2)b组实验结束后,溶液的pH=0;
(3)通过计算分析实验c组中产生气体的体积(V)范围7L<V<11.2L.
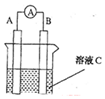 (1)如图所示,若C为浓硝酸,电流表指针发生偏转,B电极材料为Fe,A电极材料为Cu,则B电极的电极反应式为4H++2NO3-+2e-=2NO2↑+2H2O,A电极的电极反应式为Cu-2e-=Cu2+;反应进行一段时间后溶液C的pH将升高(填“升高”“降低”或“基本不变”).
(1)如图所示,若C为浓硝酸,电流表指针发生偏转,B电极材料为Fe,A电极材料为Cu,则B电极的电极反应式为4H++2NO3-+2e-=2NO2↑+2H2O,A电极的电极反应式为Cu-2e-=Cu2+;反应进行一段时间后溶液C的pH将升高(填“升高”“降低”或“基本不变”).