题目内容
16.氢气、铝、铁都是重要的还原剂.已知下列反应的热化学方程式,下列关于反应的焓变判断正确的是( )2H2(g)+O2(g)=2H2O(g)△H1
3H2 (g)+Fe2O3 (s)=2Fe (s)+3H2O(g)△H2
2Fe (s)+$\frac{3}{2}$O2 (g)=Fe2O3 (s)△H3
2Al (s)+$\frac{3}{2}$O2 (g)=Al2O3 (s)△H4
2Al (s)+Fe2O3 (s)=Al2O3 (s)+2Fe (s)△H5.
| A. | △H1<0△H3>0 | B. | △H5<0△H4<△H3 | C. | △H1=△H2+△H3 | D. | △H3=△H4+△H5 |
分析 A.燃烧为放热反应;
B.铝热反应为放热反应,且Al比Fe活泼,Al燃烧放出热量多;
C.3H2 (g)+Fe2O3 (s)=2Fe (s)+3H2O(g)△H2
2Fe (s)+$\frac{3}{2}$O2 (g)=Fe2O3 (s)△H3
由盖斯定律可知,两反应相加得到3H2 (g)+$\frac{3}{2}$O2 (g)=3H2O(g);
D.2Al (s)+$\frac{3}{2}$O2 (g)=Al2O3 (s)△H4
2Al (s)+Fe2O3 (s)=Al2O3 (s)+2Fe (s)△H5
由盖斯定律可知,两反应相减得到2Fe (s)+$\frac{3}{2}$O2 (g)=Fe2O3 (s).
解答 解:A.燃烧为放热反应,则△H1<0、△H3<0,故A错误;
B.铝热反应为放热反应,且Al比Fe活泼,Al燃烧放出热量多,则△H5<0、△H4<△H3,故B正确;
C.3H2 (g)+Fe2O3 (s)=2Fe (s)+3H2O(g)△H2
2Fe (s)+$\frac{3}{2}$O2 (g)=Fe2O3 (s)△H3
由盖斯定律可知,两反应相加得到3H2 (g)+$\frac{3}{2}$O2 (g)=3H2O(g),则3△H1=(△H2+△H3)×2,故C错误;
D.2Al (s)+$\frac{3}{2}$O2 (g)=Al2O3 (s)△H4
2Al (s)+Fe2O3 (s)=Al2O3 (s)+2Fe (s)△H5
由盖斯定律可知,两反应相减得到2Fe (s)+$\frac{3}{2}$O2 (g)=Fe2O3 (s),则△H3=△H4-△H5,故D错误;
故选B.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化、盖斯定律应用、焓变的正负为解答的关键,侧重分析与应用能力的考查,注意选项C为解答的难点,题目难度不大.

| A. | 甲苯能使酸性高锰酸钾溶液褪色,而苯不能使酸性高锰酸钾溶液褪色 | |
| B. | 苯酚能跟NaOH溶液反应,而乙醇不能与NaOH溶液反应 | |
| C. | 苯与硝酸在加热的条件生成硝基苯,而甲苯在加热条件下与硝酸发生反应生成三硝基甲苯 | |
| D. | 乙炔能发生加成,乙烷不能 |
| A. | 甲烷的燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 MPa下,将0.5 mol N2(g)和1.5 mol H2(g)置于密闭容器中充分反应生成NH3(g)放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | 在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1 | |
| D. | HCl和NaOH反应的中和热△H=-57.3 kJ•mol-1,则H2SO4和Ca(OH)2反应的△H=2×(-57.3)kJ•mol-1 |
| A. | 从溶解的整个过程来看,既包含着物理变化,又包含着化学变化 | |
| B. | 氯化钠溶于水达到饱和后,溶解过程并没有停止 | |
| C. | 氯化钠溶于水中,无论是否形成饱和溶液,都存在溶解与结晶的过程 | |
| D. | 将K37Cl投入到K35Cl的饱和溶液中,溶液中溶质的质量会减小 |
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应的平衡常数表达式K=$\frac{c(C)c(D)}{c(A)c(B)}$,该反应为放热反应(选填“吸热”、“放热”).当反应达到平衡时,升高温度,A的转化率减小(选填“增大”、“减小”或“不变”).
(2)830℃时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003mol/(L•s),则6s时c(A)=0.022mol/L,C的物质的量为0.09mol.
(3)一定条件下,向体积为2L的恒容密闭容器中充入1molA(g)和3molB(g),判断该反应达到平衡状态的依据是d.
a.c(A)=c(C) b.容器中压强不变
c.混合气体的平均相对分子质量不变 d.v逆(D)=v正(B)
(4)1200℃时反应C(g)+D(g)?A(g)+B(g)的平衡常数的值为2.5.
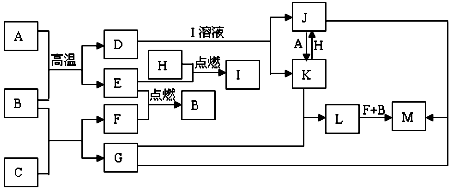
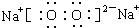 .
.