19.氮原子 2p 亚层上的 3 个电子不相同的是( )
| A. | 能量 | B. | 电子云形状 | C. | 电子云伸展方向 | D. | 自旋状态 |
18.Q、W、X、Y、Z是原子序数依次增大的短周期元素.X的焰色反应呈黄色.Q元素的原子最外层电子数是其内层电子数的2倍.W、Z元素的原子最外层电子数相同,Z元素的原子的核电荷数是W的2倍.元素Y的合金是日常生活中使用最广泛的金属材料之一.下列说法正确的是( )
| A. | X、Y的最高价氧化物的水化物之间不能发生反应 | |
| B. | W、X两种元素形成的简单离子的半径大小顺序:X>W | |
| C. | 元素Q和Z能形成QZ2型的共价化合物 | |
| D. | Z元素的氢化物稳定性大于W元素的氢化物稳定性 |
16.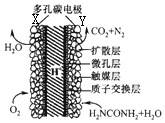 直接尿素电池的结构如图所示,下列说法不正确的是( )
直接尿素电池的结构如图所示,下列说法不正确的是( )
 直接尿素电池的结构如图所示,下列说法不正确的是( )
直接尿素电池的结构如图所示,下列说法不正确的是( )| A. | 电池工作时,化学能转化为电能 | |
| B. | 电池工作时,H+向Y极区迁移,Y极周围溶液的pH减小 | |
| C. | 碳电池采用多孔并用触媒层可加快反应速率 | |
| D. | Y极的电极反应式为H2NCONH2+H2O-6e-═N2↑+CO2+6H+ |
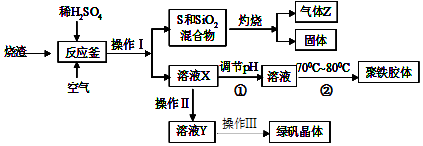
11.钨主要用于制造硬质或耐高温的合金.自然界中黑钨矿的主要成分是铁和锰的钨酸盐(FeWO4、MnWO4),还含少量Si、P、As的化合物.黑钨矿冶炼钨的工艺流程如图1:
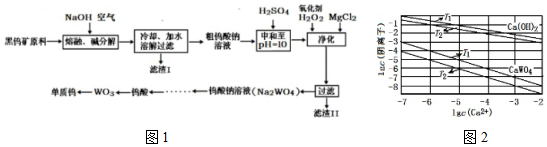
已知:①滤渣I的主要成份是Fe2O3、MnO2;
②上述流程中,除最后一步外,其余步骤中钨的化合价未变;
③常温下钨酸难溶于水.
回答下列问题:
(1)钨酸盐(FeWO4、MnWO4)中钨元素的化合价为+6,请写出MnWO4在熔融条件下发生碱分解反应生成MnO2的化学方程式2MnWO4+O2+4NaOH$\frac{\underline{\;高温\;}}{\;}$2MnO2+2Na2WO4+2H2O.
(2)上述流程中向粗钨酸钠溶液中加硫酸调pH=10后,溶液中的杂质阴离子为SiO32-、HAsO32-、HAsO42-、HPO42-等,“净化”过程中,加入H2O2的目的是氧化HAsO32-生成HAsO42-,滤渣Ⅱ的主要成分是MgSiO3、MgHAsO4、MgHPO4 .
(3)高温下密闭容器中用H2还原WO3可得到金属钨,其反应过程大致分为三个阶段,各阶段主要成分与温度的关系如表.
已知:温度过高时,WO2(s)可转变为WO2(g).
WO2(s)+2H2(g)?W(s)+2H2O(g)△H=+66.0KJ•mol-1
WO2(s)?WO2(g)△H=+203.9KJ•mol-1
则在700℃时,WO2(g)与H2(g)反应生成固体W(s)的热化学方程式为WO2(g)+2H2(g)?W(s)+2H2O(g△H=-137.9kJ•mol-1.
(4)已知氢氧化钙和钨酸钙(CaWO4)都是微溶性的电解质,两者的溶解度均随温度升高而减小.不同温度下两种物质的沉淀溶解平衡曲线如图2,则T1时Ksp(CaWO4)=1×10-10.在钨酸钠溶液中加入石灰乳得到大量钨酸钙,则T2时该反应的平衡常数为1×103.
(5)利用电解法可以从碳化钨(WC)废料中回收钨.电解时,用碳化钨做阳极,不锈钢做阴极,盐酸为电解液,阳极析出钨酸并放出CO2,该阳极反应式为WC+6H2O-10e-=H2WO4+CO2↑+10H+.

已知:①滤渣I的主要成份是Fe2O3、MnO2;
②上述流程中,除最后一步外,其余步骤中钨的化合价未变;
③常温下钨酸难溶于水.
回答下列问题:
(1)钨酸盐(FeWO4、MnWO4)中钨元素的化合价为+6,请写出MnWO4在熔融条件下发生碱分解反应生成MnO2的化学方程式2MnWO4+O2+4NaOH$\frac{\underline{\;高温\;}}{\;}$2MnO2+2Na2WO4+2H2O.
(2)上述流程中向粗钨酸钠溶液中加硫酸调pH=10后,溶液中的杂质阴离子为SiO32-、HAsO32-、HAsO42-、HPO42-等,“净化”过程中,加入H2O2的目的是氧化HAsO32-生成HAsO42-,滤渣Ⅱ的主要成分是MgSiO3、MgHAsO4、MgHPO4 .
(3)高温下密闭容器中用H2还原WO3可得到金属钨,其反应过程大致分为三个阶段,各阶段主要成分与温度的关系如表.
| 温度 | 25℃~550℃~600℃~700℃ |
| 主要成分 | WO3 W2O5 WO2 W |
WO2(s)+2H2(g)?W(s)+2H2O(g)△H=+66.0KJ•mol-1
WO2(s)?WO2(g)△H=+203.9KJ•mol-1
则在700℃时,WO2(g)与H2(g)反应生成固体W(s)的热化学方程式为WO2(g)+2H2(g)?W(s)+2H2O(g△H=-137.9kJ•mol-1.
(4)已知氢氧化钙和钨酸钙(CaWO4)都是微溶性的电解质,两者的溶解度均随温度升高而减小.不同温度下两种物质的沉淀溶解平衡曲线如图2,则T1时Ksp(CaWO4)=1×10-10.在钨酸钠溶液中加入石灰乳得到大量钨酸钙,则T2时该反应的平衡常数为1×103.
(5)利用电解法可以从碳化钨(WC)废料中回收钨.电解时,用碳化钨做阳极,不锈钢做阴极,盐酸为电解液,阳极析出钨酸并放出CO2,该阳极反应式为WC+6H2O-10e-=H2WO4+CO2↑+10H+.
10.活动小组同学采用如图装置制备并测定所得固体中亚硝酸钠(NaNO2)的质量分数(装置可重复使用,部分夹持仪器已省略).
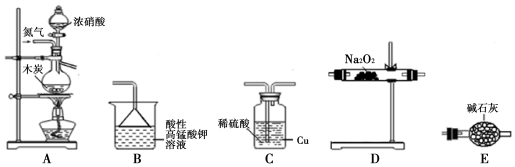
已知:①2NO+Na2O2═2NaNO2;
②酸性条件下,NO、NO2都能与MnO4-反应生成NO3-和Mn2+;NaNO2能使
酸性高锰酸钾溶液褪色.
(1)实验装置的连接顺序为ACEDEB;
(2)C瓶内发生反应的离子方程式为Cu+2H++NO2=Cu2++NO+H2O.
(3)为了测定亚硝酸钠的含量,称取4.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.10mol•L-1的酸性KMnO4溶液进行滴定,实验所得数据如表.
①第一组实验数据出现较明显异常,造成异常的原因可能是ac(填字母序号).
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶用蒸馏水洗净后未干燥
c.观察滴定终点时仰视读数
②根据表中数据进行计算,所制得的固体中亚硝酸钠的质量分数为86.25%.
(4)设计实验,比较0.1mol•L-1NaNO2溶液中NO2-的水解程度和0.1mol•L-1HNO2溶液中HNO2电离程度的相对大小25℃时,将两种溶液等体积混合,若混合溶液的pH<7,则说明HNO2的电离程度大于NO2-的水解程度;若pH>7,则说明HNO2的电离程度小于NO2-的水解程度(简要说明实验步骤、现象和结论,仪器和药品自选).
0 162432 162440 162446 162450 162456 162458 162462 162468 162470 162476 162482 162486 162488 162492 162498 162500 162506 162510 162512 162516 162518 162522 162524 162526 162527 162528 162530 162531 162532 162534 162536 162540 162542 162546 162548 162552 162558 162560 162566 162570 162572 162576 162582 162588 162590 162596 162600 162602 162608 162612 162618 162626 203614

已知:①2NO+Na2O2═2NaNO2;
②酸性条件下,NO、NO2都能与MnO4-反应生成NO3-和Mn2+;NaNO2能使
酸性高锰酸钾溶液褪色.
(1)实验装置的连接顺序为ACEDEB;
(2)C瓶内发生反应的离子方程式为Cu+2H++NO2=Cu2++NO+H2O.
(3)为了测定亚硝酸钠的含量,称取4.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.10mol•L-1的酸性KMnO4溶液进行滴定,实验所得数据如表.
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶用蒸馏水洗净后未干燥
c.观察滴定终点时仰视读数
②根据表中数据进行计算,所制得的固体中亚硝酸钠的质量分数为86.25%.
(4)设计实验,比较0.1mol•L-1NaNO2溶液中NO2-的水解程度和0.1mol•L-1HNO2溶液中HNO2电离程度的相对大小25℃时,将两种溶液等体积混合,若混合溶液的pH<7,则说明HNO2的电离程度大于NO2-的水解程度;若pH>7,则说明HNO2的电离程度小于NO2-的水解程度(简要说明实验步骤、现象和结论,仪器和药品自选).

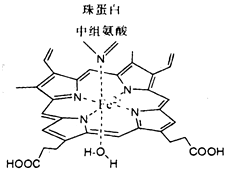 红细胞中血红素结构如图所示,回答下列问题:
红细胞中血红素结构如图所示,回答下列问题: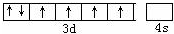 .
.