题目内容
18.Q、W、X、Y、Z是原子序数依次增大的短周期元素.X的焰色反应呈黄色.Q元素的原子最外层电子数是其内层电子数的2倍.W、Z元素的原子最外层电子数相同,Z元素的原子的核电荷数是W的2倍.元素Y的合金是日常生活中使用最广泛的金属材料之一.下列说法正确的是( )| A. | X、Y的最高价氧化物的水化物之间不能发生反应 | |
| B. | W、X两种元素形成的简单离子的半径大小顺序:X>W | |
| C. | 元素Q和Z能形成QZ2型的共价化合物 | |
| D. | Z元素的氢化物稳定性大于W元素的氢化物稳定性 |
分析 Q、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色,则X为Na元素;Q元素的原子最外层电子数是其内层电子数的2倍,Q元素原子有2个电子层,最外层电子数为4,故Q为碳元素;W、Z最外层电子数相同,二者处于同一主族,Z的核电荷数是W的2倍,故Z为硫元素,W为氧元素;元素Y的合金是日常生活中使用最广泛的金属材料之一,则Y为Al元素,以此解答该题.
解答 解:由以上分析可知Q为C元素、W为O元素、X为Na元素、Y为Al元素、Z为S元素.
A.氢氧化铝是两性氢氧化物,溶于强碱,与氢氧化钠反应生成偏铝酸钠、水,故A错误;
B.W为O元素、X为Na元素,对应的离子半径O2->Na+,故B错误;
C.CS2属于共价化合物,故C正确;
D.非金属性O>S,则O对应的氢化物较稳定,故D错误.
故选C.
点评 本题考查位置、结构、性质的关系及应用,为高频考点,题目难度中等,正确推断各元素名称是解答本题的关键,注意熟悉元素化合物的性质、物质的组成和结构等知识,试题综合性较强,有利于培养学生灵活应用所学知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.在化学反应2KBr+Cl2═2KCl+Br2中,还原剂是( )
| A. | Cl2 | B. | KBr | C. | KCl | D. | Br2 |
9.下列化学用语正确的是( )
| A. | CO2的结构式 O=C=O | B. | HCl的电子式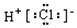 | ||
| C. | 氯离子结构示意图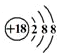 | D. | 作为相对原子质量标准的原子614C |
3. 草酸(H2C2O4)是一种重要的有机化工原料.为探究草酸的制取、性质及应用,进行如下实验.
草酸(H2C2O4)是一种重要的有机化工原料.为探究草酸的制取、性质及应用,进行如下实验.
实验Ⅰ:草酸晶体的制备
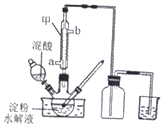
实验室用硝酸氧化淀粉水解液法制备草酸,装罝如图所示:
①一定量的淀粉水解液加入三颈烧瓶中
②控制反应温度55-60℃,边搅拌边缓慢滴加一定量的混合酸
③反应3小时,冷却,抽滤后再重结晶得到草酸晶体.
(1)右图实验装置中仪器甲的名称为冷凝管.冷凝水的进口是a(填“a”或“b”).
(2)检验淀粉是否水解完全所需要的试剂为碘水或I2.
实验Ⅱ:探究草酸与酸性高锰酸钾溶液的反应
(3)向草酸溶液中逐滴加入硫酸酸化的高锰酸钾溶液时,可观察到溶液由紫红色变为近乎无色,可推测草酸可能具有还原性.反应速率开始很慢,后来逐渐加快,可能的原因是生成的硫酸锰或锰离子对反应有催化作用,加快反应速率.写出反应的离子方程式5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O.
实验Ⅲ:草酸性质的应用
利用比H2C2O4与酸性KMnO4溶液反应探究“条件对化学反应速率的影响.”实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢.设计方案如下:
(4)为了观察到紫色褪去,H2C2O4与KMnO4溶液初始的物质的量需要满足的关系为n(H2C2O4):n(KMnO4)≥2.5.
(5)探究温度对化学反应速率影响的实验编号是乙和丙,探究反应物浓度对化学反应速率影响的实验编号是甲和乙
实验Ⅳ:草酸晶体中结晶水测定
草酸晶体的化学式可表示为H2C2O4•xH2O,为测定x的值,进行下列实验:
①称取6.3g某草酸晶体配成100.0mL的水溶液.
②取25.00mL所配溶液置于锥形瓶中,加入适量稀H2SO4,用浓度为0.5mol/L的KMnO4溶液滴定,滴定终点时消耗KMnO4的体积为10.00mL.
(6)计算x=2.
 草酸(H2C2O4)是一种重要的有机化工原料.为探究草酸的制取、性质及应用,进行如下实验.
草酸(H2C2O4)是一种重要的有机化工原料.为探究草酸的制取、性质及应用,进行如下实验.实验Ⅰ:草酸晶体的制备
实验室用硝酸氧化淀粉水解液法制备草酸,装罝如图所示:
①一定量的淀粉水解液加入三颈烧瓶中
②控制反应温度55-60℃,边搅拌边缓慢滴加一定量的混合酸
③反应3小时,冷却,抽滤后再重结晶得到草酸晶体.
(1)右图实验装置中仪器甲的名称为冷凝管.冷凝水的进口是a(填“a”或“b”).
(2)检验淀粉是否水解完全所需要的试剂为碘水或I2.
实验Ⅱ:探究草酸与酸性高锰酸钾溶液的反应
(3)向草酸溶液中逐滴加入硫酸酸化的高锰酸钾溶液时,可观察到溶液由紫红色变为近乎无色,可推测草酸可能具有还原性.反应速率开始很慢,后来逐渐加快,可能的原因是生成的硫酸锰或锰离子对反应有催化作用,加快反应速率.写出反应的离子方程式5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O.
实验Ⅲ:草酸性质的应用
利用比H2C2O4与酸性KMnO4溶液反应探究“条件对化学反应速率的影响.”实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢.设计方案如下:
| 编号 | H2C2O4溶液 | 酸性高锰酸钾溶液 | 温度/℃ | ||
| 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-l | 体积/mL | ||
| 甲 | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| 乙 | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| 丙 | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
(5)探究温度对化学反应速率影响的实验编号是乙和丙,探究反应物浓度对化学反应速率影响的实验编号是甲和乙
实验Ⅳ:草酸晶体中结晶水测定
草酸晶体的化学式可表示为H2C2O4•xH2O,为测定x的值,进行下列实验:
①称取6.3g某草酸晶体配成100.0mL的水溶液.
②取25.00mL所配溶液置于锥形瓶中,加入适量稀H2SO4,用浓度为0.5mol/L的KMnO4溶液滴定,滴定终点时消耗KMnO4的体积为10.00mL.
(6)计算x=2.
10.下列粒子中的原子均达到8电子结构的是( )
| A. | BCl3 | B. | CO2 | C. | NH3 | D. | NO2 |
17.25℃时,用0.100mol/L的盐酸滴定10.00mL0.100mol/L的Na2CO3溶液,滴定曲线如图所示.下列说法正确的是( )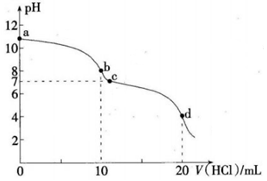

| A. | a、d 两点溶液中水电离出的c(H+):a<d | |
| B. | b点溶液存在:c(CO32-)+c(HCO3-)+c(H2CO3)=0.100mol/L | |
| C. | c点溶液存在:c(Na+)-c(Cl-)=c(HCO3-)+2c(CO32-) | |
| D. | b点溶液加水稀释过程中,溶液的pH不断升高 |
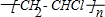 .
.