9.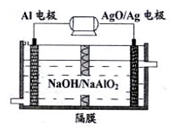 铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.下列说法不正确的是( )
铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.下列说法不正确的是( )
 铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.下列说法不正确的是( )
铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.下列说法不正确的是( )| A. | 在正极发生的电极反应为:AgO+2e-+H2O=Ag+2OH- | |
| B. | 在正极区H+浓度增大,在负极区H+浓度减少 | |
| C. | 该电池总反应的化学方程式:2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O | |
| D. | 当电池负极的质量变化10.8g,则过程中电池流动的电子物质的量为1.2NA |
7.在容积不变的密闭容器中发生反应:N2(g)+3H2(g)?2NH3(g),反应达平衡状态的标志是( )
①单位时间内生成n mol N2的同时生成2n mol NH3
②用N2、H2、NH3的物质的量浓度变化表示的反应速率比为1:3:2的状态
③2v(H2)正=3v(NH3)逆
④混合气体的密度不再改变的状态
⑤混合气体的平均相对分子质量不再改变的状态.
①单位时间内生成n mol N2的同时生成2n mol NH3
②用N2、H2、NH3的物质的量浓度变化表示的反应速率比为1:3:2的状态
③2v(H2)正=3v(NH3)逆
④混合气体的密度不再改变的状态
⑤混合气体的平均相对分子质量不再改变的状态.
| A. | ①③④ | B. | ②③⑤ | C. | ①③⑤ | D. | ①②③④⑤ |
6.将4mol A气体和2mol B气体在2L的容器中混合,并在一定条件下发生如下反应:2A(g)+B(g)=2C(g),若经2s后测得C的物质的量为0.6mol.下列叙述正确的是( )
| A. | 用物质C表示的反应的平均速率为0.3 mol•L-1•s-1 | |
| B. | 反应开始到2 s,物质B的物质的量浓度减少了0.85 mol/L | |
| C. | 2 s时物质A的转化率为15% | |
| D. | 2v(A)=v(B) |
5.在一个密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g).已知反应过程中的某一时间SO2、O2和SO3的浓度分别为:0.2mol/L、0.1mol/L和0.2mol/L.当反应达到平衡时可能存在的数据正确的是( )
| A. | c(O2)=0.2 mol/L | B. | c(SO2)=0.25 mol/L | ||
| C. | c(SO2)+c(SO3)=0.3 mol/L | D. | c(SO2)=c(SO3)=0.15 mol/L |
3.设N0为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A. | 0.5 摩1,3-丁二烯分子中含有共价键数为5.5N0 | |
| B. | 1 mol甲基(-CH3)所含的电子总数为9N0 | |
| C. | 1 mol-OH和1 mol OH-所含电子数都为9N0 | |
| D. | 1 mol碳正离子(CH3+)所含的电子总数为8N0 |
2.下列物质一定属于同系物的是( )
①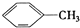
②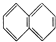
③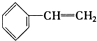
④C2H4
⑤CH2=CH-CH=CH2
⑥C3H6
⑦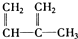
⑧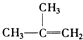
①

②

③

④C2H4
⑤CH2=CH-CH=CH2
⑥C3H6
⑦
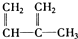
⑧

| A. | ④和⑧ | B. | ①、②和③ | C. | ④和⑤ | D. | ④、⑥和⑧ |
1.下列溶液中,不能区别SO2和CO2气体的是( )
①石灰水 ②H2S溶液 ③KMnO4溶液 ④氯水 ⑤酸化的Ba(NO3)2溶液 ⑥品红溶液.
①石灰水 ②H2S溶液 ③KMnO4溶液 ④氯水 ⑤酸化的Ba(NO3)2溶液 ⑥品红溶液.
| A. | ①②③⑤ | B. | ②③④⑤ | C. | 只有① | D. | ①③ |
2.已知常温下0.1mol•L-1NH4HCO3溶液的pH=7.8,溶液中含氮(或含碳)各微粒的分布分数(平衡时某种微粒的浓度占各种微粒浓度之和的分数)与pH的关系如图所示.下列说法正确的是( )

0 162419 162427 162433 162437 162443 162445 162449 162455 162457 162463 162469 162473 162475 162479 162485 162487 162493 162497 162499 162503 162505 162509 162511 162513 162514 162515 162517 162518 162519 162521 162523 162527 162529 162533 162535 162539 162545 162547 162553 162557 162559 162563 162569 162575 162577 162583 162587 162589 162595 162599 162605 162613 203614

| A. | 常温下,碳酸的第一、二步电离常数之比为K1:K2=102.9 | |
| B. | NH4HCO3溶液中:c(HCO3-)>c(NH4+)>c(OH-)>c(H+) | |
| C. | NH4HCO3溶液中:c(NH4+)+c(NH3•H2O)+c(H+)=c(CO32-)+c(H2CO3)+c(HCO3-)+c(OH-) | |
| D. | 常温下,NH3•H2O的电离常数大于H2CO3的第一步电离常数 |