题目内容
7.在容积不变的密闭容器中发生反应:N2(g)+3H2(g)?2NH3(g),反应达平衡状态的标志是( )①单位时间内生成n mol N2的同时生成2n mol NH3
②用N2、H2、NH3的物质的量浓度变化表示的反应速率比为1:3:2的状态
③2v(H2)正=3v(NH3)逆
④混合气体的密度不再改变的状态
⑤混合气体的平均相对分子质量不再改变的状态.
| A. | ①③④ | B. | ②③⑤ | C. | ①③⑤ | D. | ①②③④⑤ |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:①单位时间内生成n mol N2的等效于消耗2n mol NH3的同时生成2n mol NH3,正逆反应速率相等,达平衡状态,故正确;
②用N2、H2、NH3的物质的量浓度变化表示的反应速率比为1:3:2的状态,并不是浓度不变的状态,故错误;
③2v(H2)正=3v(NH3)正=3v(NH3)逆,正逆反应速率相等,达平衡状态,故正确;
④混合气体的密度一直不随时间的改变的状态,故错误;
⑤混合气体的平均相对分子质量不再改变的状态,说明气体的物质的量不变,反应达平衡状态,故正确;
故选C.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
相关题目
19.下列化合物的核磁共振氢谱出现两组峰,且峰面积之比为1:1的是( )
| A. | 乙醚 | B. | 乙醇 | C. | 乙酸乙酯 | D. |  |
20.Fe2+检验的方法正确的是( )
| A. | 滴加氢氧化钠溶液 | B. | 先滴加KSCN溶液,再滴加盐酸 | ||
| C. | 滴加KSCN溶液 | D. | 先滴加氯水,再滴加KSCN溶液 |
17.向溶液中加入新物质时,其导电性(I)符合图变化趋势的实验操作是( )
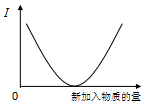

| A. | 乙酸溶液中通入氨气至过量 | B. | 石灰水中通入CO2至过量 | ||
| C. | 亚硫酸中通入氯气至过量 | D. | 氨水中通入氯化氢气体 |
2.下列物质一定属于同系物的是( )
①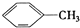
②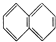
③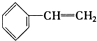
④C2H4
⑤CH2=CH-CH=CH2
⑥C3H6
⑦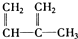
⑧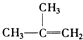
①

②

③

④C2H4
⑤CH2=CH-CH=CH2
⑥C3H6
⑦
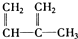
⑧

| A. | ④和⑧ | B. | ①、②和③ | C. | ④和⑤ | D. | ④、⑥和⑧ |
12.某溶液中含有大量的Cl-、CO32-、SO42-等三种阴离子.如果只取一次该溶液就能够分别将三种阴离子依次检验出来,下列实验操作顺序正确的是( )
①滴加HNO3溶液 ②过滤 ③滴加AgNO3溶液 ④滴加Ba(NO3)2溶液.
①滴加HNO3溶液 ②过滤 ③滴加AgNO3溶液 ④滴加Ba(NO3)2溶液.
| A. | ①④②③ | B. | ④②①③ | C. | ③②①④ | D. | ④②③②① |
19.下列有关Na2CO3和NaHCO3的叙述中,正确的是( )
| A. | 受热时,NaHCO3比Na2CO3容易分解 | |
| B. | NaHCO3俗名苏打,Na2CO3俗名纯碱 | |
| C. | NaHCO3溶液显酸性,Na2CO3溶液显碱性 | |
| D. | NaHCO3和Na2CO3各1mol分别与过量盐酸反应,产生CO2的质量不同 |
16.如图,CPAE是蜂胶的主要活性成分,也可由咖啡酸合成.下列说法不正确的是( )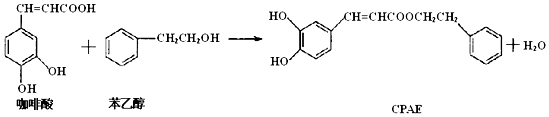

| A. | 咖啡酸分子中所有碳原子可能处在同一个平面上 | |
| B. | 1 mol CPAE与足量的溴水反应,最多消耗3molBr2 | |
| C. | 1 mol 苯乙醇在O2中完全燃烧,需消耗10 mol O2 | |
| D. | 1 mol CPAE与足量的NaOH溶液反应,最多消耗3 mol NaOH |
17.将一定量的由Cu和Cu2O组成的混合粉末加入到125mL2.6mol•L-1的硝酸中,固体恰好完全溶解,得蓝色溶液X并收集到VmL(标准状况)的纯净无色气体Y.下列结论正确的是( )
| A. | X中有两种溶质 | |
| B. | Y通入纯水中得到酸性溶液 | |
| C. | 原混合粉末的总质量小于7.8g | |
| D. | 当V=1680时,原混合粉末中Cu和Cu2O的物质的量之比为8:1 |