4.下列有关化学键的叙述,正确的是( )
| A. | 仅含有共价键的物质定是共价化合物 | |
| B. | 单质分子中均存在化学键 | |
| C. | 离子化合物中一定含有离子键,可能含有配位键和共价键 | |
| D. | 由不同种非属元素的原子形成的共价化合物一定只含极性键 |
3.若用E表示某原子中各轨道的能量,下列轨道能量大小顺序正确的是( )
| A. | E(3s)>E(3p)>E(3d) | B. | E(3s)>E(2s)>E(1s) | C. | E(4f)>E(4s)>E(3d) | D. | E(5s)>E(4s)>E(4f) |
2.0.2mol 气态燃料B2H6在氧气中燃烧,生成固态三氧化二硼和气态水,放出406.6kJ的热量,又知:H2O (l )═H2O(g)△H=+44kJ•mol-1,则B2H6的燃烧热为( )
| A. | 2165 kJ•mol-1 | B. | 2033 kJ•mol-1 | C. | 406.6 kJ•mol-1 | D. | 2077 kJ•mol-1 |
1.已知汽车尾气无害化处理反应为2NO(g)+2CO(g)?N2(g)+2CO2(g)△H<0.下列说法错误的是( )
| A. | 该反应常温下能自发进行,高温和催化剂只是加快反应的速率 | |
| B. | 该反应中反应物的总能量低于生成物的总能量 | |
| C. | 反应达到平衡后,NO的反应速率保持恒定 | |
| D. | 单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡 |
18.烷烃 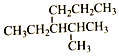 的命名正确的是( )
的命名正确的是( )
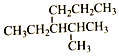 的命名正确的是( )
的命名正确的是( )| A. | 2-甲基-3-乙基己烷 | B. | 2-甲基-3-丙基戊烷 | ||
| C. | 3-异丙基己烷 | D. | 4-甲基-3-丙基戊烷 |
17.下列关于热化学方程式书写及对应表达均正确的是( )
| A. | 密闭容器中9.6克硫粉与11.2克铁粉混合加热生成硫化亚铁17.6克时放出19.12 kJ热量,则Fe(S)+S(S)=FeS(S)△H=-95.6 kJ•mol-1 | |
| B. | 稀醋酸和0.1mol/L的氢氧化钠溶液反应,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol | |
| C. | 已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g)△H=+285.5kJ/mol | |
| D. | 已知2C(s)+O2(g)=2CO(g)△H=-221 kJ/mol,则可知C的燃烧热△H=-110.5 kJ/mol |
16.反应2C+O2═2CO的能量变化如图所示.下列说法正确的是( )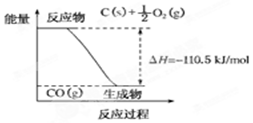
0 162277 162285 162291 162295 162301 162303 162307 162313 162315 162321 162327 162331 162333 162337 162343 162345 162351 162355 162357 162361 162363 162367 162369 162371 162372 162373 162375 162376 162377 162379 162381 162385 162387 162391 162393 162397 162403 162405 162411 162415 162417 162421 162427 162433 162435 162441 162445 162447 162453 162457 162463 162471 203614

| A. | 12g C(s)与一定量O2(g)反应生成14 g CO(g)放出的热量为110.5 kJ | |
| B. | 2 mol C(s)与足量O2(g)反应生成CO2(g),放出的热量大于221 kJ | |
| C. | 该反应的热化学方程式是2C(s)+O2(g)═2CO(g);△H=-221 kJ | |
| D. | 该反应的反应热等于CO分子中化学键形成时所释放的总能量与O2分子中化学键断裂时所吸收的总能量的差 |
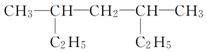 的名称为:3,5-二甲基庚烷.
的名称为:3,5-二甲基庚烷.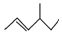 的分子式为:C7H14;名称为:4-甲基-2-己烯.
的分子式为:C7H14;名称为:4-甲基-2-己烯.