��Ŀ����
16����Ӧ2C+O2�T2CO�������仯��ͼ��ʾ������˵����ȷ���ǣ�������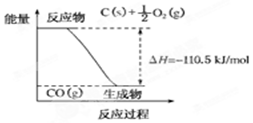
| A�� | 12g C��s����һ����O2��g����Ӧ����14 g CO��g���ų�������Ϊ110.5 kJ | |
| B�� | 2 mol C��s��������O2��g����Ӧ����CO2��g�����ų�����������221 kJ | |
| C�� | �÷�Ӧ���Ȼ�ѧ����ʽ��2C��s��+O2��g���T2CO��g������H=-221 kJ | |
| D�� | �÷�Ӧ�ķ�Ӧ�ȵ���CO�����л�ѧ���γ�ʱ���ͷŵ���������O2�����л�ѧ������ʱ�����յ��������IJ� |
���� ����ͼʾ��֪C��s��+$\frac{1}{2}$O2��g��=2CO��g����H=-110.5kJ/mol��Ϊ���ȷ�Ӧ���Ҹ÷�Ӧ�ķ�Ӧ�ȵ���O2���Ӻ�̼�л�ѧ������ʱ�����յ���������CO�����л�ѧ���γ�ʱ���ͷŵ��������IJ�Դ˽����⣮
��� �⣺A.12 g C��s����һ����O2��g����Ӧ����28 g CO��g���ų�������Ϊ110.5 kJ����Ӧ����14g CO��g��ʱ��12g̼δȫ����Ӧ����A����
B.2mol C��s��������O2��g����Ӧ����CO2��g������Ӧ������һ����̼���ɶ�����̼�Ƿ��ȷ�Ӧ�����Էų�����������221kJ����B��ȷ��
C���ʱ䵥λΪKJ/mol���ʸ÷�Ӧ���Ȼ�ѧ����ʽ��2C��s��+O2��g��=2CO��g����H=-221kJ/mol����C����
D���÷�Ӧ�ķ�Ӧ�ȵ���O2���Ӻ�̼�л�ѧ������ʱ�����յ���������CO�����л�ѧ���γ�ʱ���ͷŵ��������IJ��D����
��ѡB��
���� ���⿼�鷴Ӧ�����仯������Ϊ��Ƶ���㣬���ؿ���ѧ���ķ��������ͼ���������ע�ⷴӦ�ʱ�����ͼ��㷽����ͼ������жϣ���Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
7����������п�������Ļ��Լ�����ǿ����������п��ƷΪԭ���Ʊ���������п����������������ͼ��
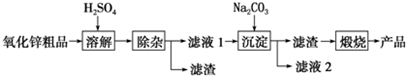
һЩ������������������ʽ��ȫ����ʱ��Һ��pH���±�
��1�����ܽ⡱ǰ������п��Ʒ�����ϸ������Ŀ���������Һ�Ӵ�������ӿ��ܽ�ʱ�ķ�Ӧ���ʣ�
��2���ܽ⡱��õ���������Һ�к���Zn2+��SO42-��������Fe2+��Cu2+�����ʣ��ȼ���Na2CO3���Na2CO3����H2SO4����������Һ��pH��5.4��Ȼ���������KMnO4��Fe2+ת��ΪFe��OH��3��ͬʱKMnO4 ת��ΪMnO2���������Һ��Fe2+��Ũ��Ϊ0.009mol•L-1����ÿ����Һ������Ӧ����0.003mol KMnO4��
��3������Cu2+�������û���Ӧ��ȥ��Ӧѡ����Լ���п�ۣ�
��4�����������õ�ZnCO3•2Zn��OH��2•H2O�������ա���450��500���½��У������ա���Ӧ�Ļ�ѧ����ʽΪ��ZnCO3•2Zn��OH��2•H2O$\frac{\underline{\;450�桫500��\;}}{\;}$3ZnO+CO2��+3H2O����
��5����֪������п�����ڰ�ˮ��п��������NH3�����γ��ĸ���λ���������ӣ���д��������п��NH3���ӷ�Ӧ�����ӷ���ʽZn��OH��2+4NH3=Zn��NH3��42++2OH-��
��6�����и����е�������Һ������μӵ�ʵ�鷽�����ɼ�����Ǣ٢ܣ�����ţ�
������������������ ���������Ͱ�ˮ ������п��̼���� ������п�Ͱ�ˮ��

һЩ������������������ʽ��ȫ����ʱ��Һ��pH���±�
| ������ | Fe��OH��3 | Cu��OH��2 | Zn��OH��2 | Fe��OH��2 |
| pH | 3.2 | 6.7 | 8.0 | 9.7 |
��2���ܽ⡱��õ���������Һ�к���Zn2+��SO42-��������Fe2+��Cu2+�����ʣ��ȼ���Na2CO3���Na2CO3����H2SO4����������Һ��pH��5.4��Ȼ���������KMnO4��Fe2+ת��ΪFe��OH��3��ͬʱKMnO4 ת��ΪMnO2���������Һ��Fe2+��Ũ��Ϊ0.009mol•L-1����ÿ����Һ������Ӧ����0.003mol KMnO4��
��3������Cu2+�������û���Ӧ��ȥ��Ӧѡ����Լ���п�ۣ�
��4�����������õ�ZnCO3•2Zn��OH��2•H2O�������ա���450��500���½��У������ա���Ӧ�Ļ�ѧ����ʽΪ��ZnCO3•2Zn��OH��2•H2O$\frac{\underline{\;450�桫500��\;}}{\;}$3ZnO+CO2��+3H2O����
��5����֪������п�����ڰ�ˮ��п��������NH3�����γ��ĸ���λ���������ӣ���д��������п��NH3���ӷ�Ӧ�����ӷ���ʽZn��OH��2+4NH3=Zn��NH3��42++2OH-��
��6�����и����е�������Һ������μӵ�ʵ�鷽�����ɼ�����Ǣ٢ܣ�����ţ�
������������������ ���������Ͱ�ˮ ������п��̼���� ������п�Ͱ�ˮ��
4����298K��1.01��105Pa�£���32g SO2ͨ��750mL 1mol•L-1 KOH��Һ�г�ַ�Ӧ����÷�Ӧ�ų�x kJ����������֪�ڸ������£�1mol SO2ͨ��1L 2mol•L-1KOH��Һ�г�ַ�Ӧ�ų�y kJ���������� SO2��KOH��Һ��Ӧ���� KHSO3���Ȼ�ѧ����ʽ��ȷ���ǣ�������
| A�� | SO2��g��+KOH ��aq���TKHSO3 ��aq����H=-��4x-y�� kJ•mol | |
| B�� | SO2��g��+KOH ��aq���TKHSO3 ��aq����H=-��2x-y�� kJ•mol-1 | |
| C�� | SO2��g��+KOH ��aq���TKHSO3 ��aq����H=-��2y-x�� kJ•mol | |
| D�� | 2SO2��g��+2KOH ��l���T2KHSO3 ��l����H=-��8x-2y�� kJ•mol-1 |
11�����з�Ӧ�������û���Ӧ���ǣ�������
| A�� | Fe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2 | B�� | 2Mg+CO2$\frac{\underline{\;��ȼ\;}}{\;}$C+2MgO | ||
| C�� | CuO+2HCl�TCuCl2+H2O | D�� | S+O2$\frac{\underline{\;��ȼ\;}}{\;}$SO2 |
1����֪����β������������ӦΪ2NO��g��+2CO��g��?N2��g��+2CO2��g����H��0������˵��������ǣ�������
| A�� | �÷�Ӧ���������Է����У����ºʹ���ֻ�Ǽӿ췴Ӧ������ | |
| B�� | �÷�Ӧ�з�Ӧ�������������������������� | |
| C�� | ��Ӧ�ﵽƽ���NO�ķ�Ӧ���ʱ��ֺ㶨 | |
| D�� | ��λʱ��������CO��CO2�����ʵ������ʱ����Ӧ�ﵽƽ�� |
8�����ڽ��壬����˵����ȷ���ǣ�������
| A�� | ����ľ۳��ǻ�ѧ�仯 | |
| B�� | ����0.01mol FeCl3����Һ�ƳɵĽ����У��������ӵ���ĿԼΪ6.02��1021�� | |
| C�� | ����Ľ������뽺������ֱ����С�й� | |
| D�� | NaCl����ȿ��Ƴ���Һ�ֿ��Ƴɽ��� |

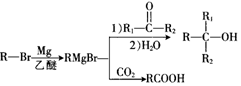
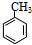 +Br2$\stackrel{FeBr_{3}}{��}$
+Br2$\stackrel{FeBr_{3}}{��}$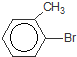 +HBr���䷴Ӧ����Ϊȡ����Ӧ
+HBr���䷴Ӧ����Ϊȡ����Ӧ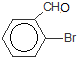
 ��H��һ�������»������ɸ߷��ӻ�����K��H����K�Ļ�ѧ����ʽΪ
��H��һ�������»������ɸ߷��ӻ�����K��H����K�Ļ�ѧ����ʽΪ
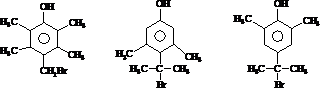
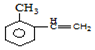 ����·������ͼ�������Լ���ѡ��
����·������ͼ�������Լ���ѡ��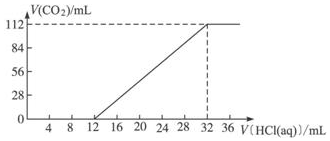 ��A�����Ԫ�أ�R����ɵ�����̼����R2CO3��RHCO3�Ļ����6.14g����ˮ�ܽ��ȡ������Һ��ʮ��֮һ�������л�������һ��Ũ�ȵ�ϡ���ᣬ��ͬʱ��¼�ų�CO2�������������ɱ�״���µ������������ϡ�����������õ���ͼ��ʾ�����ߣ�
��A�����Ԫ�أ�R����ɵ�����̼����R2CO3��RHCO3�Ļ����6.14g����ˮ�ܽ��ȡ������Һ��ʮ��֮һ�������л�������һ��Ũ�ȵ�ϡ���ᣬ��ͬʱ��¼�ų�CO2�������������ɱ�״���µ������������ϡ�����������õ���ͼ��ʾ�����ߣ�