题目内容
19.现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验.I、甲同学向1mol•L-1氯化铁溶液中加入少量的NaOH溶液;
II、乙同学直接加热饱和FeCl3溶液;
III、丙同学向25ml沸水中逐滴加入1~2mL FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热.试回答下列问题:
(1)其中操作正确的同学是丙;他的操作中涉及到的化学反应方程FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl
(2)证明有Fe(OH)3胶体生成的实验操作及现象是用激光笔照射,有一条明亮的光路,则有胶体生成
(3)丁同学利用所制得的Fe(OH)3胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带正电
②向其中加入稀硫酸,产生的现象是先生成红褐色的沉淀,后溶解为黄色溶液涉及的方程式是2Fe(OH)3+3H2SO4=Fe2(SO4)3+3H2O.
分析 (1)制备氢氧化铁胶体的方法:向25ml沸水中逐滴加入1~2mL FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热;
(2)只有胶体具有丁达尔效应,可以验证胶体的产生;
(3)胶体的电泳实验证明了胶体胶粒是带电的;加入稀硫酸,胶体先发生聚沉,氢氧化铁沉淀和稀硫酸进一步发生中和反应.
解答 解:(1)实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热,反应的化学方程式为FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$ Fe(OH)3(胶体)+3HCl,其它做法都不能生成胶体,往往得到沉淀,
故答案为:丙;FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$ Fe(OH)3(胶体)+3HCl;
(2)胶体具有丁达尔效应,当用激光笔照射时,会有一道明亮的光路,
故答案为:用激光笔照射,有一条明亮的光路,则有胶体生成;
(3)①Fe(OH)3胶粒带正电,通电时带正电荷的粒子向阴极移动,阴极附的颜色逐渐变深,
故答案为:Fe(OH)3胶粒带正电;
②向氢氧化铁胶体中逐滴加入过量H2SO4溶液,H2SO4电离出的SO42-使Fe(OH)3胶体发生聚沉,H+使Fe(OH)3沉淀溶解,会观察到先出现红褐色沉淀,后沉淀消失,方程式为2Fe(OH)3+3H2SO4=Fe2(SO4)3+3H2O,
故答案为:先生成红褐色的沉淀,后溶解为黄色溶液;2Fe(OH)3+3H2SO4=Fe2(SO4)3+3H2O.
点评 本题考查胶体的制备以及性质探究,为高频考点,侧重考查学生的分析能力和实验能力,题目难度不大,易错点为胶体的制备,注意制备方法.本题重点把握胶体的聚沉的性质.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
7.下列有关化学用语表示正确的是( )
| A. | 硫化钠的电子式: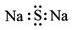 | B. | 中子数为10的氧原子:${\;}_8^{10}O$ | ||
| C. | 硫离子的结构示意图: | D. | HC1O的结构式:H-O-Cl |
14.少量铁粉与100mL 0.01mol/L的稀盐酸反应,反应速率太慢.为了加快此反应速率而不改变H2的产量,可以使用如下方法中的( )
①加H2O ②加NaOH固体 ③滴入几滴浓盐酸
④加CH3COONa固体 ⑤加NaCl溶液 ⑥滴入几滴硫酸铜溶液
⑦升高温度(不考虑盐酸挥发)
①加H2O ②加NaOH固体 ③滴入几滴浓盐酸
④加CH3COONa固体 ⑤加NaCl溶液 ⑥滴入几滴硫酸铜溶液
⑦升高温度(不考虑盐酸挥发)
| A. | ①⑥⑦ | B. | ③⑦ | C. | ③⑤⑥ | D. | ③⑥⑦ |
4.下列有关化学键的叙述,正确的是( )
| A. | 仅含有共价键的物质定是共价化合物 | |
| B. | 单质分子中均存在化学键 | |
| C. | 离子化合物中一定含有离子键,可能含有配位键和共价键 | |
| D. | 由不同种非属元素的原子形成的共价化合物一定只含极性键 |
9.下列各化合物的命名中正确的是( )
| A. | CH2=CH-CH=CH2 1,3-二丁烯 | B. | CH3-CH2-CH=CH2 3-丁烯 | ||
| C. | 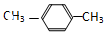 ,对二甲苯 ,对二甲苯 | D. | 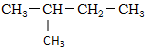 ,3-甲基丁烷 ,3-甲基丁烷 |