题目内容
2.0.2mol 气态燃料B2H6在氧气中燃烧,生成固态三氧化二硼和气态水,放出406.6kJ的热量,又知:H2O (l )═H2O(g)△H=+44kJ•mol-1,则B2H6的燃烧热为( )| A. | 2165 kJ•mol-1 | B. | 2033 kJ•mol-1 | C. | 406.6 kJ•mol-1 | D. | 2077 kJ•mol-1 |
分析 0.2mol 气态燃料B2H6在氧气中燃烧,生成固态三氧化二硼和气态水,放出406.6kJ的热量,则1mol气态燃料B2H6在氧气中燃烧,生成固态三氧化二硼和气态水,放出2033KJ的热量,反应的热化学方程式为:B2H6(g)+3O2(g)═B2O3(s)+3H2O(g)△H=-2033kJ/mol,又H2O (l )═H2O(g)△H=+44kJ•mol-1,而燃烧热指1mol燃料在氧气中安全燃烧生成稳定的化合物放出的热量,据此分析.
解答 解:0.2mol 气态燃料B2H6在氧气中燃烧,生成固态三氧化二硼和气态水,放出406.6kJ的热量,则1mol气态燃料B2H6在氧气中燃烧,生成固态三氧化二硼和气态水,放出2033KJ的热量,反应的热化学方程式为:B2H6(g)+3O2(g)═B2O3(s)+3H2O(g)△H=-2033kJ/mol,又H2O (l )═H2O(g)△H=+44kJ•mol-1,所以1mol气态燃料B2H6在氧气中燃烧,生成固态三氧化二硼和液态水,放出2033+44×3=2165KJ的热量,则B2H6的燃烧热为2165 kJ•mol-1,
故选:A.
点评 本题考查燃烧热的求算,题目难度不大,注意燃烧热指1mol燃料在氧气中安全燃烧生成稳定的化合物放出的热量,应该生成液态水.

练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
6.一种新储能电池如图所示.下列说法正确的是( )
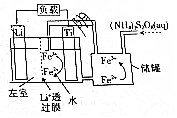

| A. | 左室电解质溶液为含Li+的水溶液 | |
| B. | 放电时,储罐中发生的离子反应为2Fe3++2SO42-═S2O82-+2Fe2+ | |
| C. | 充电时,钛极与外电源的负极相连 | |
| D. | 充电时发生的反应为Li++Fe2+$\frac{\underline{\;电解\;}}{\;}$Li+Fe3+ |
13.下列离子方程式书写正确的是( )
| A. | 已知电离常数H2SO3 K1=1.3×10-2 K2=6.3×10-8;H2CO3 K1=4.2×10-7 K2=5.6×10-11.H2SO3溶液和NaHCO3溶液反应:H2SO3+2HCO3-═SO32-+2CO2↑+2H2O | |
| B. | 控制pH为9~10,用NaClO溶液将含NaCN的废水中的CN-氧化为两种无污染的气体:2CN-+5ClO-+2H+═N2↑+2CO2↑+5Cl-+H2O | |
| C. | 已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液中,形成无色溶液.当Pb(CH3COO)2溶液中通入H2S气体时有黑色沉淀生成:Pb2++H2S═PbS↓+2H+ | |
| D. | CuSO4溶液与过量浓氨水反应:Cu2++4NH3•H2O═[Cu(NH3)4]2++4H2O |
10.VmL密度为ρg/mL的某溶液,含有相对分子质量为M的溶质mg,该溶液中溶质的质量分数为w%,物质的量浓度为cmol/L那么下列关系式正确的是( )
| A. | m=$\frac{{v}_{ρ}w}{1000}$ | B. | c=$\frac{(100{0}_{ρ}w)}{M}$ | C. | W%=[$\frac{cM}{1{0}_{ρ}}$]% | D. | C=$\frac{m}{VM}$ |
17.下列关于热化学方程式书写及对应表达均正确的是( )
| A. | 密闭容器中9.6克硫粉与11.2克铁粉混合加热生成硫化亚铁17.6克时放出19.12 kJ热量,则Fe(S)+S(S)=FeS(S)△H=-95.6 kJ•mol-1 | |
| B. | 稀醋酸和0.1mol/L的氢氧化钠溶液反应,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol | |
| C. | 已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g)△H=+285.5kJ/mol | |
| D. | 已知2C(s)+O2(g)=2CO(g)△H=-221 kJ/mol,则可知C的燃烧热△H=-110.5 kJ/mol |
14.用NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标况下,11.2L CO和N2混合气体中含有的原子数是NA | |
| B. | 100g 98%的浓硫酸中,氧原子总数为4NA | |
| C. | 1 mol•L-1的NaClO溶液中含有ClO-的数目小于NA | |
| D. | 1 mol SO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子 |
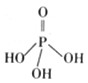 磷单质及其化合物的有广泛应用.
磷单质及其化合物的有广泛应用.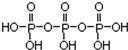 .三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10
.三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10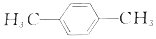 )与对苯二甲醛(
)与对苯二甲醛(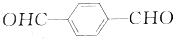 )均可被氧气直接氧化为对苯二甲酸,前后两种方案中,制备等量的对苯二甲酸时.理论上消耗的氧气物质的量之比为( )
)均可被氧气直接氧化为对苯二甲酸,前后两种方案中,制备等量的对苯二甲酸时.理论上消耗的氧气物质的量之比为( )