题目内容
1.已知汽车尾气无害化处理反应为2NO(g)+2CO(g)?N2(g)+2CO2(g)△H<0.下列说法错误的是( )| A. | 该反应常温下能自发进行,高温和催化剂只是加快反应的速率 | |
| B. | 该反应中反应物的总能量低于生成物的总能量 | |
| C. | 反应达到平衡后,NO的反应速率保持恒定 | |
| D. | 单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡 |
分析 A.2NO(g)+2CO(g)?N2(g)+2CO2(g)△H<0、△S<0,所以该反应常温下能自发进行,升高温度正逆反应速率都增大,使用催化剂能同等程度加快化学反应速率;
B.2NO(g)+2CO(g)?N2(g)+2CO2(g)△H<0,反应是放热反应,所以反应中反应物的总能量高于生成物的总能量;
C.反应达到平衡后,正逆反应速率相等,且不变;
D.达到平衡状态,单位时间内消耗CO和CO2的物质的量相等.
解答 解:A.2NO(g)+2CO(g)?N2(g)+2CO2(g)△H<0、△S<0,所以该反应常温下能自发进行,升高温度正逆反应速率都增大,使用催化剂能同等程度加快化学反应速率,所以升温和使用催化剂能加快化学反应的速率,故A正确;
B.2NO(g)+2CO(g)?N2(g)+2CO2(g)△H<0,反应是放热反应,所以反应中反应物的总能量高于生成物的总能量,而不是低于,故B错误;
C.反应达到平衡后,正逆反应速率相等,且不变,所以反应达到平衡后,NO的反应速率保持恒定,故C正确;
D.达到平衡状态,单位时间内消耗CO和CO2的物质的量相等,即正逆反应速率,所以能据此判断平衡状态,故D正确;
故选B.
点评 本题考查化学反应速率影响因素、化学平衡状态的判断等知识点,知道只有反应前后改变的物理量才能作为平衡状态的判断依据,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.NH3•H2O分子中NH3与H2O之间氢键表示为( )(填序号)
| A. | N-H••O | B. | O-H…N | C. | H-N…N | D. | H-O…H |
9.有机物的种类繁多,但其命名是有规则的.下列有机物命名正确的是( )
| A. |  2-乙基丁烷 2-乙基丁烷 | B. | CH3CHBr2 二溴乙烷 | ||
| C. | 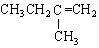 2-甲基丁烯 2-甲基丁烯 | D. | 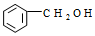 苯甲醇 苯甲醇 |
16.反应2C+O2═2CO的能量变化如图所示.下列说法正确的是( )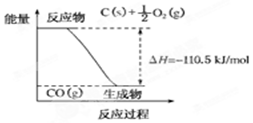

| A. | 12g C(s)与一定量O2(g)反应生成14 g CO(g)放出的热量为110.5 kJ | |
| B. | 2 mol C(s)与足量O2(g)反应生成CO2(g),放出的热量大于221 kJ | |
| C. | 该反应的热化学方程式是2C(s)+O2(g)═2CO(g);△H=-221 kJ | |
| D. | 该反应的反应热等于CO分子中化学键形成时所释放的总能量与O2分子中化学键断裂时所吸收的总能量的差 |
6.下列各组物质,前者是混合物,后者是纯净物的是( )
| A. | 胆矾 玻璃 | B. | 汽油 液氯 | C. | 石油 盐酸 | D. | 干冰 铝热剂 |
13.常温时,下列叙述正确的是( )
| A. | 稀释pH=3的醋酸,溶液中所有离子的浓度均降低 | |
| B. | 用标准盐酸滴定未知浓度的烧碱,滴定前仰视,滴定后俯视,烧碱浓度偏低 | |
| C. | pH均为11的NaOH和NH3•H2O溶液中,水的电离程度不相同 | |
| D. | 分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多 |
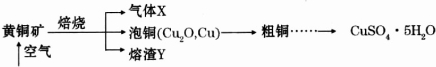

 (填写电子式).
(填写电子式).