题目内容
4.下列有关化学键的叙述,正确的是( )| A. | 仅含有共价键的物质定是共价化合物 | |
| B. | 单质分子中均存在化学键 | |
| C. | 离子化合物中一定含有离子键,可能含有配位键和共价键 | |
| D. | 由不同种非属元素的原子形成的共价化合物一定只含极性键 |
分析 A、仅含有共价键的物质可能是单质,也可能是化合物;
B、稀有气体分子中不存任何化学键;
C、离子化合物氯化铵中含有离子键、配位键和共价键;
D、氢和氧两种不同的非金属元素,形成的化合物过氧化氢分子中既含极性键氧氢键,也含非极性氧氧键.
解答 解:A、仅含有共价键的物质可能是单质,也可能是化合物,所以不一定是化合物,故A错误;
B、稀有气体分子中不存任何化学键,所以单质分子中不一定存在化学键,故B错误;
C、含有离子键的化合物是离子化合物,所以离子化合物中一定存在离子键,如离子化合物氯化铵中含有离子键、配位键和共价键,故C正确;
D、氢和氧两种不同的非金属元素,形成的化合物过氧化氢分子中既含极性键氧氢键,也含非极性氧氧键,所以不一定只含极性键,故D错误;
故选C.
点评 本题考查了物质和化学键的关系,根据物质的构成微粒确定化学键,并不是所有物质中都存在化学键,稀有气体中不存在化学键,只存在分子间作用力,为易错点.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目
8.二甲醚(CH3OCH3)-空气燃料电池的工作原理如图所示.电池工作时,下列说法正确的是( )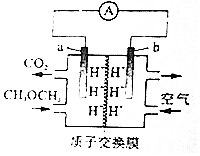

| A. | a极区域溶液的pH变大 | |
| B. | b极有H2O生成 | |
| C. | a极反应式:CH3OCH3+3O2--12e-═2CO2↑+6H+ | |
| D. | 每消耗11.2LO2(标准状况).有2molH+向左侧移动 |
15.对于反应A(g)+3B(g)═4C(g)+2D(g),在相同时间内,用不同物质表示的平均反应速率如下,则反应速率最快的是( )
| A. | v(A)=0.4 mol/(L•s) | B. | v(B)=0.8 mol/(L•s) | C. | v(C)=1.2 mol/(L•s) | D. | v(D)=0.7 mol/(L•s) |
16.NA为阿伏伽德罗常数的值,下列叙述错误的是( )
| A. | 18 g H2O中含的质子数为10 NA | |
| B. | 12 g金刚石含有的电子数为4 NA | |
| C. | 46 g NO2和N2O4混合气体中含有原子总数为3 NA | |
| D. | 23 g Na 与足量 O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
13.某研究小组通过实验探究Al、Fe、Cu及其化合物的性质,操作正确且能达到实验目的是( )
| A. | 将铝、铜、铁片插入浓硫酸,以证明常温下Al、Fe、Cu能否与浓硫酸反应 | |
| B. | 加过量NaOH溶液,过滤弃去沉淀,以除去混在Al2O3中的Fe2O3 | |
| C. | 将铁器、铜器放入盐酸中浸泡,以除去表面的铁锈和铜绿[Cu2(OH)2CO3] | |
| D. | 将FeCl3、CuCl2溶液在蒸发皿中加热蒸干,以制得FeCl3、CuCl2固体 |
14.下列分子中的σ键是由两个原子的s、p轨道以“头碰头”方式重叠构建而成的是( )
| A. | H2 | B. | Cl2 | C. | NaH | D. | HF |