3.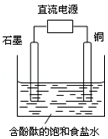 某小组设计电解饱和食盐水的装置如图,通电后两极均有气泡产生,下列叙述正确的是( )
某小组设计电解饱和食盐水的装置如图,通电后两极均有气泡产生,下列叙述正确的是( )
 某小组设计电解饱和食盐水的装置如图,通电后两极均有气泡产生,下列叙述正确的是( )
某小组设计电解饱和食盐水的装置如图,通电后两极均有气泡产生,下列叙述正确的是( )| A. | 铜是电解池的阳极 | B. | 石墨电极附近溶液呈红色 | ||
| C. | 铜电极上产生的是无色气体 | D. | 石墨电极上发生还原反应 |
2.下列元素属于ds区的是( )
| A. | Ca | B. | Fe | C. | Cu | D. | P |
1.在以下性质的比较中,正确的是( )
| A. | 微粒半径:Li+<O2-<F-<Na+ | B. | 电负性:F>N>O>C | ||
| C. | 分子中的键角:CO2>H2O>CH4>NH3 | D. | 共价键的键能:H-F>H-Cl>H-Br>H-I |
20.N2+3H2$?_{高温高压}^{催化剂}$2NH3制造氮肥的重要反应.下列关于该反应的说法正确的是( )
| A. | 增加N2的浓度能加快反应速率 | B. | 降低体系温度能加快反应速率 | ||
| C. | 使用催化剂不影响反应速率 | D. | N2足量时,H2能100%转化为NH3 |
18.下列现象不能用“相似相溶”解释的是( )
| A. | 二氧化硫易溶于水 | B. | 用CCl4 萃取碘水中的碘 | ||
| C. | 氯气易溶于NaOH溶液 | D. | 苯与水混合静置后分层 |
17.下列四种元素中,其单质氧化性最强的是( )
| A. | 原子中2p能级比2s能级多一个电子的第二周期元素 | |
| B. | 位于元素周期表中第三周期ⅢA族的元素 | |
| C. | 原子最外层电子排布为2s22p6的元素 | |
| D. | 原子最外层电子排布为2s22p5的元素 |
16.根据表(部分短周期元素的原子半径及主要化合价)信息,判断以下叙述中正确的是( )
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.186 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +1 | +3 | +2 | +6、-2 | -2 |
| A. | 最高价氧化物对应水化物的碱性A<C | |
| B. | 氢化物的稳定性H2D<H2E | |
| C. | 单质与稀盐酸反应的速率A<B | |
| D. | C2+与A+的核外电子数相等 |
15.从海带中提取碘,可经过一下实验不走完成.
海带$\stackrel{灼烧}{→}$海带灰$→_{溶解}^{30mL蒸馏水}$ $\stackrel{蒸沸}{→}$$\stackrel{过滤}{→}$ 滤液$→_{氧化}^{2mL稀H_{2}SO_{4},5mLH_{2}O_{3}}$
( )
海带$\stackrel{灼烧}{→}$海带灰$→_{溶解}^{30mL蒸馏水}$ $\stackrel{蒸沸}{→}$$\stackrel{过滤}{→}$ 滤液$→_{氧化}^{2mL稀H_{2}SO_{4},5mLH_{2}O_{3}}$

( )
| A. | 在灼烧过程中使用的玻璃仪器有酒精灯、玻璃棒、坩埚 | |
| B. | 在上述氧化过程中发生反应的离子方程式为2I-+H2O2→I2+2OH- | |
| C. | 检验碘单质时,可选用淀粉碘化钾试纸,若试纸变蓝说明有碘单质 | |
| D. | 在分液时,待下层液体完全流出后,关闭旋塞,上层液体从上口倒出 |
14.化学与生产、生活密切相关.下列表示符合化学事实的是( )
0 162201 162209 162215 162219 162225 162227 162231 162237 162239 162245 162251 162255 162257 162261 162267 162269 162275 162279 162281 162285 162287 162291 162293 162295 162296 162297 162299 162300 162301 162303 162305 162309 162311 162315 162317 162321 162327 162329 162335 162339 162341 162345 162351 162357 162359 162365 162369 162371 162377 162381 162387 162395 203614
| A. | HDO与H2O化学性质不同 | |
| B. | 用漂粉精和洁厕灵(主要成分是盐酸)混合后的浓溶液清洗马桶效果更佳 | |
| C. | 工业上最理想的化学反应是原子利用率达到100%的反应 | |
| D. | 新原子的发现意味着新元素的合成 |
 .
. .
.