4.乙酸和乙醛的鉴别有多种方法,下列可行的操作中最不简便的一种是( )
| A. | 使用蒸馏水 | B. | 使用NaHCO3溶液 | ||
| C. | 使用CuSO4和NaOH溶液 | D. | 使用pH试纸 |
3.下列关于有机化合物的结构、性质的叙述正确的是( )
| A. | 松油醇的结构简式为 ,则其同分异构体可能属于醛类、酮类或芳醇类 ,则其同分异构体可能属于醛类、酮类或芳醇类 | |
| B. | 甲烷和氯气的反应与乙烯和Br2的反应属于同一类型的反应 | |
| C. | 分子式为C4H8O2且能与氢氧化钠溶液反应的有机物(不考虑立体异构和醛类物质)有6种 | |
| D. | 乙醇、乙酸均能与NaOH溶液反应,因为分子中均含有-OH |
2.下列实验操作与预期实验目的或所得实验结论一致的是( )
| 选项 | 实验操作 | 实验目的或结论 |
| A | 在少量无水乙醇中加入金属Na,缓慢生成可以在空气中燃烧的气体 | CH3CH2OH是弱电解质 |
| B | 将SO2气体通入紫色石蕊溶液中,观察溶液颜色的变化 | 能证明SO2具有漂白性 |
| C | 向2mL1mol•L-1NaOH溶液中先加入0.2mL1mol•L-1FeCl3溶液,再加入0.2mL1mol•L-1MgCl2溶液 | 证明Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| D | 向2mL品红溶液和2mL加入少许醋酸的品红溶液中分别滴入3滴“84”消毒液,观察红色褪色的快慢 | 证明溶液pH的减少,“84”消毒液的氧化能力增强 |
| A. | A | B. | B | C. | C | D. | D |
1.下列措施中,能使饱和食盐水中c(OH-)减小的是( )
| A. | 加热 | B. | 投入金属钠 | C. | 加入NaHSO4固体 | D. | 以惰性电极电解 |
20.下列说法正确的是( )
| A. | 纳米铁粉可以高效地去除被污染水体中的 Pb2+、Cu2+、Cd2+、Hg2+等重金属离子,其本质是纳米铁粉对重金属离子有较强的物理吸附 | |
| B. | 凡含有添加剂的食物对人体健康均有害,不宜食用 | |
| C. | 煤经过气化和液化等物理变化可以转化为清洁燃料 | |
| D. | 火力发电中,燃烧是使化学能转换为电能的关键 |
16.某化学兴趣小组学生设计了制取KClO3和氯水的实验(装置如图所示),并进行相关性质的探究.
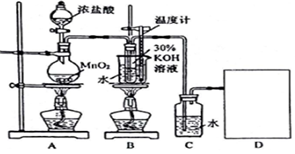
请按要求回答下列问题:
(1)请在D处方框内画出所需装置,并标注试剂名称.
装置A中发生反应的离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;当产生2.24mL(标准状况)Cl2时,转移电子数目为1.204×1022.
(2)B中反应的离子方程式:3Cl2+6OH-$\frac{\underline{\;\;△\;\;}}{\;}$5Cl-+ClO3-+3H2O.该小组学生深入研讨后将B和C装置对调了位置,这样做的优点是提高氯酸钾的纯度.
(3)制取实验结束后,取出上图B中试管,经冷却结晶、过滤、洗涤、干燥,得晶体样品.
另取图C中氯水样品,进行如下实验,请分析:
①在少量样品中滴入几滴石蕊溶液后的现象是溶液先变红后褪色.
②测定其中所含氯元素的总量;在一定量试样中加入足量的H2O2溶液,充分反应后加热除去过量的H2O2,冷却,在加入足量的硝酸银溶液,经系列操作后,称取沉淀质量.其中加入的H2O2溶液的作用是将氯气、次氯酸、次氯酸根离子还原为氯离子.
(4)欲证明相同条件下HClO的电离常数大于HCO3-,实验方案是分别测同温度物质的量浓度的次氯酸钠和碳酸氢钠溶液的pH.
(5)在不同条件下KClO3可将KI氧化成I2或KIO3.该小组设计了系列实验研究反应条件对产物的影响,其中某系列实验数据记录如表(均室温下进行);
①此系列实验中a=9.0.此系列实验目的是探究其他条件不变时,硫酸浓度对该反应产物的影响.
②为使实验现象更加明显,此系列实验中还需添加的一种试剂是淀粉溶液.
0 162129 162137 162143 162147 162153 162155 162159 162165 162167 162173 162179 162183 162185 162189 162195 162197 162203 162207 162209 162213 162215 162219 162221 162223 162224 162225 162227 162228 162229 162231 162233 162237 162239 162243 162245 162249 162255 162257 162263 162267 162269 162273 162279 162285 162287 162293 162297 162299 162305 162309 162315 162323 203614

请按要求回答下列问题:
(1)请在D处方框内画出所需装置,并标注试剂名称.
装置A中发生反应的离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;当产生2.24mL(标准状况)Cl2时,转移电子数目为1.204×1022.
(2)B中反应的离子方程式:3Cl2+6OH-$\frac{\underline{\;\;△\;\;}}{\;}$5Cl-+ClO3-+3H2O.该小组学生深入研讨后将B和C装置对调了位置,这样做的优点是提高氯酸钾的纯度.
(3)制取实验结束后,取出上图B中试管,经冷却结晶、过滤、洗涤、干燥,得晶体样品.
另取图C中氯水样品,进行如下实验,请分析:
①在少量样品中滴入几滴石蕊溶液后的现象是溶液先变红后褪色.
②测定其中所含氯元素的总量;在一定量试样中加入足量的H2O2溶液,充分反应后加热除去过量的H2O2,冷却,在加入足量的硝酸银溶液,经系列操作后,称取沉淀质量.其中加入的H2O2溶液的作用是将氯气、次氯酸、次氯酸根离子还原为氯离子.
(4)欲证明相同条件下HClO的电离常数大于HCO3-,实验方案是分别测同温度物质的量浓度的次氯酸钠和碳酸氢钠溶液的pH.
(5)在不同条件下KClO3可将KI氧化成I2或KIO3.该小组设计了系列实验研究反应条件对产物的影响,其中某系列实验数据记录如表(均室温下进行);
| 实验 编号 | 试剂及其用量 | |||
| 0.2mol•L-1kJ/mL | KClO3(s)/g | 6.0mol•L-1H2SO4/mL | H2O/mL | |
| 1 | 1.0 | 0.1 | 0 | a |
| 2 | 1.0 | 0.1 | 3.0 | b |
| 3 | 1.0 | 0.1 | 6.0 | c |
| 4 | 1.0 | 0.1 | 9.0 | 0 |
②为使实验现象更加明显,此系列实验中还需添加的一种试剂是淀粉溶液.
 .
.
