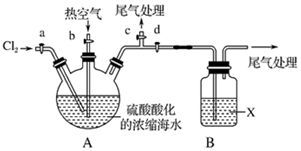
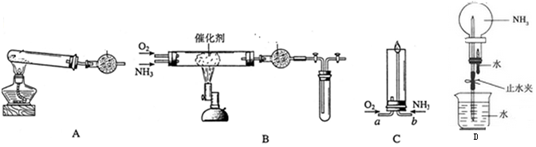
11.在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)?2Z(g)△H<0,3min时达到平衡.此时Y的物质的量为0.10mol.反应过程中测定的数据如下表,下列说法正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反应前3min的平均速率v(Z)=2.0×10-5 mol/(L•min) | |
| B. | 其他条件不变,降低温度,反应达到新平衡前v(正)>v(逆) | |
| C. | 升高温度,该反应的平衡常数将增大 | |
| D. | 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大 |
9.高铁酸钾(K2FeO4)是一种既能杀菌、消毒,又能絮凝净水的水处理剂.工业制备高铁酸钾反应的离子方程式为:Fe(OH)3+ClO-+OH-→FeO42-+Cl-+H2O(未配平)下列有关说法不正确的是( )
| A. | 由上述反应可知,ClO-的氧化性强于FeO42- | |
| B. | 高铁酸钾中铁显+6价 | |
| C. | 上述反应中氧化剂和还原剂的物质的量之比为2:3 | |
| D. | K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质 |
4.水资源非常重要,下列说法错误的是( )
| A. | 蒸馏法是海水谈化的方法之一 | |
| B. | 海水中的${\;}_{92}^{235}$U元素经浓缩提炼后可作核反应堆燃料 | |
| C. | 海水中的Li元素属于微量元素,提炼后可作Li电池原料 | |
| D. | 0℃以上,温度越高,水的密度越小 |
3.将Na、Al、Al2O3三种物质的混合物加入水中,完全反应后,所得溶液中只含有NaAlO2一种溶质,则Na、Al、Al2O3的物质的量之比可能是( )
| A. | 1:1:2 | B. | 1:4:1 | C. | 4:4:1 | D. | 4:2:1 |
2.常温下,用0.1mol/L的盐酸滴定a mL NaOH稀溶液.反应恰好完全时,消耗盐酸b mL.此时溶液时中c (OH-)是( )
0 162053 162061 162067 162071 162077 162079 162083 162089 162091 162097 162103 162107 162109 162113 162119 162121 162127 162131 162133 162137 162139 162143 162145 162147 162148 162149 162151 162152 162153 162155 162157 162161 162163 162167 162169 162173 162179 162181 162187 162191 162193 162197 162203 162209 162211 162217 162221 162223 162229 162233 162239 162247 203614
| A. | 1.0×10-7 mol/L | B. | 1.0×107 mol/L | C. | $\frac{0.1}{a}$mol/L | D. | $\frac{0.1b}{a+b}$mol/L |
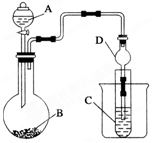 为探究元素的非金属性的变化规律,某化学兴趣小组同学设计了如下一系列实验,利用如图所示装置:
为探究元素的非金属性的变化规律,某化学兴趣小组同学设计了如下一系列实验,利用如图所示装置: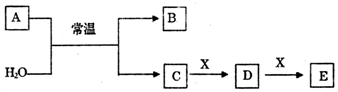
 .
.