11.下列有关实验的选项正确的是( )
| A装置实验说明 Ksp(AgCl)>Ksp(Ag2S) | B.制备Fe(OH)2沉淀 | C.苯萃取碘水中的I2,分出水层后的操作 | D.记录滴定终点读数 为12.20mL |
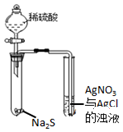 | 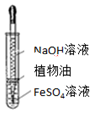 | 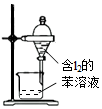 | 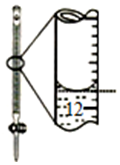 |
| A. | A | B. | B | C. | C | D. | D |
10.下列与化学有关的说法中正确的是( )
| A. | 在0.1mol/lHNO3溶液中加入FeCO3粉末,发生反应的离子方程式为:2FeCO3+2H+═2Fe2++CO2↑+H2O | |
| B. | 在$\frac{c(O{H}^{-})}{c({H}^{+})}$=1010的溶液中NO3-、I-、Na+、SO42-不能大量共存 | |
| C. | 25℃时pH=13的NaOH溶液中含有OH-的数目为0.1 NA | |
| D. | 闭容器中2molNO与1molO2充分反应,产物的分子数小于2NA |
8.利用湿法炼锌产生的铜镉渣生产金属镉的流程如图:已知铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质.
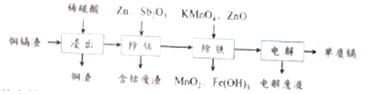
表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1mol•L-1计算):
(1)为了提高铜镉渣浸出的速率,可采取的措施有:①适当升高温度;②搅拌;③等.已知浸出的金属离子均为二价,写出浸出钴的化学方程式Co+H2SO4=CoSO4+H2↑
(2)除钴的过程中,需要加入活化剂Sb2O3,锌粉会与Sb2O3等形成微电池产生合金CoSb.该微电池的正极反应式为Sb2O3+Co2++6H++10e-=2CoSb+3H2O
(3)除铁的过程分两步进行,①加入适量KMnO4,发生反应的离子方程式为3Fe2++MnO4-+4H+=3Fe3++MnO2+2H2O,②加入ZnO控制反应液的PH范围为3.3-7.2
(4)除铁过程第①步,若加入KMnO4时条件控制不当,MnO2会继续反应,造成的结果是,若加入的KMnO4不足量,则待电解溶液中有Fe元残余.请设计实验方案加以验证.
(5)净化后的溶液用惰性电极电解可获得镉单质.电解废液中可循环利用的溶质是H2SO4
(6)处理含镉废水常用化学沉淀法,以下是几种镉的难溶化合物的溶度积常数(25℃):
Kap(CdCO3)=5.2×10-12
Kap(CdS)=3.6×10-29
Kap(Cd(OH)2)=2.0×10-16,根据上述信息:
沉淀Cd2+效果最佳的试剂是b
a.Na2CO3 b.Na2S c.CaO
若采用生石灰处理含镉废水最佳PH为11,此时溶液中c(Cd2+)=2.0×10-10 mol•L-1.

表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1mol•L-1计算):
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 | Mn(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.2 | 8.2 |
| 沉淀完全的pH | 3.3 | 9.9 | 9.5 | 10.6 |
(2)除钴的过程中,需要加入活化剂Sb2O3,锌粉会与Sb2O3等形成微电池产生合金CoSb.该微电池的正极反应式为Sb2O3+Co2++6H++10e-=2CoSb+3H2O
(3)除铁的过程分两步进行,①加入适量KMnO4,发生反应的离子方程式为3Fe2++MnO4-+4H+=3Fe3++MnO2+2H2O,②加入ZnO控制反应液的PH范围为3.3-7.2
(4)除铁过程第①步,若加入KMnO4时条件控制不当,MnO2会继续反应,造成的结果是,若加入的KMnO4不足量,则待电解溶液中有Fe元残余.请设计实验方案加以验证.
(5)净化后的溶液用惰性电极电解可获得镉单质.电解废液中可循环利用的溶质是H2SO4
(6)处理含镉废水常用化学沉淀法,以下是几种镉的难溶化合物的溶度积常数(25℃):
Kap(CdCO3)=5.2×10-12
Kap(CdS)=3.6×10-29
Kap(Cd(OH)2)=2.0×10-16,根据上述信息:
沉淀Cd2+效果最佳的试剂是b
a.Na2CO3 b.Na2S c.CaO
若采用生石灰处理含镉废水最佳PH为11,此时溶液中c(Cd2+)=2.0×10-10 mol•L-1.
7.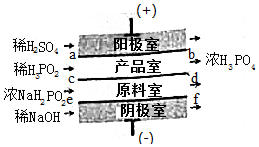 次磷酸(H3PO2)位一元酸,具有较强的还原性.可利用NaH2PO2为原料,通过四室电渗析法制备,工作原理如图所示,采用惰性电极,ab,cd,ef均为只允许阳离子(或阴离子)通过的离子交换膜,分别称为阳膜(或阴离子),下列说法描述错误的是( )
次磷酸(H3PO2)位一元酸,具有较强的还原性.可利用NaH2PO2为原料,通过四室电渗析法制备,工作原理如图所示,采用惰性电极,ab,cd,ef均为只允许阳离子(或阴离子)通过的离子交换膜,分别称为阳膜(或阴离子),下列说法描述错误的是( )
 次磷酸(H3PO2)位一元酸,具有较强的还原性.可利用NaH2PO2为原料,通过四室电渗析法制备,工作原理如图所示,采用惰性电极,ab,cd,ef均为只允许阳离子(或阴离子)通过的离子交换膜,分别称为阳膜(或阴离子),下列说法描述错误的是( )
次磷酸(H3PO2)位一元酸,具有较强的还原性.可利用NaH2PO2为原料,通过四室电渗析法制备,工作原理如图所示,采用惰性电极,ab,cd,ef均为只允许阳离子(或阴离子)通过的离子交换膜,分别称为阳膜(或阴离子),下列说法描述错误的是( )| A. | 阳极室反应为:2H2O-4e-=O2↑+4H+ | |
| B. | ab,ef均为阳膜,cd为阴膜 | |
| C. | 若将稀H2SO4改为H3PO3,撤去ab膜,产品中总混有杂质的原因是:H3PO2在阳极放电而被氧化生成H3PO4 | |
| D. | 通电后产品室中的H+离子向原料室迁移 |
6.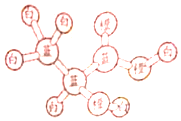 某有机物分子的球棍模型如图所示,图中“棍”代表化学键,不同颜色的“球”代表不同元素的原子,下列说法错误的是( )
某有机物分子的球棍模型如图所示,图中“棍”代表化学键,不同颜色的“球”代表不同元素的原子,下列说法错误的是( )
 某有机物分子的球棍模型如图所示,图中“棍”代表化学键,不同颜色的“球”代表不同元素的原子,下列说法错误的是( )
某有机物分子的球棍模型如图所示,图中“棍”代表化学键,不同颜色的“球”代表不同元素的原子,下列说法错误的是( )| A. | 1mol该有机物可与2molNa反应,生成1mol气体 | |
| B. | 该有机物可以发生加聚反应 | |
| C. | 该有机物可以发生取代反应,氧化反应、酯化反应 | |
| D. | 该有机物可以生成分子式为C6H8O4的酯 |
5.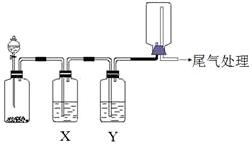 利用图装置可以进行实验并能达到实验目的是( )
利用图装置可以进行实验并能达到实验目的是( )
 利用图装置可以进行实验并能达到实验目的是( )
利用图装置可以进行实验并能达到实验目的是( )| 选项 | 实验目的 | X中试剂 | Y中试剂 |
| A | 用MnO2和浓盐酸制取并收集纯净干燥的Cl2 | 饱和食盐水 | 浓硫酸 |
| B | 用Cu与稀硝酸制取并收集纯净干燥的NO | 水 | 浓硫酸 |
| C | 用CaO于浓氨水制取并收集纯净干燥的NH3 | NaOH溶液 | 碱石灰 |
| D | CaCO3和稀盐酸制取并收集纯净干燥的CO2 | 饱和NaHCO3溶液 | 浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
4.下列物质的应用或现象解释正确的是( )
0 161795 161803 161809 161813 161819 161821 161825 161831 161833 161839 161845 161849 161851 161855 161861 161863 161869 161873 161875 161879 161881 161885 161887 161889 161890 161891 161893 161894 161895 161897 161899 161903 161905 161909 161911 161915 161921 161923 161929 161933 161935 161939 161945 161951 161953 161959 161963 161965 161971 161975 161981 161989 203614
| A. | 维生素C能促进人体对铁的吸收,利用了维生素C的氧化性 | |
| B. | 食品中大量添加苯甲酸钠灯防腐剂,可有效延长其保质期 | |
| C. | 《本草经集注》中记载了区别硝石(KNO3)和朴消(Na2SO4)的方法:“以火烧之,紫青烟起,乃真硝石也”,这是运用了焰色反应 | |
| D. | “从沙滩到用户”,计算机芯片的材料是指单质铁 |



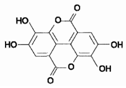 紫薯中的鞣花酸(结构如图)具有防癌和抗癌作用.
紫薯中的鞣花酸(结构如图)具有防癌和抗癌作用.
 .
.