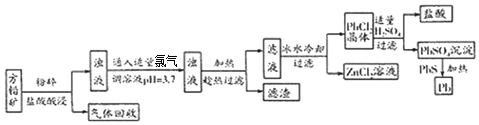
3.设NA代表阿伏加德罗常数,下列说法不正确的是( )
| A. | 1.5 mol NO2与足量的H2O反应,转移的电子数为NA | |
| B. | 常温常压下,0.5NA个CO2分子质量为22 g | |
| C. | 1 mol/L的CH3COOH中CH3COO-的浓度小于1 mol/L,而1 mol/L CH3COONa中CH3COO-等于1 mol/L | |
| D. | 18g 18O2中含有的中子数为10NA |
1.事实上,许多氧化物在一定条件下能与Na2O2反应,且反应极有规律,如Na2O2+SO2═Na2SO4,2Na2O2+2SO3═2Na2SO4+O2,据此你认为下列反应方程式中不正确的是( )
| A. | 2Na2O2+2N2O5═4NaNO3+O2↑ | B. | Na2O2+2NO2═2NaNO2+O2 | ||
| C. | Na2O2+N2O4═2NaNO3 | D. | 2Na2O2+2Mn2O7═4NaMnO4+O2↑ |
19.Al-Ag2O电池可用作水下动力电源,其原理如图所示,电池工作时,下列说法错误的是( )


| A. | 电子由Al电极通过外电路流向Ag2O/Ag电极 | |
| B. | 电池负极附近溶液pH升高 | |
| C. | 正极反应式为:Ag2O+2e-+H2O=2Ag+2OH- | |
| D. | 负极会发生副反应:2Al+2NaOH+2H2O═2NaAlO2+3H2↑ |
16.某化学兴趣小组的同学利用图所示实验装置进行实验.
(1)气体发生装置中反应的化学方程式是MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)实验室常用排饱和食盐水的方法来收集 Cl2,试用化学平衡原理加以解释因为饱和食盐水中 C(Cl-)较大,促使平衡 Cl2+H2O?H++Cl-+HClO逆向移动,减少Cl2 的溶解.
以下甲学生对 Cl2 与 FeCl2 和 KSCN 混合溶液的反应进行实验探究.
(3)A 中溶液变红的原因是Fe2+被Cl2氧化生成Fe3+,Fe3+与SCN-反应生成红色的硫氰化钾,所以溶液变红.
(4)为了探究现象 II 的原因,甲同学进行如下实验.
①取 A 中黄色溶液于试管中,加入 NaOH 溶液,有红褐色沉淀生成,则溶液中一定存在Fe3+.
②取 A 中黄色溶液于试管中,加入过量的 KSCN 溶液,最终得到红色溶液.
甲同学的实验证明产生现象Ⅱ的原因是 SCN-与 Cl2发生了反应.
(5)甲同学猜想 SCN-可能被 Cl2氧化了,他又进行了如下研究.
资料显示:SCN-的电子式为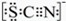
①甲同学认为 SCN-中碳元素没有被氧化,理由是SCN-中的碳元素是最高价态+4价.
②取 A 中黄色溶液于试管中,加入用盐酸酸化的 BaCl2溶液,产生白色沉淀,由此证明被氧化的元素是硫元素(填名称).
③通过实验证明了 SCN-中氮元素转化为 NO3-,他的实验方案是取足量铜粉于试管中,加入A中黄色溶液和一定量的稀盐酸,加热,观察到试管上方有红棕色气体生成,证明A中存在SCN-中氮元素被氧化成NO3-.中被氧化的元2
④若 SCN-与 Cl反应生成 CO2,写出反应离子方程式SCN-+8Cl2+9H2O=NO3-+SO42-+CO2+16Cl-+18H+,.
0 161738 161746 161752 161756 161762 161764 161768 161774 161776 161782 161788 161792 161794 161798 161804 161806 161812 161816 161818 161822 161824 161828 161830 161832 161833 161834 161836 161837 161838 161840 161842 161846 161848 161852 161854 161858 161864 161866 161872 161876 161878 161882 161888 161894 161896 161902 161906 161908 161914 161918 161924 161932 203614
| 操作 | 现象 |
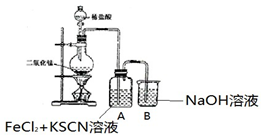 | I.A 中溶液变红 Ⅱ.稍后,溶液由红色变为黄色 |
(2)实验室常用排饱和食盐水的方法来收集 Cl2,试用化学平衡原理加以解释因为饱和食盐水中 C(Cl-)较大,促使平衡 Cl2+H2O?H++Cl-+HClO逆向移动,减少Cl2 的溶解.
以下甲学生对 Cl2 与 FeCl2 和 KSCN 混合溶液的反应进行实验探究.
(3)A 中溶液变红的原因是Fe2+被Cl2氧化生成Fe3+,Fe3+与SCN-反应生成红色的硫氰化钾,所以溶液变红.
(4)为了探究现象 II 的原因,甲同学进行如下实验.
①取 A 中黄色溶液于试管中,加入 NaOH 溶液,有红褐色沉淀生成,则溶液中一定存在Fe3+.
②取 A 中黄色溶液于试管中,加入过量的 KSCN 溶液,最终得到红色溶液.
甲同学的实验证明产生现象Ⅱ的原因是 SCN-与 Cl2发生了反应.
(5)甲同学猜想 SCN-可能被 Cl2氧化了,他又进行了如下研究.
资料显示:SCN-的电子式为
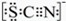
①甲同学认为 SCN-中碳元素没有被氧化,理由是SCN-中的碳元素是最高价态+4价.
②取 A 中黄色溶液于试管中,加入用盐酸酸化的 BaCl2溶液,产生白色沉淀,由此证明被氧化的元素是硫元素(填名称).
③通过实验证明了 SCN-中氮元素转化为 NO3-,他的实验方案是取足量铜粉于试管中,加入A中黄色溶液和一定量的稀盐酸,加热,观察到试管上方有红棕色气体生成,证明A中存在SCN-中氮元素被氧化成NO3-.中被氧化的元2
④若 SCN-与 Cl反应生成 CO2,写出反应离子方程式SCN-+8Cl2+9H2O=NO3-+SO42-+CO2+16Cl-+18H+,.
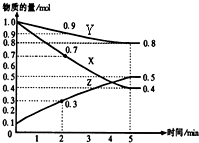 某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示:
某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示: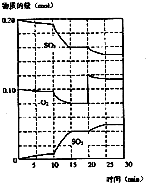 (1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示可逆反应的进行程度越大,K值大小与温度的关系是:温度升高,K值可能增大也可能减小(填一定增大、一定减小、或可能增大也可能减小).
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示可逆反应的进行程度越大,K值大小与温度的关系是:温度升高,K值可能增大也可能减小(填一定增大、一定减小、或可能增大也可能减小).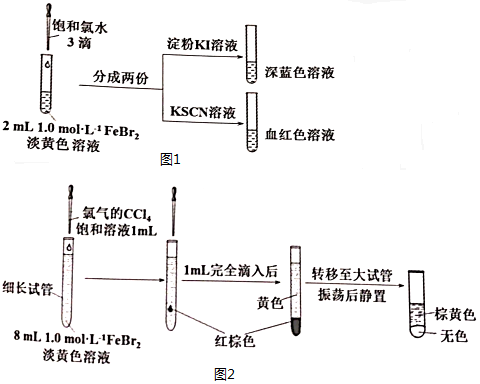
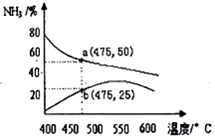 氨是一种重要的化工原料,也是重要的工业产品,在工农业生产和国防等领域发挥着重要作用.
氨是一种重要的化工原料,也是重要的工业产品,在工农业生产和国防等领域发挥着重要作用.