题目内容
16.某化学兴趣小组的同学利用图所示实验装置进行实验.| 操作 | 现象 |
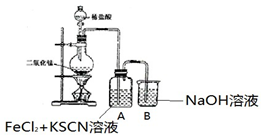 | I.A 中溶液变红 Ⅱ.稍后,溶液由红色变为黄色 |
(2)实验室常用排饱和食盐水的方法来收集 Cl2,试用化学平衡原理加以解释因为饱和食盐水中 C(Cl-)较大,促使平衡 Cl2+H2O?H++Cl-+HClO逆向移动,减少Cl2 的溶解.
以下甲学生对 Cl2 与 FeCl2 和 KSCN 混合溶液的反应进行实验探究.
(3)A 中溶液变红的原因是Fe2+被Cl2氧化生成Fe3+,Fe3+与SCN-反应生成红色的硫氰化钾,所以溶液变红.
(4)为了探究现象 II 的原因,甲同学进行如下实验.
①取 A 中黄色溶液于试管中,加入 NaOH 溶液,有红褐色沉淀生成,则溶液中一定存在Fe3+.
②取 A 中黄色溶液于试管中,加入过量的 KSCN 溶液,最终得到红色溶液.
甲同学的实验证明产生现象Ⅱ的原因是 SCN-与 Cl2发生了反应.
(5)甲同学猜想 SCN-可能被 Cl2氧化了,他又进行了如下研究.
资料显示:SCN-的电子式为
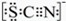
①甲同学认为 SCN-中碳元素没有被氧化,理由是SCN-中的碳元素是最高价态+4价.
②取 A 中黄色溶液于试管中,加入用盐酸酸化的 BaCl2溶液,产生白色沉淀,由此证明被氧化的元素是硫元素(填名称).
③通过实验证明了 SCN-中氮元素转化为 NO3-,他的实验方案是取足量铜粉于试管中,加入A中黄色溶液和一定量的稀盐酸,加热,观察到试管上方有红棕色气体生成,证明A中存在SCN-中氮元素被氧化成NO3-.中被氧化的元2
④若 SCN-与 Cl反应生成 CO2,写出反应离子方程式SCN-+8Cl2+9H2O=NO3-+SO42-+CO2+16Cl-+18H+,.
分析 (1)用浓盐酸与二氧化锰反应制取氯气,据此书写化学方程式;
(2)氯气与水反应生成盐酸和次氯酸,食盐水中含有氯离子,能抑制氯气的溶解;
(3)Fe2+被Cl2氧化生成Fe3+,Fe3+与SCN-反应生成红色的硫氰化铁溶液,呈红色,据此答题;
(4)①A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,应当是氢氧化铁固体,所以原溶液中应当有Fe3+,据此答题;
(5)①根据SCN-的电子式为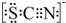 可知,SCN-中碳显+4价,硫显-2价,氮显-3价,碳已经是最高正价了,不能再被氧化了,据此答题;
可知,SCN-中碳显+4价,硫显-2价,氮显-3价,碳已经是最高正价了,不能再被氧化了,据此答题;
②加入用盐酸酸化的BaCl2溶液,产生白色沉淀,说明白色沉淀为硫酸钡,即溶液中有硫酸根离子,其中硫显+6价,而原来SCN-中硫显-2价,所以被氧化的元素为硫元素,据此答题;
③利用硝酸根离子在酸性条件下有强氧化性,遇到铜被还原,生成一氧化氮,在空气中被氧化成红棕色的二氧化氮气体,可以检验硝酸根离子的存在,据此答题;
④SCN-与Cl2反应生成硫酸根和硝酸根还有二氧化碳,据此书写离子方程式.
解答 解:(1)浓盐酸有还原性,二氧化锰有氧化性,浓盐酸和二氧化锰能发生氧化还原反应生成氯化锰、氯气和水,MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)浓盐酸易挥发,所以加热二氧化锰固体和浓盐酸制取氯气时,产生的氯气中容易混有氯化氢气体,要除去氯化氢气体,所选的除杂试剂只能吸收氯化氢而不能吸收氯气,排饱和食盐水的方法来收集氯气,是因Cl2+H2O?H++Cl-+HClO,加入食盐,氯离子浓度增大,化学平衡逆向移动,抑制氯气与水的反应,
故答案为:因为饱和食盐水中 C(Cl-)较大,促使平衡 Cl2+H2O?H++Cl-+HClO逆向移动,减少Cl2 的溶解;
(3)氯气具有强氧化性,则Fe2+被Cl2氧化生成Fe3+,离子方程式为:Cl2+2Fe2+=2C1-+2Fe3+,Fe3+与SCN-反应生成红色的硫氰化铁溶液,Fe3++3SCN-?Fe(SCN)3,呈红色,
故答案为:Fe2+被Cl2氧化生成Fe3+,Fe3+与SCN-反应生成红色的硫氰化钾,所以溶液变红;
(4)①A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,应当是氢氧化铁固体,所以原溶液中应当有Fe3+,
故答案为:Fe3+;
(5)①根据SCN-的电子式为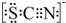 可知,SCN-中碳显+4价,硫显-2价,氮显-3价,碳已经是最高正价了,不能再被氧化了,
可知,SCN-中碳显+4价,硫显-2价,氮显-3价,碳已经是最高正价了,不能再被氧化了,
故答案为:SCN-中的碳元素是最高价态+4价;
②加入用盐酸酸化的BaCl2溶液,产生白色沉淀,说明白色沉淀为硫酸钡,即溶液中有硫酸根离子,其中硫显+6价,而原来SCN-中硫显-2价,所以被氧化的元素为硫元素,
故答案为:硫元素;
③利用硝酸根离子在酸性条件下有强氧化性,遇到铜被还原,生成一氧化氮,在空气中被氧化成红棕色的二氧化氮气体,可以检验硝酸根离子的存在,据此可知实验方案为:取足量铜粉于试管中,加入A中黄色溶液和一定量的稀盐酸,加热,观察到试管上方有红棕色气体生成,证明A中存在,SCN-中氮元素被氧化成NO3-,
故答案为:取足量铜粉于试管中,加入A中黄色溶液和一定量的稀盐酸,加热,观察到试管上方有红棕色气体生成,证明A中存在,SCN-中氮元素被氧化成NO3-;
④SCN-与Cl2反应生成硫酸根和硝酸根还有二氧化碳,所以它们反应的化学方程式为:SCN-+8Cl2+9H2O=NO3-+SO42-+CO2+16Cl-+18H+,
故答案为:SCN-+8Cl2+9H2O=NO3-+SO42-+CO2+16Cl-+18H+.
点评 本题考查了氯气的实验室制法、实验方案的设计与评价,考查较为综合,涉及到了离子的检验、氧化还原的离子方程式的书写、实验步骤的设计等知识点,熟练掌握元素化合物的基础知识及实验基本操作要求为解答关键,题目难度中等.

| A. | 分子 | B. | 元素 | C. | 原子 | D. | 单质 |
(2)25℃时,若向0.1mol/L氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=amol/L,则c(SO42-)=0.5amol/L.
(3)室温下,若向0.1mol/L氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,则所得溶液中各离子的物质的量浓度由大到小的顺序是c(NH4+)>c(SO42-)>c(H+)>c(OH-).
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量.已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×l0-10 |
| CH3COOH | K=1.8×l0-5 |
| H2CO3 | K1=4.3×l0-7、K2=5.6×l0-11 |
?25℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三溶液的pH由大到小的顺序为Na2CO3溶液>NaCN溶液>CH3COONa溶液.
?向NaCN溶液中通入少量CO2,所发生反应的化学方程式为:NaCN+H2O+CO2=HCN+NaHCO3.
(5)常温下,在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11.若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是1:4.
| A. | NaCl晶体 BaSO4 | B. | 铜 二氧化硫 | ||
| C. | 液态的醋酸 酒精 | D. | 熔融的KNO3 硫酸溶液 |
| A. | C3H6和C4H8互为同系物 | |
| B. | CH2Cl2有2种同分异构体 | |
| C. | 苯乙烯分子中的所有原子不可能处于同一个平面 | |
| D. | 乙酸与乙醇的酯化反应是可逆反应 |
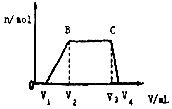 1L某混合溶液,可能含有的离子如表:
1L某混合溶液,可能含有的离子如表:| 可能大量含有的阳离子 | H+、K+、Mg2+、Al3+、NH4+、Fe2+、Fe3+ |
| 可能大量含有的阴离子 | Cl-、Br-、I-、CO32-、AlO2- |
(2)BC段离子方程式为NH4++OH-═NH3•H2O.
(3)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向1L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如表所示,分析后回答下列问题:
| Cl2的体积(标准状况) | 2.8L | 5.6L | 11.2L |
| n(Cl-) | 1.25mol | 1.5mol | 2mol |
| n(Br-) | 1.5mol | 1.4mol | 0.9mol |
| N(I-) | a mol | 0 | 0 |
②当通入Cl2的体积为2.8L时,溶液中发生反应的离子方程式为Cl2+2I-=I2+2Cl-.
③原溶液中Cl-、Br-、I-的物质的量浓度之比为10:15:4.
| A. | AlCl3溶液中加入过量氨水:A13++4 NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | NaA1O2溶液中AlO2-的水解:AlO2-+2H2O═A1(OH)3↓+OH- | |
| C. | AgCl悬浊液中加入KI溶液得到黄色沉淀:Ag++I-═AgI↓ | |
| D. | 明矾净水原理:A13++3H2O?A1(OH)3(胶体)+3H+ |
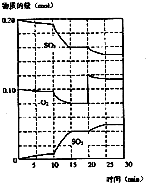 (1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示可逆反应的进行程度越大,K值大小与温度的关系是:温度升高,K值可能增大也可能减小(填一定增大、一定减小、或可能增大也可能减小).
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示可逆反应的进行程度越大,K值大小与温度的关系是:温度升高,K值可能增大也可能减小(填一定增大、一定减小、或可能增大也可能减小).