9.将一定量的氯气通入50mL 10.00mol•L-1的氢氧化钠浓溶液中,加热少许时间后,溶液中形成NaCl、NaClO、NaClO3共存体系(不考虑氯气和水的反应).下列说法正确的是( )
| A. | 若反应中转移的电子为nmol,则0.25<n<0.5 | |
| B. | 溶液中n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1 | |
| C. | 与NaOH反应的氯气物质的量:0.25 mol<n (Cl2)<0.75mol | |
| D. | 当溶液中n(NaClO):n(NaClO3)=5:1时,反应的离子方程式为:8Cl2+16OH-═10Cl-+5ClO-+ClO3-+8H2O |
8.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 足量Mg与2.8gN2完全反应后失去0.2NA电子 | |
| B. | 3.0g由葡萄糖和冰醋酸组成的混合物中含有的原子总数为0.3NA | |
| C. | 常温常压下,2.8gC2H4含有共用电子对的数目为0.6NA | |
| D. | 16gO2含有NA个18O原子 |
7.设NA为阿伏加德罗常数的值,下列叙述错误的是( )
| A. | 分子总数为NA的NO2和CO2的混合气体中含有的氧原子数为2 NA | |
| B. | 0.1 mol/L (NH4)2SO4溶液与0.2 mol/L NH4Cl溶液中的NH4+数目相同 | |
| C. | 标准状况下,H2和CO混合气体8.96 L在足量O2中充分燃烧消耗O2分子数为0.2 NA | |
| D. | 1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
6.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 30gSiO2晶体中含有NA个硅氧键 | |
| B. | 常温常压下,11.2LCl2含有的分子数目少于0.5NA | |
| C. | 25℃时,pH=12的NaOH溶液含有的OH-数目为0.01NA | |
| D. | 50mL18.4mol/L浓硫酸与足量铜微热,生成SO2分子的数目为0.46NA |
4.如图所示,△E1=393.5kJ,△E2=395.4kJ,下列说法正确的是( )
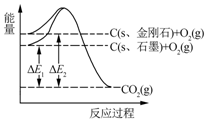

| A. | 1 mol石墨完全转化为金刚石需吸收1.9 kJ热量 | |
| B. | 石墨和金刚石的转化是物理变化 | |
| C. | 金刚石的稳定性强于石墨 | |
| D. | 1 mol金刚石和1 mol O2化学键断裂吸收的能量总和大于1 mol CO2分子中化学键断裂吸收的能量 |
3.下列有关实验操作、现象及结论的叙述正确的是( )
| A. | 用钠可以检验某无水酒精中是否含有水 | |
| B. | 140℃时,无水乙醇与浓硫酸共热可制备乙烯 | |
| C. | 制取乙酸乙酯时,试剂加入的顺序是:先加入乙醇,后慢慢加入浓硫酸,最后加入乙酸 | |
| D. | 在蔗糖溶液中加入少量稀硫酸,水浴加热后,再加入少量新制的氢氧化铜悬浊液,加热至沸腾,没有砖红色沉淀生成,说明蔗糖没有水解 |
2.设NA表示阿伏伽德罗常数值.下列说法正确的是( )
0 161686 161694 161700 161704 161710 161712 161716 161722 161724 161730 161736 161740 161742 161746 161752 161754 161760 161764 161766 161770 161772 161776 161778 161780 161781 161782 161784 161785 161786 161788 161790 161794 161796 161800 161802 161806 161812 161814 161820 161824 161826 161830 161836 161842 161844 161850 161854 161856 161862 161866 161872 161880 203614
| A. | 标准状况下,11.2L的甲醇所含的氢原子数等于2NA | |
| B. | 常温常压下,Na2O2 与 H2O 反应生成 1mol O2 时,转移电子数是 2NA | |
| C. | 25℃时,Kap(BaSO4)=1×10-10,则BaSO4饱和溶液中Ba2+数目为1×10-6 NA | |
| D. | 1L 1 mol/L AlCl3溶液中含有的Al3+数目为NA |

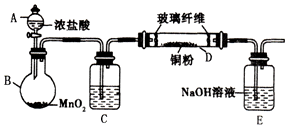 实验室采用如图所示的装置制取氯化铜(部分仪器和夹持装置已略去).
实验室采用如图所示的装置制取氯化铜(部分仪器和夹持装置已略去).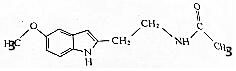 某保健品脑白金包装盒内附有一张产品说明书,其中给出了该产品的主要成分的结构简式(如图).
某保健品脑白金包装盒内附有一张产品说明书,其中给出了该产品的主要成分的结构简式(如图).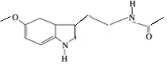 .
.