11.利用某有机物之间的转换可以贮存太阳能,如原降冰片二烯(NBD)经太阳光照可转化成四环烷(Q),其反应可表示为: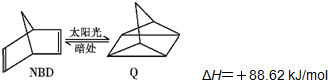 ,下列有关说法正确的是( )
,下列有关说法正确的是( )
 ,下列有关说法正确的是( )
,下列有关说法正确的是( )| A. | NBD和Q二者互为同分异构体 | |
| B. | 物质NBD的分子式为C7H7 | |
| C. | 物质Q的一氯取代物有2种 | |
| D. | 一定条件下,1molNBD最多可与2molBr2发生加成反应 |
8.Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色反应呈黄色,五种元素核电荷数之和为54,W、Z最外层电子数相同,Z的核电荷数是W的2倍,工业上一般通过电解氧化物的方法获得Y的单质,则下列说法不正确的是( )
| A. | 原子半径:X>Y>Z>Q>W | |
| B. | X、Y和Z三种元素的最高价氧化物的水化物两两间能反应 | |
| C. | 阳离子的氧化性:X>Y | |
| D. | W的最简单氢化物沸点比Z的高 |
7.设NA为阿伏加徳罗常数的值,下列说法正确的是( )
| A. | 23gNa与O2完全反应,生成Na2O和Na2O2的混合物,转移的电子数为NA | |
| B. | 88.0g14CO2与14N2O的混合物中所含中子数为44NA | |
| C. | 0.1L,l.0mol/L的NaAlO2水溶液中含有的氧原子数为0.2NA | |
| D. | 室温下,将1mol铁片投入到0.5L,18.4mol/L的硫酸中,转移的电子数为3NA |
6.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 5.6gFe在氧气中燃烧,完全反应时转移电子数为0.3NA | |
| B. | 标准状况下,4.48LCH3C1中所含原子数为NA | |
| C. | 1LpH=1的H2SO4溶液中含有的H+数为0.2NA | |
| D. | 常温下,1.7gNH3和3.65gHCl混合后,气体分子数为0.2NA |
5.下列物质分类正确的是( )
| A. | Na2O2、Fe3O4、CuO均为碱性氧化物 | B. | 盐酸、水玻璃、氨水均为混合物 | ||
| C. | 烧碱、冰醋酸、四氯化碳均为电解质 | D. | 稀豆浆、硅酸、氯化铁溶液均为胶体 |
4.下列化学反应中,属于氧化还原反应的是( )
| A. | Na2CO3+CaCl2═CaCO3↓+2NaCl | B. | Fe+CuSO4═Cu+FeSO4 | ||
| C. | 2NaHCO3═Na2CO3+CO2↑+H2O | D. | CaO+H2O═Ca(OH)2 |
3.设NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 1mol硫单质在过量氧气中燃烧产生NA个SO3分子 | |
| B. | 标准状况下,22.4LSO3中含有氧原子数为3NA | |
| C. | 标准状况下,18gH2O中含有氧原子数为NA | |
| D. | 5.4g铝单质与足量NaOH溶液反应,转移电子数为0.6NA |
2.下列有关物质的分类正确的是( )
0 161682 161690 161696 161700 161706 161708 161712 161718 161720 161726 161732 161736 161738 161742 161748 161750 161756 161760 161762 161766 161768 161772 161774 161776 161777 161778 161780 161781 161782 161784 161786 161790 161792 161796 161798 161802 161808 161810 161816 161820 161822 161826 161832 161838 161840 161846 161850 161852 161858 161862 161868 161876 203614
| A. | SO2、SiO2、CO均为酸性氧化物 | B. | 稀豆浆、硅酸、氯化铁溶液均为胶体 | ||
| C. | 硫酸、盐酸、氢氟酸均为强酸 | D. | 氯水、水玻璃、氨水均为混合物 |