题目内容
3.设NA代表阿伏加德罗常数,下列说法正确的是( )| A. | 1mol硫单质在过量氧气中燃烧产生NA个SO3分子 | |
| B. | 标准状况下,22.4LSO3中含有氧原子数为3NA | |
| C. | 标准状况下,18gH2O中含有氧原子数为NA | |
| D. | 5.4g铝单质与足量NaOH溶液反应,转移电子数为0.6NA |
分析 A.硫单质与氧气反应生成的是二氧化硫;
B.标准状况下三氧化硫的状态不是气体;
C.标况下水的状态不是气体;
D.铝为+3价金属,根据n=$\frac{m}{M}$计算出铝的物质的量,然后计算出转移电子的物质的量.
解答 解:A.1mol硫单质在过量氧气中燃烧产生1mol二氧化硫,产生NA个SO2分子,不会生成三氧化硫,故A错误;
B.标准状况下SO3不是气体,不能使用标况下的气体摩尔体积计算,故B错误;
C.标况下水不是气体,不能使用标况下的气体摩尔体积计算水的物质的量,故C错误;
D.5.4g铝的物质的量为:$\frac{5.4g}{27g/mol}$=0.2mol,0.2molAl与氢氧化钠溶液完全反应失去0.6mol电子,转移电子数为0.6NA,故D正确;
故选D.
点评 本题考查阿伏加德罗常数,题目难度中等,明确标况下气体摩尔体积的使用条件为解答关键,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
6.短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的原子最外层电子数之和为21.下列说法不正确的是( )
| W | |||
| X | Y | Z |
| A. | 原子半径大小:X>Y>Z | |
| B. | W、Y两种元素都能与氧元素形成化合物WO2、YO2 | |
| C. | 最高价氧化物对应水化物的酸性:W>Y>Z | |
| D. | W元素的单质能从X的氧化物中置换出X单质 |
11.柠檬烯是一种常用香料,其结构简式如图.有关柠檬烯的分析正确的是( )
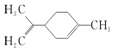

| A. | 它的一氯代物有6种 | |
| B. | 它分子式为:C10H18 | |
| C. | 它的分子中所有的碳原子一定在同一平面上 | |
| D. | 一定条件下,它分别可以发生加成、取代、氧化、加聚等反应 |
8.Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色反应呈黄色,五种元素核电荷数之和为54,W、Z最外层电子数相同,Z的核电荷数是W的2倍,工业上一般通过电解氧化物的方法获得Y的单质,则下列说法不正确的是( )
| A. | 原子半径:X>Y>Z>Q>W | |
| B. | X、Y和Z三种元素的最高价氧化物的水化物两两间能反应 | |
| C. | 阳离子的氧化性:X>Y | |
| D. | W的最简单氢化物沸点比Z的高 |
15.“酸雨”的形成主要是由于是( )
| A. | 煤燃烧时产生大量CO2 | B. | 煤不完全燃烧产生大量CO | ||
| C. | 煤燃烧时产生大量SO2 | D. | 工业生产中排放大量烟尘 |
12.化学与生活密切相关,下列说法正确的是( )
| A. | 高纯度的硅单质广泛用于制作光导纤维 | |
| B. | 绚丽缤纷的烟花中添加了含钾、钙、钠、铜等金属元素的化合物 | |
| C. | 汽车尾气中氮氧化物的产生主要是由于汽油中含有氮元素 | |
| D. | 埃博拉病毒对化学药品敏感,乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的 |
13.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | lmo1CH4中含有的电子数为9NA | |
| B. | 0.1mol•L-1的Na2S溶液中所含阴离子的数目大于0.1NA | |
| C. | 1molMg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为2NA | |
| D. | 80℃时,1LNaCl溶液中含有OH-的数目为1×10-7NA |
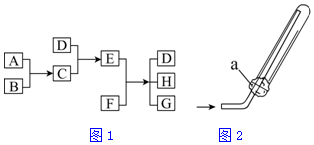 已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转化关系如图1所示:
已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转化关系如图1所示: