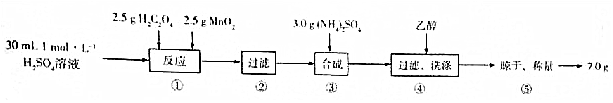
13.白磷的化学式写成P,但其实际组成为P4,而三氧化二磷其实是以六氧化四磷的形式存在的,已知P4O6分子中只含有单键,且每个原子的最外层都满足8电子结构,则分子中含有的共价键的数目是( )
| A. | 10 | B. | 12 | C. | 24 | D. | 28 |
12.下列过程中能形成离子键的是( )
| A. | 硫磺在空气中燃烧 | B. | 氢气与氯气在光照下反应 | ||
| C. | 镁在空气中逐渐失去光泽 | D. | 氯气溶于水 |
10.如图是进行电化学实验的两个装置,下列有关说法正确的是( )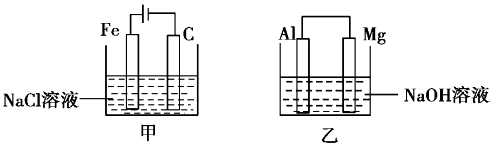

| A. | 甲装置中有沉淀生成,乙装置中Mg电极上有气泡生成 | |
| B. | 反应后,甲装置中溶液的质量增大,乙装置中溶液的质量减小 | |
| C. | 电极反应式:甲中阳极Fe-2e-=Fe2+,乙中负极Mg-2e-=Mg2+ | |
| D. | 反应后甲中溶液的pH减小,乙中溶液的pH增大 |
7.下列有关原理叙述正确的是( )
| A. | 电解饱和食盐水制氯气时,用铜片作阳极 | |
| B. | 电解法精炼铜时,以粗铜作阴极,纯铜作阳极 | |
| C. | 在原电池中,电子流出的一极是负极,发生氧化反应 | |
| D. | 在铁制品上镀银时,铁制品与电源正极相连 |
5.亚硝酞氯(NOCl,熔点:-64.5℃,沸点:-5.5℃)是一种黄色气体,遇水易水解.可用于合成清洁剂、触媒剂及中间体等.实验室可由氯气与一氧化氮在常温常压下合成.
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如图1所示:
为制备纯净干燥的气体,表中缺少的药品是:
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图2所示:
①装置连接顺序为a→e→f(或f→e)→c→b→d (按气流自左向右方向,用小写字母表示).
②装置 IV、V 除可进一步干燥NO、Cl2外,另一个作用是观察气泡调节气体的流速.
③装置 VII的作用是防止水蒸气进入反应器.
④装置 VIII中吸收尾气时,NOCl发生反应的化学方程式为NOCl+2NaOH=NaCl+NaNO2+H2O.
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酞氯和氯气,该反应的化学方程式为HNO3(浓)+3HC1(浓)=NOCl↑+Cl2↑+2H2O.
0 161661 161669 161675 161679 161685 161687 161691 161697 161699 161705 161711 161715 161717 161721 161727 161729 161735 161739 161741 161745 161747 161751 161753 161755 161756 161757 161759 161760 161761 161763 161765 161769 161771 161775 161777 161781 161787 161789 161795 161799 161801 161805 161811 161817 161819 161825 161829 161831 161837 161841 161847 161855 203614
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如图1所示:

为制备纯净干燥的气体,表中缺少的药品是:
| 装置Ⅰ | 装置Ⅱ | ||
| 烧瓶中 | 分液漏斗中 | ||
| 制备纯净Cl2 | MnO2 | ① | ② |
| 制备纯净NO | Cu | ③ | ④ |
①装置连接顺序为a→e→f(或f→e)→c→b→d (按气流自左向右方向,用小写字母表示).
②装置 IV、V 除可进一步干燥NO、Cl2外,另一个作用是观察气泡调节气体的流速.
③装置 VII的作用是防止水蒸气进入反应器.
④装置 VIII中吸收尾气时,NOCl发生反应的化学方程式为NOCl+2NaOH=NaCl+NaNO2+H2O.
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酞氯和氯气,该反应的化学方程式为HNO3(浓)+3HC1(浓)=NOCl↑+Cl2↑+2H2O.
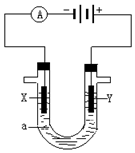 人们习惯上把电解饱和食盐水的工业叫做氯碱工业.
人们习惯上把电解饱和食盐水的工业叫做氯碱工业. 如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾.
如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾.