9.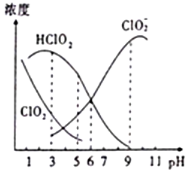 织物漂白剂亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都只有漂白作用,但ClO2是有毒气体.25℃时,各组分浓度随pH变化情况如图所示(Cl-没有画出).下列说法不正确的是( )
织物漂白剂亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都只有漂白作用,但ClO2是有毒气体.25℃时,各组分浓度随pH变化情况如图所示(Cl-没有画出).下列说法不正确的是( )
 织物漂白剂亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都只有漂白作用,但ClO2是有毒气体.25℃时,各组分浓度随pH变化情况如图所示(Cl-没有画出).下列说法不正确的是( )
织物漂白剂亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都只有漂白作用,但ClO2是有毒气体.25℃时,各组分浓度随pH变化情况如图所示(Cl-没有画出).下列说法不正确的是( )| A. | 25℃时,ClO2-的水解平衡常数Ka=10-6 | |
| B. | 在pH约为4.0~4.5范围内使用该漂白剂较好 | |
| C. | 25℃时,等浓度的HClO2溶液和NaClO2溶液等体积混合后,混合溶液中:c(HClO2)+c(H+)+c(Na+)═c(ClO2-)+2c(OH-) | |
| D. | 当pH=5时往NaClO2溶液中滴入稀氢氧化钠溶液,溶液中主要反应的离子方程式是:HClO2+OH-═H2O+ClO2- |
8.下列实验方案中,不能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 验证Cl2的氧化性强于I2 | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液,可观察到溶液变成蓝色 |
| B | 配制100mL 1.0mol•L-1CuSO4溶液 | 将25gCuSO4•5H2O溶于100mL蒸馏水中 |
| C | 比较水与乙醇中氢的活泼性 | 分別将少量钠投入到盛有水和乙醇的烧杯中 |
| D | 验证Cu(OH)2的溶解度小于Mg(OH)2 | 将0.1mol•L-1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol•L-1CuSO4溶液,可观察到先有白色沉淀生成,后变为浅蓝色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
6.如图所示,甲池的总反应式为:N2H4+O2═N2+2H2O,下列关于该电池工作时的说法正确的是( )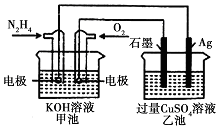

| A. | 该装置工作时,Ag电极上有气体生成 | |
| B. | 甲池和乙池中的溶液的pH均减小 | |
| C. | 甲池中负极反应为N2H4-4e-═N2+4H+ | |
| D. | 当甲池中消耗0.1molN2H4时,乙池中理沦上最多产生6.4g固体 |
5.五种短周期元素的某些性质如下所示,有关说法不正确的是( )
| 元素 | 元素的相关信息 |
| M | 最高价氧化物对应的水化物能与其气态氢化物反应生成盐 |
| N | 原子的M电子层上有3个电子 |
| W | 在短周期元素中,其原子半径最大 |
| X | 其最外层电子数是电子层数的2倍,且低价氧化物能与其气态氢化物反应生成X的单质和H2O |
| Y | 元素最高价正价与最低负价的代数和为6 |
| A. | M的气态氢化物具有还原性,常温下,该氢化物水溶液的pH>7 | |
| B. | W单质在氧气中燃烧后的产物中阴阳离子个数之比为1:2 | |
| C. | 由N和Y所形成的化合物中存在离子键,属于离子化合物 | |
| D. | N、W、X的最高价氧化物对应的水化物两两之间能相互发生反应 |
4.下列实验操作能达到实验目的是( )
| A. | 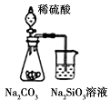 此装置可证明非金属性强弱:S>C>Si | |
| B. | 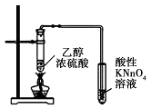 此装置可用于检验有乙烯生成 | |
| C. | 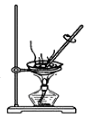 此装置可通过蒸干AlCl3饱和溶液制备AlCl3晶体 | |
| D. | 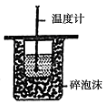 此装置可用来测定中和热 |
3.下列关于有机化合物的叙述正确的是( )
| A. | 氟利昂-12的结构式为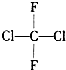 ,该分子是平面型分子 ,该分子是平面型分子 | |
| B. | 苯与液溴混合后撤入铁粉发生了加成反应 | |
| C. | 分子式为C4H9Cl的同分异构体共有4种 | |
| D. | 1mol苹果酸(HOOCCHOHCH2COOH)可与3molNaHCO3发生反应 |
2.设NA为阿伏伽德罗常数,下列说法正确的是( )
| A. | 1L1mol/L的盐酸溶液中,所含HCl分子数为NA | |
| B. | 常温常压下,71gCl2溶于水,转移的电子数目为0.1NA | |
| C. | 标准状况下,22.4LSO2和SO3的混合物,含硫原子的数目为NA | |
| D. | 0.5mol乙醇中含有的极性共价键数目为3.5NA |
1.化学在日常生活中应用广泛,下列叙述及对应关系错误的是( )
| 实际应用 | 相应性质 | |
| A | 用含有酸性重铬酸钾溶液的仪器检验酒后驾车 | 乙醇具有还原性 |
| B | 明矾常用于自来水的净化、杀菌消毒 | 明矾可发生水解生成胶状的Al(OH)3 |
| C | BaSO4可作为造影剂检查肠胃道疾病 | BaSO4难溶于水且不与盐酸反应 |
| D | 过氧化钠可用作呼吸面具中的供氧剂 | Na2O2能与CO2反应生成O2 |
| A. | A | B. | B | C. | C | D. | D |
20.实验室制备一硝基甲苯(主要含邻硝基甲苯和对硝基甲苯)的反应原理、实验装置如图:
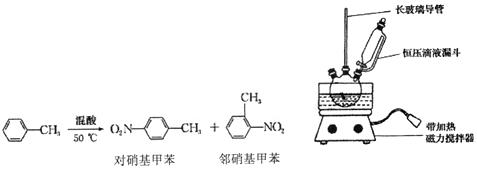
实验步骤:
①配制混酸,组装如图反应装置.取100mL 烧杯,用10mL 浓硫酸与30mL 浓硝酸配
制混酸,加入恒压滴液漏斗中,把15mL 甲苯(折合质量13.0g)加入三颈烧瓶中.
②向室温下的甲苯中逐滴加混酸,边滴边搅拌,混合均匀.
③在50一60℃下发生反应,直至反应结束.
④除去混酸后,依次用蒸馏水和10% NaCO3溶液洗涤,最后再用蒸馏水洗涤得到粗产品.
请回答下列问题:
(l)配制40mL 混酸的操作是分别取30mL浓硝酸和10mL浓硫酸,将30mL浓硝酸倒入烧杯中,再慢慢沿烧杯内壁注入10mL浓硫酸,边加边搅拌.
(2)装置中还缺少温度计 (填仪器名称).如果温度超过60℃,将会有二硝基甲苯或三硝基甲苯(填物质名称)生成.
(3)分离粗产品和水的操作方法是分液.
(4)产品用10% NaCO3溶液洗涤之后,再用蒸馏水洗涤,检验产品是否洗干净的操作是取最后一次洗涤液少许于试管中,滴加氯化钙溶液,无沉淀生成,则说明已洗净.
(5)为了得到更纯净的硝基苯,还须先向液体中加入CaO 除去水,然后蒸馏,若最终得到产品的质量为13.70g,则一硝基甲苯的产率是70.8%.
0 161639 161647 161653 161657 161663 161665 161669 161675 161677 161683 161689 161693 161695 161699 161705 161707 161713 161717 161719 161723 161725 161729 161731 161733 161734 161735 161737 161738 161739 161741 161743 161747 161749 161753 161755 161759 161765 161767 161773 161777 161779 161783 161789 161795 161797 161803 161807 161809 161815 161819 161825 161833 203614

| 密度/(g•cm-3) | 沸点/℃ | 式量 | 溶解性 | |
| 甲苯 | 0.866 | 110.6 | 92 | 不溶于水,易溶于一硝基甲苯 |
| 对硝基甲苯 | 1.286 | 237.7 | 137 | 不溶于水,易溶于液态烃 |
| 邻硝基甲苯 | 1.162 | 222 | 137 | 不溶于水,易溶于液态烃 |
①配制混酸,组装如图反应装置.取100mL 烧杯,用10mL 浓硫酸与30mL 浓硝酸配
制混酸,加入恒压滴液漏斗中,把15mL 甲苯(折合质量13.0g)加入三颈烧瓶中.
②向室温下的甲苯中逐滴加混酸,边滴边搅拌,混合均匀.
③在50一60℃下发生反应,直至反应结束.
④除去混酸后,依次用蒸馏水和10% NaCO3溶液洗涤,最后再用蒸馏水洗涤得到粗产品.
请回答下列问题:
(l)配制40mL 混酸的操作是分别取30mL浓硝酸和10mL浓硫酸,将30mL浓硝酸倒入烧杯中,再慢慢沿烧杯内壁注入10mL浓硫酸,边加边搅拌.
(2)装置中还缺少温度计 (填仪器名称).如果温度超过60℃,将会有二硝基甲苯或三硝基甲苯(填物质名称)生成.
(3)分离粗产品和水的操作方法是分液.
(4)产品用10% NaCO3溶液洗涤之后,再用蒸馏水洗涤,检验产品是否洗干净的操作是取最后一次洗涤液少许于试管中,滴加氯化钙溶液,无沉淀生成,则说明已洗净.
(5)为了得到更纯净的硝基苯,还须先向液体中加入CaO 除去水,然后蒸馏,若最终得到产品的质量为13.70g,则一硝基甲苯的产率是70.8%.