题目内容
8.下列实验方案中,不能达到实验目的是( )| 选项 | 实验目的 | 实验方案 |
| A | 验证Cl2的氧化性强于I2 | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液,可观察到溶液变成蓝色 |
| B | 配制100mL 1.0mol•L-1CuSO4溶液 | 将25gCuSO4•5H2O溶于100mL蒸馏水中 |
| C | 比较水与乙醇中氢的活泼性 | 分別将少量钠投入到盛有水和乙醇的烧杯中 |
| D | 验证Cu(OH)2的溶解度小于Mg(OH)2 | 将0.1mol•L-1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol•L-1CuSO4溶液,可观察到先有白色沉淀生成,后变为浅蓝色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.同一氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性,溶液变成蓝色,说明生成碘单质,据此可判断氯气与碘单质的氧化性强弱;
B.将25gCuSO4•5H2O溶于100mL蒸馏水中,所得溶液体积不是100mL;
C.根据反应生成氢气的快慢可以判断水与乙醇中氢的活泼性;
D.先有白色沉淀生成后变为浅蓝色沉淀,可说明氢氧化镁转化为氢氧化铜.
解答 解:A.向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液,氯气具有强氧化性,能将碘离子氧化生成碘,碘遇淀粉试液变蓝色,加入淀粉后溶液变蓝色,说明碘离子被氧化生成碘单质,氧化剂是氯气、氧化产物是碘,所以氧化性氧化性:Cl2>I2,故A正确;
B.配制100mL 1.0mol•L-1CuSO4溶液时,所得溶液体积必须为100mL,而将25gCuSO4•5H2O溶于100mL蒸馏水中,所得溶液体积不是100mL,故B错误;
C.分別将少量钠投入到盛有水和乙醇的烧杯中,根据反应剧烈程度可以比较水与乙醇中氢的活泼性,故C正确;
D.先有白色沉淀生成后变为浅蓝色沉淀,可说明氢氧化镁转化为氢氧化铜,则Cu(OH)2的溶解度比Mg(OH)2的小,故D正确;
故选B.
点评 本题考查化学实验方案的评价,涉及物质的性质的比较、溶液配制、离子检验等知识,为高频考点,侧重于学生的分析、实验能力的考查,注意把握实验的严密性和可行性的评价,难度不大.

练习册系列答案
相关题目
1.已知:在一定条件下,含高价态锰元素的化合物能被Cl-还原为Mn2+,氧化产物为Cl2,将1.0mol KMnO4加热,生成标准状况下5.6L气体后停止加热,向残留固体中加入足量浓盐酸,在加热条件下充分反应,又生成b mol气体,则b等于( )
| A. | 2 | B. | 1 | C. | 0.5 | D. | 0.25 |
19.下列物质的水溶液因水解呈碱性的是( )
| A. | HCl | B. | NaOH | C. | CH3COONa | D. | Na2SO4 |
16.某工业废水中仅含下表离子中的5种:
某同学欲探究废水的组成,进行了如下实验:
Ⅰ.取废水少许加入足量盐酸,无白色沉淀析出,但生成能使澄清石灰水变浑浊的无色无味气体
Ⅱ.向Ⅰ中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
下列推断不正确的是( )
| 阳离子 | K+、Cu2+、Fe3+、Ca2+、Fe2+ |
| 阴离子 | Cl-、CO32-、NO3-、SO42-、SiO32- |
Ⅰ.取废水少许加入足量盐酸,无白色沉淀析出,但生成能使澄清石灰水变浑浊的无色无味气体
Ⅱ.向Ⅰ中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
下列推断不正确的是( )
| A. | 溶液中一定含有的离子是K+、Cl-、CO32-、NO3-、SO42- | |
| B. | Ⅰ中加入盐酸生成无色气体的离子方程式是CO32-+2H+═CO2↑+H2O | |
| C. | 原溶液中的K+、Cl-、NO3-存在与否无法确定 | |
| D. | Ⅱ中产生白色沉淀的离子方程式是Ba2++SO42-═BaSO4↓ |
3.下列关于有机化合物的叙述正确的是( )
| A. | 氟利昂-12的结构式为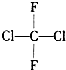 ,该分子是平面型分子 ,该分子是平面型分子 | |
| B. | 苯与液溴混合后撤入铁粉发生了加成反应 | |
| C. | 分子式为C4H9Cl的同分异构体共有4种 | |
| D. | 1mol苹果酸(HOOCCHOHCH2COOH)可与3molNaHCO3发生反应 |
13.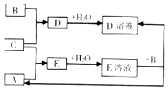 短周期元素X、Y、Z的原子序数依次增大,其中Y元素的原子半径最大.已知A、B、C分别是X、Y、Z三种元素的单质,A和C常温下为气体.在适宜的条件下,A、B、C可以发生如图所示的反应.下列说法正确的是( )
短周期元素X、Y、Z的原子序数依次增大,其中Y元素的原子半径最大.已知A、B、C分别是X、Y、Z三种元素的单质,A和C常温下为气体.在适宜的条件下,A、B、C可以发生如图所示的反应.下列说法正确的是( )
 短周期元素X、Y、Z的原子序数依次增大,其中Y元素的原子半径最大.已知A、B、C分别是X、Y、Z三种元素的单质,A和C常温下为气体.在适宜的条件下,A、B、C可以发生如图所示的反应.下列说法正确的是( )
短周期元素X、Y、Z的原子序数依次增大,其中Y元素的原子半径最大.已知A、B、C分别是X、Y、Z三种元素的单质,A和C常温下为气体.在适宜的条件下,A、B、C可以发生如图所示的反应.下列说法正确的是( )| A. | 化合物YX中含离子键 | B. | Z的含氧酸均为强酸 | ||
| C. | 非金属性:X>Z | D. | 离子半径:Y>Z |
20.薄荷醇的结构简式如图,下列说法正确的是( )
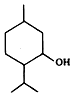

| A. | 薄荷醇属于芳香烃的含氧衍生物 | |
| B. | 薄荷醇分子式为C10H20O,它是环己醇的同系物 | |
| C. | 薄荷醇环上的一氯取代物只有三种 | |
| D. | 在一定条件下,薄荷醇能与氢气、溴水反应 |
17.已知1~20号元素的离子,aW2+、bX+、cY2-、dZ-都具有相同的电子层结构,下列说法正确的是( )
| A. | 质子数:d>c>b>a | B. | 离子半径:W2+>X+>Y2->Z- | ||
| C. | 原子半径:Z<Y<W<X | D. | 最低负价:X<W<Z<Y |
19.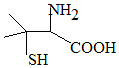 靑霉素是最重要的抗生素,其在体内经酸性水解后得到一种有机物X.己知X的结构如图,下列有关X的说法正确的是( )
靑霉素是最重要的抗生素,其在体内经酸性水解后得到一种有机物X.己知X的结构如图,下列有关X的说法正确的是( )
 靑霉素是最重要的抗生素,其在体内经酸性水解后得到一种有机物X.己知X的结构如图,下列有关X的说法正确的是( )
靑霉素是最重要的抗生素,其在体内经酸性水解后得到一种有机物X.己知X的结构如图,下列有关X的说法正确的是( )| A. | X为烃的含氧衍生物 | |
| B. | X的分子式为C5H10NO2S | |
| C. | X只能发生取代反应 | |
| D. | X中碳原子上的H若有1个被Cl取代,有2种不同产物 |