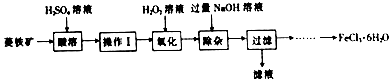
9.氮及其化合物在工农业生产、生活中有着重要应用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.
(1)已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ•mol-l
C(s)+O2(g)=CO2(g)△H=-393.5kJ•mol-l
2C(s)+O 2(g)=2CO(g)△H=-221kJ•mol-l
若某反应的平衡常数表达式为:k=$\frac{c({N}_{2})•{c}^{2}(C{O}_{2})}{{c}^{2}(NO)•{c}^{2}(CO)}$,请写出此反应的热化学方程式2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-746.5kJ•molˉ1.
(2)N2O5在一定条件下可发生分解:2N2O5(g)?4NO2(g)+O2(g).某温度下测得恒容密闭容器中N2O5浓度随时间的变化如表:
①反应开始时体系压强为P0,第3.00min时体系压强为p1,则p1:p0=1.975;2.00min~5.00min内,O2的平均反应速率为0.055mol•Lˉ1•minˉ1.
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是a.
a.容器中压强不再变化
b.NO2和O2的体积比保持不变
c.2v正(NO2)=v逆(N2O5)
d.气体的平均相对分子质量为43.2,且保持不变
(3)N2O 4与NO2之间存在反应:N2O4(g)?2NO2(g)△H=QkJ•mol-1.将一定量的NO放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度变化如图1所示.
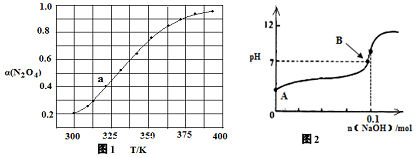
如图1中a点对应温度下,已知N2O4的起始压强p0为200kPa,该温度下反应的平衡常数Kp=213.3KPa(小数点后保留一位数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
(4)将固体氢氧化钠投入0.1mol/L的HN3(氢叠氮酸)溶液当中,溶液的体积1L(溶液体积变化忽略不计)溶液的pH变化如图2所示,HN3的电离平衡常数K=1×10-5,B点时溶液的pH=7,计算B点时加入氢氧化钠的物质的量0.099mol(保留两位有效数字).
(1)已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ•mol-l
C(s)+O2(g)=CO2(g)△H=-393.5kJ•mol-l
2C(s)+O 2(g)=2CO(g)△H=-221kJ•mol-l
若某反应的平衡常数表达式为:k=$\frac{c({N}_{2})•{c}^{2}(C{O}_{2})}{{c}^{2}(NO)•{c}^{2}(CO)}$,请写出此反应的热化学方程式2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-746.5kJ•molˉ1.
(2)N2O5在一定条件下可发生分解:2N2O5(g)?4NO2(g)+O2(g).某温度下测得恒容密闭容器中N2O5浓度随时间的变化如表:
| t/min | 0.00 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 |
| c(N2O5)/(mol•L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是a.
a.容器中压强不再变化
b.NO2和O2的体积比保持不变
c.2v正(NO2)=v逆(N2O5)
d.气体的平均相对分子质量为43.2,且保持不变
(3)N2O 4与NO2之间存在反应:N2O4(g)?2NO2(g)△H=QkJ•mol-1.将一定量的NO放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度变化如图1所示.

如图1中a点对应温度下,已知N2O4的起始压强p0为200kPa,该温度下反应的平衡常数Kp=213.3KPa(小数点后保留一位数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
(4)将固体氢氧化钠投入0.1mol/L的HN3(氢叠氮酸)溶液当中,溶液的体积1L(溶液体积变化忽略不计)溶液的pH变化如图2所示,HN3的电离平衡常数K=1×10-5,B点时溶液的pH=7,计算B点时加入氢氧化钠的物质的量0.099mol(保留两位有效数字).
8.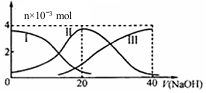 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HAˉ,III代表A2ˉ).根据图判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HAˉ,III代表A2ˉ).根据图判断,下列说法正确的是( )
 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HAˉ,III代表A2ˉ).根据图判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HAˉ,III代表A2ˉ).根据图判断,下列说法正确的是( )| A. | 当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(A2-)>c(H+)>c(HA-)>c(OH-) | |
| B. | 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水的大 | |
| C. | 当V(NaOH)=30 mL时,溶液中存在以下关系:2c(H+)+3c(H2A)+c(HA-)=c(A2-)+2c(OH-) | |
| D. | 向NaHA溶液加入水的过程中,pH可能增大也可能减小 |
7.下列有关实验原理或实验操作正确的是( )
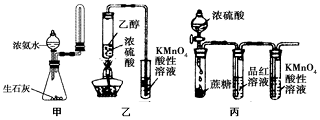

| A. | 实验室用图甲所示装置制取少量氨气 | |
| B. | 为使100ml0.5mol/L的NaNO3溶液物质的量浓度变为1mol/L,可将原溶液加热蒸发掉50ml水 | |
| C. | 利用图乙装置,可制取乙烯并验证其易被酸性KMnO4溶液氧化 | |
| D. | 利用图丙装置,可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性 |
6.实验室以苯甲酸和乙醇为原料制备甲酸乙酯(实验装置如图所示,相关物质的沸点如表).其实验步骤如表:
步骤1:将三颈瓶中的苯甲酸、乙醇、浓硫酸和环己烷按一定配比充分混合后,升温至60℃.
步骤2:将反应混合物倒入分液漏斗中,静置、分液.
步骤3:向上层液体中加入乙醚,再向混合液中加入饱和碳酸钠溶液,分离出乙醚层.
步骤4:向乙醚层中加入固体氯化钙后进行蒸馏,收集相应馏分.
(1)反应容器中制取苯甲酸乙酯的化学方程式为 +CH3CH2OH$?_{60℃}^{浓H_{2}SO_{4}}$
+CH3CH2OH$?_{60℃}^{浓H_{2}SO_{4}}$ +H2O;实验装置中冷凝管的主要作用是冷凝回流.
+H2O;实验装置中冷凝管的主要作用是冷凝回流.
(2)向反应体系中加入环己烷,可以提高产物效率的原因是与反应物形成共沸溶液,有利于将生成的水带走,使化学平衡向右移动.
(3)步骤4中加入固体氯化钙的作用是吸收水分.
(4)向反应体系中加入苯也可以制取苯甲酸乙酯,用环己烷代替苯的优点是减少有毒试剂的使用.
(5)步骤3中加入乙醚和饱和碳酸钠溶液的作用是萃取.
| 物质 | 苯甲酸 | 乙醇 | 环己烷 | 浓硫酸 | 苯甲酸乙酯 |
| 沸点/℃ | 249 | 78.3 | 80.7 | 338 | 212.6 |
步骤2:将反应混合物倒入分液漏斗中,静置、分液.
步骤3:向上层液体中加入乙醚,再向混合液中加入饱和碳酸钠溶液,分离出乙醚层.
步骤4:向乙醚层中加入固体氯化钙后进行蒸馏,收集相应馏分.
(1)反应容器中制取苯甲酸乙酯的化学方程式为
 +CH3CH2OH$?_{60℃}^{浓H_{2}SO_{4}}$
+CH3CH2OH$?_{60℃}^{浓H_{2}SO_{4}}$ +H2O;实验装置中冷凝管的主要作用是冷凝回流.
+H2O;实验装置中冷凝管的主要作用是冷凝回流.(2)向反应体系中加入环己烷,可以提高产物效率的原因是与反应物形成共沸溶液,有利于将生成的水带走,使化学平衡向右移动.
(3)步骤4中加入固体氯化钙的作用是吸收水分.
(4)向反应体系中加入苯也可以制取苯甲酸乙酯,用环己烷代替苯的优点是减少有毒试剂的使用.
(5)步骤3中加入乙醚和饱和碳酸钠溶液的作用是萃取.
4.下列实验方案能达到实验目的是( )
| A. | 证明浓度的改变可导致平衡移动:将少量KCl晶体加入FeCl3+3KSC?Fe(SCN)3+3KCl的平衡体系中 | |
| B. | 除去MgCl2溶液中少量的FeCl3:向含有少量FeCl3的MgCl2溶液中加入足量的Mg(OH)2粉末,搅拌一段时间后过滤 | |
| C. | 检验某溶液中是否含有乙醛:向盛有2mL 10%CuSO4溶液的试管中滴加0.5mL10%NaOH溶液,混合均匀,滴入待检液,加热 | |
| D. | 证明Fe3+的氧化性大于I2:将KI溶液和FeCl3溶液在试管中混合后,加入CCl4,振荡、静置,下层溶液显紫红色 |
3.常温下,下列各组离子能在指定溶液中大量共存的是( )
| A. | 使甲基橙变红色的溶液中:Na+、Fe2+、MnO4-、AlO2- | |
| B. | $\frac{{K}_{w}}{c({H}^{+})}$=1×10-12mol/L,的溶液中:NH4+、Ca2+、Cl-、NO3- | |
| C. | PH=0的溶液中:Al3+、Ag(NH3)2+、I-、SO42- | |
| D. | 加入Mg能放出H2的溶液中:Ca2+、NH4+、ClO-、NO3- |
2.扁桃酸衍生物是重要的医药中间体,在合成该有机物的过程中涉及如图转化:
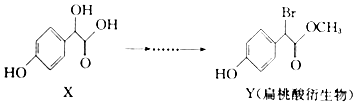
下列说法正确的是( )

下列说法正确的是( )
| A. | 化合物X的分子式为C8H8O4 | |
| B. | 化合物X、Y均可与NaHCO3溶液反应生成CO2 | |
| C. | 化合物X、Y分子中均含有1个手性碳原子 | |
| D. | 在一定条件下,化合物Y可发生加成反应和消去反应 |
1.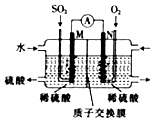 某兴趣小组用电化学法模拟工业处理SO2.强硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验.下列说法正确的是( )
某兴趣小组用电化学法模拟工业处理SO2.强硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验.下列说法正确的是( )
0 161635 161643 161649 161653 161659 161661 161665 161671 161673 161679 161685 161689 161691 161695 161701 161703 161709 161713 161715 161719 161721 161725 161727 161729 161730 161731 161733 161734 161735 161737 161739 161743 161745 161749 161751 161755 161761 161763 161769 161773 161775 161779 161785 161791 161793 161799 161803 161805 161811 161815 161821 161829 203614
 某兴趣小组用电化学法模拟工业处理SO2.强硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验.下列说法正确的是( )
某兴趣小组用电化学法模拟工业处理SO2.强硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验.下列说法正确的是( )| A. | N极为负极 | |
| B. | 反应一段时间后,左侧电解质溶液的pH增大 | |
| C. | M极发生的电极反应为SO2+2H2O-2e-═SO42-+4H+ | |
| D. | 在相同条件下,M、N两极上消耗的气体体积之比为1:2 |