题目内容
5.某化学兴趣小组以菱铁矿(主要成分为FeCO3,含有SiO2、Al2O3等少量杂质)为原料制备氯化铁晶体(FeCl3•6H2O)的实验过程如图: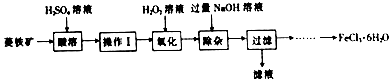
(1)酸溶及后续过程中均需保持算过量,其目的除了提高铁元素的浸出率之外,还有抑制Fe3+水解.
(2)操作Ⅰ名称是过滤.
(3)滴加H2O2溶液氧化时,发生主要反应的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O.
(4)在氧化过程中,如何检验铁元素全部以Fe3+形式存在:取少许氧化后的溶液于试管中,向试管中滴加1-2滴酸性高锰酸钾溶液,紫色不褪去,说明铁元素全部以Fe3+形式存在.
(5)加入过量NaOH溶液的目的是将Al3+转化为AlO2-,分离Fe3+与Al3+.
(6)请补充完整由过滤后得到的固体制备FeCl3•6H2O的实验方案:向过滤后所得固体,用水洗涤固体2-3次,低温干燥,得到FeCl3•6H2O.
分析 以菱铁矿(主要成分为FeCO3,含有SiO2、Al2O3)为原料,加入稀硫酸酸溶过滤得到滤液为硫酸铝、硫酸亚铁溶液,滤渣为SiO2,滤液中加入过氧化氢氧化亚铁离子为铁离子,加入过量氢氧化钠溶液沉淀铁离子,过滤得到氢氧化铁,滤液为偏铝酸钠和氢氧化钠的混合溶液,向过滤后所得固体,用水洗涤固体2-3次,加入稀盐酸使固体完全溶解,在氯化氢氛围内蒸发浓缩、冷却结晶,过滤,低温干燥,得到FeCl3•6H2O,据此分析解答.
解答 解:(1)酸溶及后续过程中均需保持算过量,其目的除了提高铁元素的浸出率之外,还有抑制Fe3+水解;
故答案为:抑制Fe3+水解;
(2)向菱铁矿加稀硫酸,二氧化硅不溶,从流程可知二氧化硅被除去,故操作Ⅰ为过滤;
故答案为:过滤;
(3)滴加H2O2溶液氧化时,发生主要反应的离子方程式为:H2O2+2Fe2++2H+=2Fe3++2H2O;
故答案为:H2O2+2Fe2++2H+=2Fe3++2H2O;
(4)检验铁元素全部以Fe3+形式存在,即检验是否有亚铁离子即可,方法为:取少许氧化后的溶液于试管中,向试管中滴加1-2滴酸性高锰酸钾溶液,紫色不褪去,说明铁元素全部以Fe3+形式存在;
故答案为:取少许氧化后的溶液于试管中,向试管中滴加1-2滴酸性高锰酸钾溶液,紫色不褪去,说明铁元素全部以Fe3+形式存在;
(5)经过氧化氢氧化后的溶液有铁离子和铝离子,加入过量NaOH溶液的目的是,将Al3+转化为AlO2-,分离Fe3+与Al3+;
故答案为:将Al3+转化为AlO2-,分离Fe3+与Al3+;
(6)过滤后得到的固体为氢氧化铁,由氢氧化铁制备FeCl3•6H2O的实验方案为:向过滤后所得固体,用水洗涤固体2-3次,加入稀盐酸使固体完全溶解,在氯化氢氛围内蒸发浓缩、冷却结晶,过滤,低温干燥,得到FeCl3•6H2O;
故答案为:加入稀盐酸使固体完全溶解,在氯化氢氛围内蒸发浓缩、冷却结晶,过滤.
点评 本题考查物质的制备实验及混合物的分离和提纯,为高频考点,把握流程图中每一步发生的反应及操作方法是解本题关键,注意结合题给信息解答,侧重分析与实验能力的考查,题目难度中等.

 同步练习强化拓展系列答案
同步练习强化拓展系列答案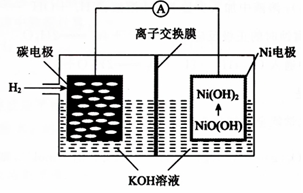
| A. | 离子交换膜选用阳离子交换膜(只允许阳离子通过) | |
| B. | 正极的电极反应为NiO(OH)+H2O+e-═Ni(OH)2+OH- | |
| C. | 导线中通过1mol电子时,理论上负极区溶液质量增加1g | |
| D. | 充电时,碳电极与电源的正极相连 |
| A. | 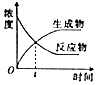 图表示某可逆反应物质的浓度随时间的变化,且在t时刻达到平衡状态 | |
| B. | 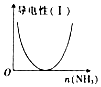 图表示向CH3COOH溶液中通入NH3至过量的过程中溶液导电性的变化 | |
| C. |  图表明合成氨反应时放热反应,b表示在反应体系中加入了催化剂 | |
| D. | 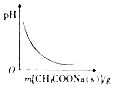 图表示向CH3COOH溶液中逐渐加入CH3COONa固体后,溶液pH的变化 |
(1)已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ•mol-l
C(s)+O2(g)=CO2(g)△H=-393.5kJ•mol-l
2C(s)+O 2(g)=2CO(g)△H=-221kJ•mol-l
若某反应的平衡常数表达式为:k=$\frac{c({N}_{2})•{c}^{2}(C{O}_{2})}{{c}^{2}(NO)•{c}^{2}(CO)}$,请写出此反应的热化学方程式2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-746.5kJ•molˉ1.
(2)N2O5在一定条件下可发生分解:2N2O5(g)?4NO2(g)+O2(g).某温度下测得恒容密闭容器中N2O5浓度随时间的变化如表:
| t/min | 0.00 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 |
| c(N2O5)/(mol•L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是a.
a.容器中压强不再变化
b.NO2和O2的体积比保持不变
c.2v正(NO2)=v逆(N2O5)
d.气体的平均相对分子质量为43.2,且保持不变
(3)N2O 4与NO2之间存在反应:N2O4(g)?2NO2(g)△H=QkJ•mol-1.将一定量的NO放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度变化如图1所示.
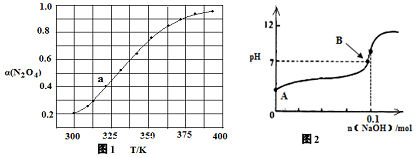
如图1中a点对应温度下,已知N2O4的起始压强p0为200kPa,该温度下反应的平衡常数Kp=213.3KPa(小数点后保留一位数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
(4)将固体氢氧化钠投入0.1mol/L的HN3(氢叠氮酸)溶液当中,溶液的体积1L(溶液体积变化忽略不计)溶液的pH变化如图2所示,HN3的电离平衡常数K=1×10-5,B点时溶液的pH=7,计算B点时加入氢氧化钠的物质的量0.099mol(保留两位有效数字).
| A. | Cl2O | B. | H2SO4 | C. | C2H5OH | D. | KNO3 |
| A. | 碘单质升华,克服的是其分子间作用力 | |
| B. | 金刚石、石墨、纳米碳管是碳元素的同素异形体 | |
| C. | 目前科学家还无法实现对原子或分子的操纵 | |
| D. | HCl气体溶于水后,共价键被破坏,从而形成了H+和Cl- |
(1)该同学选用如图所示的部分装置(可以重复选用)进行实验,装置依次连接的合理顺序为A、B、D、C、E、D、F.
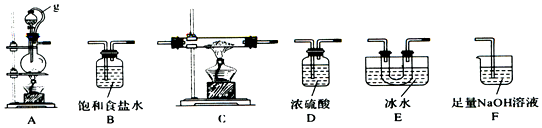
(2)A中反应的离子方程式为MnO2+2Cl-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(3)图中g管的作用是保持气压平衡,便于分液漏斗中的液体流入蒸馏烧瓶,装置E 的作用是冷凝并收集BC13.
(4)停止实验,正确的操作是先熄灭C处酒精灯,再拔F处导管,后熄灭A处酒精灯.
(5)硼酸是一元弱酸,其钠盐化学式为Na[B(OH)4〕,则硼酸在水中的电离方程式是H3BO3+H2O═[B(OH)4]-+H+.
(6)实验完成后,某同学向F中(溶液含有0.05mol/LNaC10、0.05mol/LNaCl、0.1mol/LN a0H)滴加品红溶液,发现溶液褪色.现设计实验探究溶液褪色的原因,请在表中空格处填上数据,完成实验方案.
| 实验序号 | 0.1mol/L NaClO溶液/mL | 0.1mol/L NaCl溶液/mL | 0.2mol/L NaOH溶液/mL | H2O/mL | 品红溶液 | 现象 |
| ① | 4.0 | 0 | 0 | 4.0 | 3滴 | 较快褪色 |
| ② | 0 | 4.0 | 4.0 | 0 | 3滴 | 不褪色 |
| ③ | 4.0 | 0 | 4.0 | 0 | 3滴 | 缓慢褪色 |
 ;氯离子的电子式
;氯离子的电子式 .
.