题目内容
1.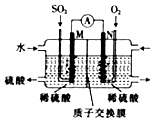 某兴趣小组用电化学法模拟工业处理SO2.强硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验.下列说法正确的是( )
某兴趣小组用电化学法模拟工业处理SO2.强硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验.下列说法正确的是( )| A. | N极为负极 | |
| B. | 反应一段时间后,左侧电解质溶液的pH增大 | |
| C. | M极发生的电极反应为SO2+2H2O-2e-═SO42-+4H+ | |
| D. | 在相同条件下,M、N两极上消耗的气体体积之比为1:2 |
分析 本质是二氧化硫、氧气与水反应生成硫酸,M电极上二氧化硫失去电子氧化生成SO42-为负极,电极反应式为:SO2+2H2O-2e -═SO42-+4H+,N电极为氧气得电子结合氢离子生成水为正极,电极反应式为:O2+4H++4e -═2H2O,据此分析解答.
解答 解:A.N电极为氧气得电子结合氢离子生成水为正极,故A错误;
B.左侧M电极上二氧化硫失去电子氧化生成SO42-为负极,电极反应式为:SO2+2H2O-2e -═SO42-+4H+,所以反应一段时间后,左侧电解质溶液的pH减小,故B错误;
C.M电极上二氧化硫失去电子氧化生成SO42-为负极,电极反应式为:SO2+2H2O-2e -═SO42-+4H+,故C正确;
D.M电极电极反应式为:SO2+2H2O-2e -═SO42-+4H+,N电极电极反应式为:O2+4H++4e -═2H2O,所以在相同条件下,M、N两极上消耗的气体体积之比为2:1,故D错误;
故选C.
点评 本题考查了原电池原理,根据电极反应确定电极上的生成物及溶液pH变化,难点是电极反应式的书写.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.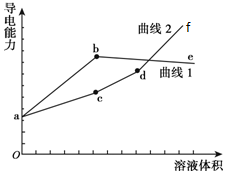 分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,测得导电能力随溶液加入变化曲线如图所示,下列说法中正确的是( )
分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,测得导电能力随溶液加入变化曲线如图所示,下列说法中正确的是( )
 分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,测得导电能力随溶液加入变化曲线如图所示,下列说法中正确的是( )
分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,测得导电能力随溶液加入变化曲线如图所示,下列说法中正确的是( )| A. | 曲线1代表滴加NaOH溶液的变化曲线 | |
| B. | C点溶液中大量存在的离子是Na+和SO42- | |
| C. | b和d点对应的溶液均显酸性 | |
| D. | be段导电能力下降的原因是NH3•H2O?NH4++OH-,导致离子数目减少 |
14.下列说法正确的是( )
| A. | 化学反应中,化学能全部转化为热能 | |
| B. | 已知C(s)+$\frac{1}{2}$O2(g)═CO(g),△H=-110.5kJ•mol-1,则碳的燃烧热为-110.5kJ•mol-1 | |
| C. | 测定中和热时,用铜制搅拌棒代替环形玻璃搅拌棒不影响测定结果 | |
| D. | 反应C(s)+CO2(g)═2CO(g)△H>0在较高温度下能自发进行 |
16.下列说法不正确的是( )
| A. | 利用浓硫酸的吸水性,干燥氢气 | |
| B. | 碳酸氢钠溶液呈碱性,可用于治疗胃酸过多 | |
| C. | 氯化铝是电解质,电解熔融的氯化铝制备金属铝 | |
| D. | 镁在空气中燃烧时发出耀眼的白光,可用于制造信号弹 |
12.a、b、c、d为短周期元素,a的M电子层有1个电子,b的一种核素14b常用于鉴定文物年代,c的最高价化合物与最低价化合物代数和为4,d的低价含氧酸能杀菌、消毒、漂白.下列叙述不正确的是( )
| A. | 最高价含氧酸酸性:d>c>b | |
| B. | 它们均存在两种或两种以上的氧化物 | |
| C. | b与氢形成的化合物只存在极性共价键 | |
| D. | a、b、c的离子半径依次增大 |
9.下列说法正确的是( )
| A. | 在紫外线、饱和(NH4)2SO4溶液、CuSO4溶液等作用下,蛋白质均会发生变化 | |
| B. | 为检验皂化反应进行程度,取几滴反应液,滴入装有热水的试管中,振荡,若有油滴浮在液面上,说明油脂已完全反应 | |
| C. | 只用新制Cu(OH)2悬浊液就可以鉴别乙酸溶液、葡萄糖溶液、淀粉溶液 | |
| D. | 苯是从煤中分离得到的一种重要的化工原料,是无色、有特殊气味的液态烃 |
10.用NA表示阿佛加德罗常数的值,下列说法正确的是( )
| A. | 在浓硫酸作用下,60g冰醋酸与足量无水乙醇反应生成乙酸乙酯的分子数为NA | |
| B. | 标准状况下,3.36LC2H4和C3H6的混合气体中含有碳碳双键的数目为0.15NA | |
| C. | 电解精炼铜,当外电路转移NA个电子时,阳极质量减少32g | |
| D. | 含0.01molFeCl3的浓溶液滴入沸水,制得的胶体粒子数目小于0.01NA |