2.常温下,Ksp(CaSO4)=9×10-6,CaSO4在水中的沉淀溶解平衡曲线如图所示.下列判断错误的是( )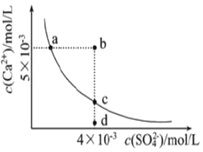

| A. | a、c两点均可以表示常温下CaSO4溶于水所形成的饱和溶液 | |
| B. | a点对应的Ksp不等于c点对应的Ksp | |
| C. | b点将有沉淀生成,平衡后溶液中c(Ca2+)•c(SO42-)一定等于9×10-6 | |
| D. | 向d点溶液中加入适量CaCl2固体可以变成c点 |
1.向一定量的FeO、Fe、Fe2O3的混合物中加入100mL 1mol/L盐酸,恰好使混合物完全溶解,放出112mL(标准状况)的气体,在所得溶液中加入KSCN溶液无血红色出现.若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量为( )
| A. | 2.8g | B. | 5.6g | C. | 8.4g | D. | 无法计算 |
20.常温下,对于1L0.1mol/L的醋酸溶液,下列判断不正确的是( )
| A. | 该溶液的PH大于1 | |
| B. | c(OH-)=c(H+)-C(CH3COO-) | |
| C. | 与等体积、等浓度的NaOH溶液完全中和后,溶液显中性 | |
| D. | 与足量锌反应比等体积、等浓度的盐酸反应速率慢,生成氢气的质量相等 |
19.下列化合物中,同分异构体数目最少的是( )
| A. | 戊烷 | B. | 苯酚 | C. | 1-氯己烷 | D. | 乙酸乙酯 |
18.下列说法不正确的是( )
| A. | 分子式为C7H8O的芳香族化合物,其中能与钠反应生成H2的结构有4种 | |
| B. | 通过核磁共振氢谱可以区分乙醇和乙酸乙酯 | |
| C. | 三硝基甲苯和硝化甘油都是烈性炸药,它们都属于酯类物质 | |
| D. | 不慎将苯酚沾到手上,应立即用酒精洗涤,再用水冲洗 |
16.已知短周期主族元素X、Y、Z、W、R五种元素,原子序数依次增大,X元素的原子是所有元素中原子半径最小的,Y、W同主族,Z、W同周期.X与Y可形成具有18个电子的化合物G,在酸性条件下,在含W阴离子的溶液中加入G可得到W单质.Z是同周期中金属性最强的元素.下列说法不正确的是( )
| A. | 原子半径:X<Y<W<R<Z | |
| B. | 由Y、Z元素可形成两种离子化合物其阳离子与阴离子物质的量之比都是2:1 | |
| C. | 沸点:X2Y>X2W | |
| D. | w与R可形成共价化合物WR2,且WR2是极性分子 |
15.含FeS286%的黄铁矿燃烧时损失硫5%,由SO2转化为SO3时转化率为99%,则生产98%硫酸1吨,需黄铁矿的质量为( )
| A. | 0.742吨 | B. | 0.85吨 | C. | 0.875吨 | D. | 1吨 |
14.下列说法正确的是( )
| A. | 第3层最多能容纳32个电子 | |
| B. | 磷原子的结构示意图 | |
| C. | 第2周期元素的最高正价从+1递增到+7 | |
| D. | 同周期主族元素的原子半径随原子序数的递增而逐渐减小 |
13.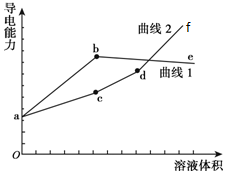 分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,测得导电能力随溶液加入变化曲线如图所示,下列说法中正确的是( )
分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,测得导电能力随溶液加入变化曲线如图所示,下列说法中正确的是( )
0 161628 161636 161642 161646 161652 161654 161658 161664 161666 161672 161678 161682 161684 161688 161694 161696 161702 161706 161708 161712 161714 161718 161720 161722 161723 161724 161726 161727 161728 161730 161732 161736 161738 161742 161744 161748 161754 161756 161762 161766 161768 161772 161778 161784 161786 161792 161796 161798 161804 161808 161814 161822 203614
 分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,测得导电能力随溶液加入变化曲线如图所示,下列说法中正确的是( )
分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,测得导电能力随溶液加入变化曲线如图所示,下列说法中正确的是( )| A. | 曲线1代表滴加NaOH溶液的变化曲线 | |
| B. | C点溶液中大量存在的离子是Na+和SO42- | |
| C. | b和d点对应的溶液均显酸性 | |
| D. | be段导电能力下降的原因是NH3•H2O?NH4++OH-,导致离子数目减少 |
 ;氯离子的电子式
;氯离子的电子式 .
.