题目内容
13.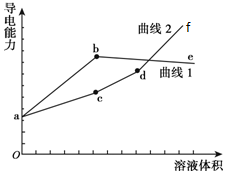 分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,测得导电能力随溶液加入变化曲线如图所示,下列说法中正确的是( )
分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,测得导电能力随溶液加入变化曲线如图所示,下列说法中正确的是( )| A. | 曲线1代表滴加NaOH溶液的变化曲线 | |
| B. | C点溶液中大量存在的离子是Na+和SO42- | |
| C. | b和d点对应的溶液均显酸性 | |
| D. | be段导电能力下降的原因是NH3•H2O?NH4++OH-,导致离子数目减少 |
分析 分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,一水合氨滴入发生反应:6NH3•H2O+Al2(SO4)3=2Al(OH)3↓+3(NH4)2SO4,氢氧化钠溶液滴入发生的反应为:6NaOH+Al2(SO4)3=2Al(OH)3↓+3Na2SO4 ,Al(OH)3+NaOH=NaAlO2+2H2O,所以曲线1为氨水滴入的反应,曲线2位氢氧化钠滴入的反应,据此分析选项.
解答 解:A.一水合氨滴入发生反应:6NH3•H2O+Al2(SO4)3=2Al(OH)3↓+3(NH4)2SO4,氢氧化钠溶液滴入发生的反应为:6NaOH+Al2(SO4)3=2Al(OH)3↓+3Na2SO4 ,Al(OH)3+NaOH=NaAlO2+2H2O,所以曲线1为氨水滴入的反应,曲线2位氢氧化钠滴入的反应,故A错误;
B.c点发生的反应是6NaOH+Al2(SO4)3=2Al(OH)3↓+3Na2SO4 ,溶液中大量存在的离子是Na+和SO42-,故B正确;
C.b点为硫酸铵溶液,铵根水解溶液显酸性,d点是NaAlO2溶液,偏铝酸根离子水解溶液显碱性,故C错误;
D.be段导电能力下降是因为溶液中离子浓度减小,故D错误;
故选B.
点评 本题考查了电解质溶液反应前后溶液导电性的分析判断,主要是离子浓度变化决定溶液导电的变化,注意图象变化的实质理解,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.25℃时,①纯水 ②pH=2的醋酸溶液 ③pH=12的氢氧化钠溶液 ④pH=2的醋酸溶液和pH=12的氢氧化钠溶液等体积混合,上述溶液中水的电离程度由小到大的顺序是( )
| A. | ②<①<③<④ | B. | ②=③<④<① | C. | ②=③<①<④ | D. | ②=④<③<① |
8.已知20°C时AgBr的溶解度为8.4×10-6AgCl的溶解度为1.5×10-4将AgCl与AgBr的饱和溶液等体积混合,再加入足量浓硝酸银,发生的反应为( )
| A. | AgCl沉淀多于AgBr沉淀 | B. | AgCl和AgBr沉淀等量生成 | ||
| C. | AgCl沉淀少于AgBr沉淀 | D. | 只有AgBr沉淀生成 |
18.下列说法不正确的是( )
| A. | 分子式为C7H8O的芳香族化合物,其中能与钠反应生成H2的结构有4种 | |
| B. | 通过核磁共振氢谱可以区分乙醇和乙酸乙酯 | |
| C. | 三硝基甲苯和硝化甘油都是烈性炸药,它们都属于酯类物质 | |
| D. | 不慎将苯酚沾到手上,应立即用酒精洗涤,再用水冲洗 |
5.向14.8g Fe2O3、FeO和Cu的混合物中,加入1mol•L-1硫酸溶液200mL时,固体恰好完全溶解,所得溶液中不含Fe3+.若用足量的CO在高温下还原相同质量的原混合物,得到的固体质量为( )
| A. | 11.6g | B. | 10.8g | C. | 8.4g | D. | 13.2g |
2.向300mL 1mol/L的稀硝酸中,加入5.6g铁粉,充分反应后,铁粉全部溶解(假设还原产物只有NO),下列说法不正确的是( )
| A. | 最终所得溶液中既有Fe2+又有Fe3+ | |
| B. | 最终溶液中,硝酸无剩余 | |
| C. | 标准状况下生成NO的体积为1.68L | |
| D. | 再向最终所得溶液中滴加稀硝酸,无明显变化 |
1.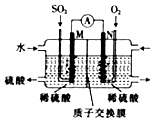 某兴趣小组用电化学法模拟工业处理SO2.强硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验.下列说法正确的是( )
某兴趣小组用电化学法模拟工业处理SO2.强硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验.下列说法正确的是( )
 某兴趣小组用电化学法模拟工业处理SO2.强硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验.下列说法正确的是( )
某兴趣小组用电化学法模拟工业处理SO2.强硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验.下列说法正确的是( )| A. | N极为负极 | |
| B. | 反应一段时间后,左侧电解质溶液的pH增大 | |
| C. | M极发生的电极反应为SO2+2H2O-2e-═SO42-+4H+ | |
| D. | 在相同条件下,M、N两极上消耗的气体体积之比为1:2 |
 bB(g)+cC(g)达平衡后,保持温度不变,将容器体积增加一倍,最终测得A的物质的量的浓度变为原来的50%,则
bB(g)+cC(g)达平衡后,保持温度不变,将容器体积增加一倍,最终测得A的物质的量的浓度变为原来的50%,则