9.Na3N是一种离子化合物,它与水反应有NH3生成,以下关于Na3N的叙述正确的是( )
| A. | Na+与N3-的电子层结构都与氩原子相同 | |
| B. | Na3N中的Na+的半径大于N3-的半径 | |
| C. | Na3N与盐酸反应可生成两种盐 | |
| D. | Na3N与水的反应属于氧化还原反应 |
8.实现下列变化时,必须克服相同类型作用的是( )
| A. | 二氧化硅和冰的熔化 | B. | 氯化钠和铁的熔化 | ||
| C. | 烧碱和金刚石的熔化 | D. | 碘和干冰的升华 |
7.某同学为证明氯化钠晶体中存在离子键,设计了以下实验,其中合理的是( )
| A. | 测量氯化钠的熔点 | B. | 测量固体氯化钠的导电性 | ||
| C. | 测量熔融氯化钠的导电性 | D. | 测量氯化钠水溶液的导电性 |
5.下列选项中,互为同位素的是( )
| A. | 金刚石和石墨 | B. | CO和CO2 | C. | 16O和18O | D. | 1H216O和2H218O |
4.下列关于气体摩尔体积的叙述中正确的是( )
| A. | 1mol二氧化碳在标准状况时所占的体积约是22.4L | |
| B. | 氧气在标准状况下頕有体积约为22.4L | |
| C. | 1mol任何物质在0℃,1.01×105Pa时体积都约是22.4L | |
| D. | 1mol任何气体的体积都约是22.4L |
3.下列制备有关化学物质的工艺不可行的是( )
| A. | 提取食盐后的母液$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{稀HCl}{→}$MgCl2溶液$\stackrel{电解}{→}$Mg | |
| B. | Cu$\stackrel{H_{2}O_{2},稀H_{2}SO_{4}}{→}$CuSO4溶液$\stackrel{蒸发,结晶}{→}$CuSO4•5H2O | |
| C. | 饱和食盐水$\stackrel{NH_{3}}{→}$$\stackrel{CO_{2}}{→}$NaHCO3$\stackrel{△}{→}$Na2CO3 | |
| D. | N2$→_{催化剂}^{H_{2}}$NH3$→_{催化剂}^{O_{2}}$NO→NO2$\stackrel{H_{2}O}{→}$HNO3 |
2.下列转化中不涉及化学变化的是( )
| A. | 煤的液化 | B. | 海水晒盐 | C. | 蜡烛照明 | D. | 石油裂解 |
1.卤块的主要成分是MgCl2,此外还含Fe2+、Fe3+和Mn2+等杂质离子.以卤块为原料按图所示流程进行生产,可制得轻质氧化镁.
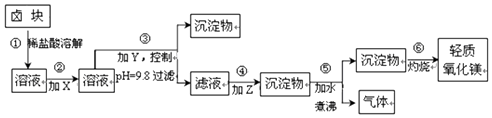
若要求产品尽量不含杂质且生产成本较低,请根据上表提供的资料回答:
(1)流程中加入的试剂X、Y、Z最佳选择依次是表2中的acd( 选填试剂编号).
(2)步骤②发生反应的离子方程式为2Fe2++ClO-+2H+=Cl-+2Fe3++H2O;步骤⑤中发生反应的化学方程为MgCO3+H2O $\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+CO2↑.
(3)步骤③控制pH=9.8的目的是使除Mg2+以外的各种杂质金属离子都成为氢氧化物沉淀以便除去.
(4)若在实验室进行步骤⑥的灼烧实验,必须用到的仪器是铁三脚、酒精喷灯、坩埚和泥三角.
0 161188 161196 161202 161206 161212 161214 161218 161224 161226 161232 161238 161242 161244 161248 161254 161256 161262 161266 161268 161272 161274 161278 161280 161282 161283 161284 161286 161287 161288 161290 161292 161296 161298 161302 161304 161308 161314 161316 161322 161326 161328 161332 161338 161344 161346 161352 161356 161358 161364 161368 161374 161382 203614

| 表1:生成氢氧化物沉淀的pH | 表2:原料价格表 | |||
| 物质 | 开始沉淀 | 沉淀完全 | 物质 | 价格(元/吨) |
| Fe(OH)3 | 2.7 | 3.7 | a.漂液(含25.2%NaClO) | 450 |
| Fe(OH)2 | 7.6 | 9.6﹡ | b.双氧水(含30%H2O2) | 2400 |
| 资*源%库Mn(OH)2 | 8.3 | 9.8 | c.烧碱(含98%NaOH) | 2100 |
| Mg(OH)2 | 9.6 | 11.1 | d.纯碱(含99.5%Na2CO3) | 600 |
(1)流程中加入的试剂X、Y、Z最佳选择依次是表2中的acd( 选填试剂编号).
(2)步骤②发生反应的离子方程式为2Fe2++ClO-+2H+=Cl-+2Fe3++H2O;步骤⑤中发生反应的化学方程为MgCO3+H2O $\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+CO2↑.
(3)步骤③控制pH=9.8的目的是使除Mg2+以外的各种杂质金属离子都成为氢氧化物沉淀以便除去.
(4)若在实验室进行步骤⑥的灼烧实验,必须用到的仪器是铁三脚、酒精喷灯、坩埚和泥三角.
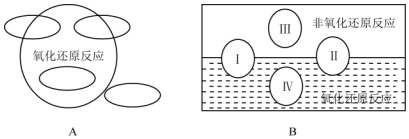 氧化还原是常见的反应类型,根据信息回答以下问题:
氧化还原是常见的反应类型,根据信息回答以下问题: