14.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | PH=12的溶液:Cl-、OH-、K+、Ba2+ | |
| B. | 能使酚酞变红的溶液中:SO42-、NH4+、K+、NO3- | |
| C. | 0.1mol/L的Na2CO3溶液中:K+、Ba2+、NO3-、Cl- | |
| D. | 无色透明溶液中:K+、Na+、MnO4-、Cl- |
13.下列变化属于还原反应的是( )
| A. | Fe→FeSO4 | B. | Cu(NO3)2→Cu | C. | CO→CO2 | D. | NaCl→AgCl |
12.按照初中化学的分类方法,下列反应既属于氧化反应又属于化合反应的是( )
| A. | NaHCO3+HCl═NaCl+H2O+CO2↑ | B. | 2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$ 2KCl+2O2↑ | ||
| C. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | D. | 2CuO+C$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+CO2 |
10.设NA表示阿伏伽德罗常数的值,下列说法中正确的是( )
| A. | 200g63%的浓硝酸中含氧原子个数为6NA | |
| B. | 50mL12mol•L-1 盐酸和足量MnO2共热,转移的电子数目为0.3NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标况下)气体时,电路中通过的电子数目为4NA | |
| D. | 若CH3COONa溶液中CH3COO-的数目为6NA,则Na+的目为6NA |
8.在理论上不能用于设计原电池的化学反应是( )
| A. | Al(OH)3(s)+NaOH(aq)═NaAlO2(aq)+2H2O(aq)△H<0 | |
| B. | CH3CH3OH(l)+3O2(g)-→2CO2(g)+3H2O(l)△H<0 | |
| C. | CO2(g)+C(g)═2CO(g)△H>0 | |
| D. | H2(g)+Cl2(g)═2HCl(g)△H<0 |
7.下列说法正确的是( )
| A. | 常温下.NH4Cl溶液加水稀释,$\frac{c(N{H}_{3•}{H}_{2}O)•c({H}^{+})}{c(N{{H}_{4}}^{+})}$增大 | |
| B. | 0.1mol/LNa2CO3溶液加热后,溶液的pH减小 | |
| C. | 室温下稀释O.lmol/LCH3COOH溶液,溶液的导电能力减弱,因此溶液中所有离子浓度均减小 | |
| D. | 向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体的原理是加热促进Fe3+水解 |
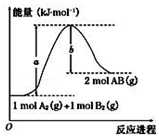
6.化学反应 A2(g)+B2(g)?2AB(g)的能量变化如图所示,下列叙述中正确的是( )
0 161015 161023 161029 161033 161039 161041 161045 161051 161053 161059 161065 161069 161071 161075 161081 161083 161089 161093 161095 161099 161101 161105 161107 161109 161110 161111 161113 161114 161115 161117 161119 161123 161125 161129 161131 161135 161141 161143 161149 161153 161155 161159 161165 161171 161173 161179 161183 161185 161191 161195 161201 161209 203614

| A. | 每生成 2 个分子 AB 吸收(a-b) kJ 热量 | |
| B. | 该反应热△H=+(a-b)kJ•mol-1 | |
| C. | 逆反应的活化能高于正反应的活化能 | |
| D. | 断裂1mol A-A 和 1mol B-B 键,放出 a kJ 能量 |
 糠醛(
糠醛(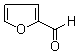 )可与新制含有NaOH的Cu(OH)2悬浊液在加热条件下反应得到砖红色沉淀Cu2O.
)可与新制含有NaOH的Cu(OH)2悬浊液在加热条件下反应得到砖红色沉淀Cu2O.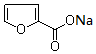 +Cu2O↓+3H2O.
+Cu2O↓+3H2O. 化学在能源开发与利用中起到十分关键的作用.甲醇是一种新型的绿色能源,又是一种重要的化工原料.甲醇燃料电池能量转化率高,具有广阔的发展前景.现用甲醇燃料电池进行如图实验.已知:2CH3OH+3O2+4OH-═2CO32-+6H2O
化学在能源开发与利用中起到十分关键的作用.甲醇是一种新型的绿色能源,又是一种重要的化工原料.甲醇燃料电池能量转化率高,具有广阔的发展前景.现用甲醇燃料电池进行如图实验.已知:2CH3OH+3O2+4OH-═2CO32-+6H2O