题目内容
12.按照初中化学的分类方法,下列反应既属于氧化反应又属于化合反应的是( )| A. | NaHCO3+HCl═NaCl+H2O+CO2↑ | B. | 2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$ 2KCl+2O2↑ | ||
| C. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | D. | 2CuO+C$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+CO2 |
分析 化合反应:两种或两种以上物质反应后生成一种物质的反应,其特点可总结为“多变一”; 物质与氧发生的化学反应是氧化反应;据此进行分析判断;
解答 解:A、NaHCO3+HCl═NaCl+H2O+CO2↑无元素化合价的变化,是非氧化还原反应,故A错误;
B、2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$ 2KCl+2O2↑是分解反应,非氧化还原反应,故B错误;
C、S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2是氧化还原型的化合反应,故C正确;
D、2CuO+C$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+CO2是氧化还原型的置换反应,故D错误;
故选C.
点评 本题难度不大,掌握化合反应的特征(“多变一”)、氧化反应的特征是正确解答本题的关键.

练习册系列答案
相关题目
3.甲苯和苯相比较,下列叙述中错误的是( )
| A. | 常温下都是液体 | B. | 都能在空气中燃烧 | ||
| C. | 都能使酸性高锰酸钾溶液褪色 | D. | 都能发生取代反应 |
7.下列说法正确的是( )
| A. | 常温下.NH4Cl溶液加水稀释,$\frac{c(N{H}_{3•}{H}_{2}O)•c({H}^{+})}{c(N{{H}_{4}}^{+})}$增大 | |
| B. | 0.1mol/LNa2CO3溶液加热后,溶液的pH减小 | |
| C. | 室温下稀释O.lmol/LCH3COOH溶液,溶液的导电能力减弱,因此溶液中所有离子浓度均减小 | |
| D. | 向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体的原理是加热促进Fe3+水解 |
17.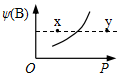 现有mA(s)+nB(g)?qC(g);△H<0的可逆反应,在一定温度下达平衡时,B的体积分数ψ(B)和压强P的关系如图所示,则下列有关该反应的描述正确的是( )
现有mA(s)+nB(g)?qC(g);△H<0的可逆反应,在一定温度下达平衡时,B的体积分数ψ(B)和压强P的关系如图所示,则下列有关该反应的描述正确的是( )
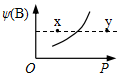 现有mA(s)+nB(g)?qC(g);△H<0的可逆反应,在一定温度下达平衡时,B的体积分数ψ(B)和压强P的关系如图所示,则下列有关该反应的描述正确的是( )
现有mA(s)+nB(g)?qC(g);△H<0的可逆反应,在一定温度下达平衡时,B的体积分数ψ(B)和压强P的关系如图所示,则下列有关该反应的描述正确的是( )| A. | m+n<q | B. | n>q | ||
| C. | x点比y点的正反应速率小 | D. | x点的混合物中v(正)<v(逆) |
1.一定条件下,一种反应物过量,另一种反应物仍不能完全反应的是( )
| A. | 过量的铁与浓硝酸 | B. | 过量的浓盐酸与二氧化锰 | ||
| C. | 过量的铜与浓硫酸 | D. | 过量的锌与18mol/L硫酸 |
18.NA代表阿伏加德罗常数的值,下列叙述不正确的是( )
| A. | 常温下,100 mL 1 mol•L-1 FeCl3溶液中含有Fe3+数目小于0.1NA | |
| B. | 1 mol-OH和17 g NH3所含的电子数相等 | |
| C. | 标准状况下,2.24 L Cl2与过量铁粉反应,转移的电子总数为2NA | |
| D. | 常温下,23 g NO2和N2O4的混合气体中含有NA个氧原子 |
19.在容量瓶上无需标有( )
| A. | 刻度线 | B. | 容量标准 | C. | 浓度 | D. | 温度 |
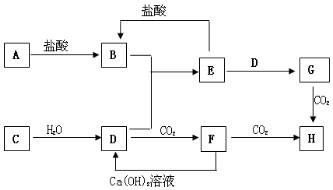 如图,图中A~H均为中学化学中常见的物质,它们之间有如下转化关系.其中A、C均为金属单质,C与水反应生成D和最轻的气体,D、H的焰色反应均呈黄色,在通常状况下E(氢氧化物)跟NaOH或盐酸均可发生复分解反应.(反应过程中生成的水及其他产物已略去)
如图,图中A~H均为中学化学中常见的物质,它们之间有如下转化关系.其中A、C均为金属单质,C与水反应生成D和最轻的气体,D、H的焰色反应均呈黄色,在通常状况下E(氢氧化物)跟NaOH或盐酸均可发生复分解反应.(反应过程中生成的水及其他产物已略去) ;F是Na2CO3.(填化学式)
;F是Na2CO3.(填化学式)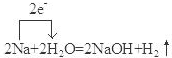 .
.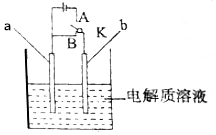 用如图所示装置进行实验,请回答下列问题:
用如图所示装置进行实验,请回答下列问题: