��Ŀ����
7������˵����ȷ���ǣ�������| A�� | �����£�NH4Cl��Һ��ˮϡ�ͣ�$\frac{c��N{H}_{3•}{H}_{2}O��•c��{H}^{+}��}{c��N{{H}_{4}}^{+}��}$���� | |
| B�� | 0.1mol/LNa2CO3��Һ���Ⱥ���Һ��pH��С | |
| C�� | ������ϡ��O��lmol/LCH3COOH��Һ����Һ�ĵ������������������Һ����������Ũ�Ⱦ���С | |
| D�� | ���ˮ�еμ�FeCl3������Һ�Ʊ�Fe��OH��3�����ԭ���Ǽ��ȴٽ�Fe3+ˮ�� |
���� A���Ȼ����Һ��笠�����ˮ�������ԣ�ˮ��ƽ�ⳣ�����䣻
B��̼������Һ��̼�������ˮ����Һ�Լ��ԣ�ˮ�ⷴӦΪ���ȷ�Ӧ�����ȴٽ�ˮ�⣻
C������Ϊ������Һ�д��ڵ���ƽ�⣬ϡ����Һ�ٽ�����ƽ��������У�ƽ��״̬�µ�����Ũ�ȼ�С����Һ�д������ӻ�������
D�����ȴٽ��˵�Fe3+ˮ�⣻
��� �⣺A�������£�NH4Cl��Һ�д���ˮ��ƽ�⣬NH4++H2O?NH3•H2O+H+����ˮϡ�ʹٽ�ˮ�⣬��ˮ��ƽ�ⳣ�����䣬$\frac{c��N{H}_{3}•{H}_{2}O��c��{H}^{+}��}{c��N{{H}_{4}}^{+}��}$���䣬��A����
B��̼������Һ��̼�������ˮ����Һ�Լ��ԣ�CO32-+H2O?HCO3-+OH-�����ȴٽ�ˮ��ƽ��������У���Һ������ǿ��PH����B����
C��CH3COOH��Һ��ˮϡ����Һ�ĵ������������������Һ��ƽ��״̬������Ũ�Ⱦ���С����Һ������������Ũ������C����
D�����ˮ�еμ�FeCl3������Һ�Ƹ�Fe��OH��3�����ԭ���Ǽ��ȴٽ���Fe3+ˮ�⣬��D��ȷ��
��ѡD��
���� ���⿴��������ˮ�⡢������ʵ���ƽ�⡢Ӱ��ƽ��״̬�����ط����жϣ�ע��ƽ�ⳣ�������ӻ������ķ��������ջ����ǽ���Ĺؼ�����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
17�������й�������ԭ��Ӧ��������ȷ���ǣ�������
| A�� | ���������ڷ�Ӧ��ֻ����ԭ�� | |
| B�� | �ǽ��������ڷ�Ӧ��ֻ�������� | |
| C�� | ����ʧ����Խ�࣬�仹ԭ��Խǿ���� | |
| D�� | Cu2+��Fe2+������ǿ��Fe��Cu��ԭ��ǿ |
18������һ����ʾ��ҺŨ�ȵ�λ���ǣ�������
| A�� | g/L | B�� | % | C�� | mol•L-1 | D�� | L/mol |
15������ʵ���ܻ�óɹ����ǣ�������
| A�� | 140��ʱ����ˮ�Ҵ���Ũ���Ṳ�ȿ��Ʊ���ϩ | |
| B�� | ����֬�м�ϡ������֮���ȿɷ���������Ӧ | |
| C�� | ���õ���Һ��������Ƿ�ˮ����ȫ | |
| D�� | ��֤�������е���Ԫ�أ���ֱ�Ӽ�AgNO3��Һ�۲��Ƿ��е���ɫ�������� |
2�����й���������ԭ��Ӧ����������ȷ���ǣ�������
| A�� | ʧȥ���ӵķ�Ӧ�ǻ�ԭ��Ӧ | B�� | ����������Ӧ���������� | ||
| C�� | �������������ʲ���ͬʱ����ԭ�� | D�� | ʧȥ���ӵ������ǻ�ԭ�� |
12�����ճ��л�ѧ�ķ���������з�Ӧ������������Ӧ�����ڻ��Ϸ�Ӧ���ǣ�������
| A�� | NaHCO3+HCl�TNaCl+H2O+CO2�� | B�� | 2KClO3$\frac{\underline{\;MnO_{2}\;}}{��}$ 2KCl+2O2�� | ||
| C�� | S+O2$\frac{\underline{\;��ȼ\;}}{\;}$SO2 | D�� | 2CuO+C$\frac{\underline{\;\;��\;\;}}{\;}$2Cu+CO2 |
13����NAΪ�����ӵ�������ֵ������˵����ȷ���ǣ�������
| A�� | 1L 0.1mol/L�İ�ˮ����0.1NA��NH4+ | |
| B�� | ��״���£�22.4L���Ậ��NA��HCI���� | |
| C�� | ���³�ѹ�£�14g��N2��CO�Ļ�����庬��0.5NA��ԭ�� | |
| D�� | ��״���£�6.72L N02��ˮ��ַ�Ӧת��0.2NA������ |
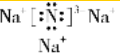 ���û������������Ӽ��γɵģ�
���û������������Ӽ��γɵģ�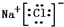 ��
��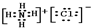 ��
��