1.下列物质的化学式中,具有非极性键的离子化合物是( )
| A. | Na2O | B. | MgF2 | C. | NaOH | D. | Na2O2 |
9.2016年诺贝尔化学奖授予美国、法国、荷兰的三位科学家,以表彰他们在分子机器设计与合成领域的杰出贡献.下列物质是由分子构成的是( )
| A. | 金刚石 | B. | 氧化铝 | C. | 聚乙烯 | D. | 不锈钢 |
6.常温下,下列有关电解质溶液的说法,正确的是( )
| A. | 1mol/L的CH3COOH溶液和0.1mol/L的CH3COOH溶液,水的电离程度前者大于后者 | |
| B. | pH=2的HA溶液和pH=12的NaOH溶液等体积混合后溶液显碱性,则混合后的溶液中存在平衡:A-+H2O?HA+OH- | |
| C. | 已知同浓度的NaA、NaB、NaX溶液碱性逐渐增强,则Ks(HA)<Ks(HB)<Ks(HX) | |
| D. | 已知常温下AgCl的Ksp=1.56×10-10,则浓度均为2.2×10-5mol/L的AgNO3溶液、NaCl溶液等体积混合,会产生AgCl白色沉淀 |
5.室温下,将0.05mol Na2CO3固体溶于水配成100mL溶液,向溶液中加入下列物质.有关结论正确的是( )
| 加入的物质 | 结论 | |
| A | 50mL 1mol/L H2SO4 | 反应结束后,c(Na+)=c(SO42-) |
| B | 0.5mol CaO | 溶液中$\frac{c(O{H}^{-})}{c(HC{O}_{3}^{-})}$增大 |
| C | 50mL H2O | 由水电离出的c(H+)•c(OH-)不变 |
| D | 0.1mol NaHSO4固体 | 反应完全后,溶液pH减小,c (Na+)不变 |
| A. | A | B. | B | C. | C | D. | D |
4.下列物质中既能与盐酸反应,又可与KOH溶液反应的是( )
| A. | 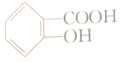 | B. | 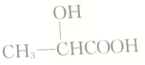 | C. | 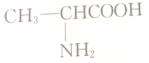 | D. | 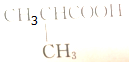 |
3.下列物质的性质与应用的对应关系正确的是( )
0 160946 160954 160960 160964 160970 160972 160976 160982 160984 160990 160996 161000 161002 161006 161012 161014 161020 161024 161026 161030 161032 161036 161038 161040 161041 161042 161044 161045 161046 161048 161050 161054 161056 161060 161062 161066 161072 161074 161080 161084 161086 161090 161096 161102 161104 161110 161114 161116 161122 161126 161132 161140 203614
| A. | MgO的熔点很高,可用于制造耐火材料 | |
| B. | (NH4)2SO4浓溶液能使蛋白质溶液发生盐析,可用于杀菌消毒 | |
| C. | 常温下Al与浓硝酸不反应,可以用铝槽车运输浓硝酸 | |
| D. | 碳具有强还原性,高温下能将二氧化硅还原为硅 |