16.化学反应中,反应物用量、浓度或反应条件不同可能对生成物产生影响.下列反应的生成物不受上述因素影响的是( )
| A. | 铜与硝酸反应 | B. | 钠与氧气反应 | ||
| C. | 氢气与氯气反应 | D. | 氯化铝与氢氧化钠溶液反应 |
15.用Cl2生产某些含氯有机物时会生成副产物HCl,利用下列反应可实现氯的循环利用:
4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6kJ/mol
恒温恒容的密闭容器中,充入一定量的反应物发生上述反应,能充分说明该反应达到化学平衡状态的是
( )
4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6kJ/mol
恒温恒容的密闭容器中,充入一定量的反应物发生上述反应,能充分说明该反应达到化学平衡状态的是
( )
| A. | 气体的质量不再改变 | |
| B. | 氯化氢的转化率不再改变 | |
| C. | 断开4 mol H-Cl键的同时生成4 mol H-O键 | |
| D. | n(HCl):n(O2):n(Cl2):n(H2O)=4:1:2:2 |
14.下列化学用语表述正确的是( )
| A. | 二氧化碳的结构式:O=C=O | B. | 氯化氢的电子式: | ||
| C. | ${\;}_{1}^{3}$H的原子结构示意图: | D. | 水的电离方程式:H2O=H++OH- |
12.室温下,向100mL 0.1mol/L NH4Cl溶液中加入下列物质.有关结论正确的是( )
| 加入的物质 | 结论 | |
| A. | 100 mL 0.1 mol/L盐酸 | 溶液中2c=c(Cl-) |
| B. | 0.01 mol Na2O2固体 | 反应完全后,溶液pH增大,c(Na+)=2c(Cl-) |
| C. | 100 mL H2O | 由水电离出的c(H+)•c(OH-)不变 |
| D. | 100 mL 0.1 mol/L NH3•H2O | 溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$减小 |
| A. | A | B. | B | C. | C | D. | D |
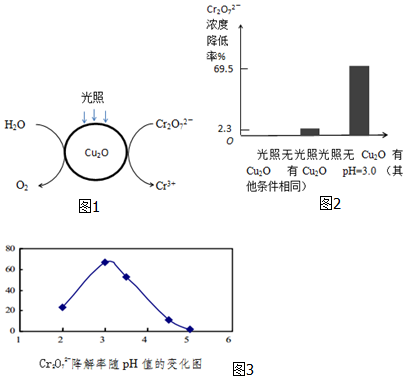
11. H2O2广泛应用于化学品合成、纸浆和纺织品的漂白,是环保型液体漂白剂.有研究表明,H2O2溶液的漂白性是HO2-所致.
H2O2广泛应用于化学品合成、纸浆和纺织品的漂白,是环保型液体漂白剂.有研究表明,H2O2溶液的漂白性是HO2-所致.
(1)H2O2溶液显弱酸性,测得0.15mol•L-1H2O2溶液pH约为6.写出H2O2生成HO2-的电离方程式:H2O2?HO2-+H+.
(2)其他条件相同时,研究不同初始pH条件下H2O2溶液的漂白效果,结果如下:由图可得到的结论是其他条件相同时,初始pH越大染料脱色率越高,即H2O2的漂白效果越好,结合平衡移动原理简述理由:c(OH-)增大,促使H2O2?HO2-+H+正向移动,c(HO2-)增大.
(3)实验发现:若pH>11,则H2O2溶液的漂白效果随pH增大而降低.针对这一现象,继续进行实验,发现溶液中H2O2的分解与pH有关.测定不同初始pH条件下,初始浓度均为0.15mol•L-1的H2O2溶液发生分解反应,结果如表:
查阅资料:HO2-+H2O2═H2O+O2+OH-.
①结合离子方程式解释1小时后pH没有明显变化的原因:碱性条件下:H2O2+OH-═HO2-+H2O,又知HO2-+H2O2═H2O+O2+OH-,OH-可看作是H2O2分解反应的催化剂,故反应前后pH不变.
②从反应速率的角度分析pH过大,H2O2溶液漂白效果会降低的原因:pH过大,H2O2分解过快,使参与漂白的c(HO2-)下降,故漂白效果降低.
 H2O2广泛应用于化学品合成、纸浆和纺织品的漂白,是环保型液体漂白剂.有研究表明,H2O2溶液的漂白性是HO2-所致.
H2O2广泛应用于化学品合成、纸浆和纺织品的漂白,是环保型液体漂白剂.有研究表明,H2O2溶液的漂白性是HO2-所致.(1)H2O2溶液显弱酸性,测得0.15mol•L-1H2O2溶液pH约为6.写出H2O2生成HO2-的电离方程式:H2O2?HO2-+H+.
(2)其他条件相同时,研究不同初始pH条件下H2O2溶液的漂白效果,结果如下:由图可得到的结论是其他条件相同时,初始pH越大染料脱色率越高,即H2O2的漂白效果越好,结合平衡移动原理简述理由:c(OH-)增大,促使H2O2?HO2-+H+正向移动,c(HO2-)增大.
(3)实验发现:若pH>11,则H2O2溶液的漂白效果随pH增大而降低.针对这一现象,继续进行实验,发现溶液中H2O2的分解与pH有关.测定不同初始pH条件下,初始浓度均为0.15mol•L-1的H2O2溶液发生分解反应,结果如表:
| 初始pH | pH=10 | pH=12 |
| 1小时后H2O2溶液浓度 | 0.13mol•L-1 | 0.07mol•L-1 |
| 1小时后pH | 没有明显变化 | 没有明显变化 |
①结合离子方程式解释1小时后pH没有明显变化的原因:碱性条件下:H2O2+OH-═HO2-+H2O,又知HO2-+H2O2═H2O+O2+OH-,OH-可看作是H2O2分解反应的催化剂,故反应前后pH不变.
②从反应速率的角度分析pH过大,H2O2溶液漂白效果会降低的原因:pH过大,H2O2分解过快,使参与漂白的c(HO2-)下降,故漂白效果降低.
10.为探究FeCl3溶液中的离子平衡和离子反应,某小组同学进行了如下实验.
(1)配制50mL 1.0mol•L-1的FeCl3溶液,测其pH约为0.7,即c(H+)=0.2mol•L-1.
①用化学用语解释FeCl3溶液呈酸性的原因:Fe3++3H2O?Fe(OH)3+3H+.
②下列实验方案中,能使FeCl3溶液pH升高的是acd(填字母序号).
a.加水稀释 b.加入FeCl3固体 c.滴加浓KSCN溶液 d.加入NaHCO3固体
(2)小组同学利用上述FeCl3溶液探究其与足量锌粉的反应.实验操作及现象如表:
已知:Zn的性质与Al相似,能发生反应:Zn+2NaOH═Na2ZnO2+H2↑
①结合实验现象和平衡移动原理解释出现红褐色沉淀的原因:溶液温度升高,反应过程中出现H2使溶液中c(H+)降低,都会促进Fe3++3H2O?Fe(OH)3+3H+正向移动,出现红褐色Fe(OH)3沉淀.
②用离子方程式解释反应后溶液为浅绿色的原因:2Fe3++Zn═2Fe2++Zn2+.
③分离出黑色固体,经下列实验证实了其中含有的主要物质.
i.黑色固体可以被磁铁吸引;
ii.向黑色固体中加入足量的NaOH溶液,产生气泡;
iii.将ii中剩余固体用蒸馏水洗涤后,加入稀盐酸,产生大量气泡;
iv.向iii反应后的溶液中滴加KSCN溶液,无变化.
a.黑色固体中一定含有的物质是Fe和Zn.
b.小组同学认为上述实验无法确定黑色固体中是否含有Fe3O4,理由是iii中,若存在Fe3O4,稀盐酸与Fe3O4反应产生的Fe3+可与Fe继续反应生成Fe2+,导致在iv中检测不到Fe3+,与没有Fe3O4得到的iv中现象相同.
(3)为进一步探究上述1.0mol•L-1FeCl3溶液中Fe3+和H+氧化性的相对强弱,继续实验并观察到反应开始时现象如表:
小组同学得出结论:在1.0mol•L-1FeCl3溶液中,Fe3+的氧化性比H+更强.
(1)配制50mL 1.0mol•L-1的FeCl3溶液,测其pH约为0.7,即c(H+)=0.2mol•L-1.
①用化学用语解释FeCl3溶液呈酸性的原因:Fe3++3H2O?Fe(OH)3+3H+.
②下列实验方案中,能使FeCl3溶液pH升高的是acd(填字母序号).
a.加水稀释 b.加入FeCl3固体 c.滴加浓KSCN溶液 d.加入NaHCO3固体
(2)小组同学利用上述FeCl3溶液探究其与足量锌粉的反应.实验操作及现象如表:
| 操作 | 现象 |
| 向反应瓶中加入6.5g锌粉,然后加入50mL 1.0mol•L-1的FeCl3溶液,搅拌 | 溶液温度迅速上升,稍后出现红褐色沉淀,同时出现少量气泡;反应一段时间后静置,上层溶液为浅绿色,反应瓶底部有黑色固体 |
| 收集检验反应过程中产生的气体 | 集气管口靠近火焰,有爆鸣声 |
①结合实验现象和平衡移动原理解释出现红褐色沉淀的原因:溶液温度升高,反应过程中出现H2使溶液中c(H+)降低,都会促进Fe3++3H2O?Fe(OH)3+3H+正向移动,出现红褐色Fe(OH)3沉淀.
②用离子方程式解释反应后溶液为浅绿色的原因:2Fe3++Zn═2Fe2++Zn2+.
③分离出黑色固体,经下列实验证实了其中含有的主要物质.
i.黑色固体可以被磁铁吸引;
ii.向黑色固体中加入足量的NaOH溶液,产生气泡;
iii.将ii中剩余固体用蒸馏水洗涤后,加入稀盐酸,产生大量气泡;
iv.向iii反应后的溶液中滴加KSCN溶液,无变化.
a.黑色固体中一定含有的物质是Fe和Zn.
b.小组同学认为上述实验无法确定黑色固体中是否含有Fe3O4,理由是iii中,若存在Fe3O4,稀盐酸与Fe3O4反应产生的Fe3+可与Fe继续反应生成Fe2+,导致在iv中检测不到Fe3+,与没有Fe3O4得到的iv中现象相同.
(3)为进一步探究上述1.0mol•L-1FeCl3溶液中Fe3+和H+氧化性的相对强弱,继续实验并观察到反应开始时现象如表:
| 操作 | 现象 |
| 将5mL 1.0mol•L-1的FeCl3溶液与0.65g锌粉混合 | 溶液温度迅速上升,开始时几乎没有气泡 |
| 将5 mL 0.2 mol•L-1(或pH=0.7)的盐酸与0.65g锌粉混合 | 溶液中立即产生大量气泡 |
9. 我国科研人员研制出一种室温“可呼吸”Na-CO2电池.放电时该电池“吸入”CO2,充电时“呼出”CO2.吸入CO2时,其工作原理如图所示.吸收的全部CO2中,有$\frac{2}{3}$转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面.下列说法正确的是( )
我国科研人员研制出一种室温“可呼吸”Na-CO2电池.放电时该电池“吸入”CO2,充电时“呼出”CO2.吸入CO2时,其工作原理如图所示.吸收的全部CO2中,有$\frac{2}{3}$转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面.下列说法正确的是( )
 我国科研人员研制出一种室温“可呼吸”Na-CO2电池.放电时该电池“吸入”CO2,充电时“呼出”CO2.吸入CO2时,其工作原理如图所示.吸收的全部CO2中,有$\frac{2}{3}$转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面.下列说法正确的是( )
我国科研人员研制出一种室温“可呼吸”Na-CO2电池.放电时该电池“吸入”CO2,充电时“呼出”CO2.吸入CO2时,其工作原理如图所示.吸收的全部CO2中,有$\frac{2}{3}$转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面.下列说法正确的是( )| A. | “吸入”CO2时,钠箔为正极 | |
| B. | “呼出”CO2时,Na+向多壁碳纳米管电极移动 | |
| C. | “吸入”CO2时的正极反应:4Na++3CO2+4e-═2Na2CO3+C | |
| D. | 标准状况下,每“呼出”22.4 L CO2,转移电子数为0.75 mol |
8.某同学进行下列实验:
下列说法不合理的是( )
| 操作 | 现象 |
 取一块打磨过的生铁片,在其表面滴1滴含酚酞和K3[Fe(CN)6]的食盐水 | 放置一段时间后,生铁片上出现如图所示“斑痕”.其边缘处为红色,中心区域为蓝色,在两色环交界处出现铁锈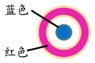 |
| A. | 生铁片发生吸氧腐蚀 | |
| B. | 中心区:Fe-2e-═Fe2+ | |
| C. | 边缘处:O2+2H2O+4e-═4OH- | |
| D. | 交界处:4Fe2++O2+10H2O═4 Fe(OH)3+8H+ |
7.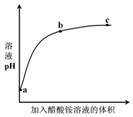 室温下,向0.01mol•L-1的醋酸溶液中滴入pH=7的醋酸铵溶液,溶液pH随滴入醋酸铵
室温下,向0.01mol•L-1的醋酸溶液中滴入pH=7的醋酸铵溶液,溶液pH随滴入醋酸铵
溶液体积变化的曲线示意图如图所示.下列分析正确的是( )
0 160775 160783 160789 160793 160799 160801 160805 160811 160813 160819 160825 160829 160831 160835 160841 160843 160849 160853 160855 160859 160861 160865 160867 160869 160870 160871 160873 160874 160875 160877 160879 160883 160885 160889 160891 160895 160901 160903 160909 160913 160915 160919 160925 160931 160933 160939 160943 160945 160951 160955 160961 160969 203614
 室温下,向0.01mol•L-1的醋酸溶液中滴入pH=7的醋酸铵溶液,溶液pH随滴入醋酸铵
室温下,向0.01mol•L-1的醋酸溶液中滴入pH=7的醋酸铵溶液,溶液pH随滴入醋酸铵溶液体积变化的曲线示意图如图所示.下列分析正确的是( )
| A. | a点,pH=2 | |
| B. | b点,c(CH3COO-)>c(NH4+) | |
| C. | c点,pH可能大于7 | |
| D. | ac段,溶液pH增大是CH3COOH?H++CH3COO-逆向移动的结果 |