题目内容
15.用Cl2生产某些含氯有机物时会生成副产物HCl,利用下列反应可实现氯的循环利用:4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6kJ/mol
恒温恒容的密闭容器中,充入一定量的反应物发生上述反应,能充分说明该反应达到化学平衡状态的是
( )
| A. | 气体的质量不再改变 | |
| B. | 氯化氢的转化率不再改变 | |
| C. | 断开4 mol H-Cl键的同时生成4 mol H-O键 | |
| D. | n(HCl):n(O2):n(Cl2):n(H2O)=4:1:2:2 |
分析 化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,得出正确结论.
解答 解:A、气体的质量一直不变,所以不一定达平衡状态,故A错误;
B、氯化氢的转化率不再改变,说明各物质的量不变,反应达平衡状态,故B正确;
C、只要反应发生就存在断开4 mol H-Cl键的同时生成4 mol H-O键,故C错误;
D、n(HCl):n(O2):n(Cl2):n(H2O)=4:1:2:2,不能说明各物质的量不变,故D错误;
故选B.
点评 本题考查化学平衡状态的判断,题目难度不大.要注意把握平衡状态的特征.

练习册系列答案
相关题目
3.关于SO2性质和现象的对应描述,正确的是( )
| A. | SO2具有氧化性,能使品红溶液褪色 | |
| B. | SO2具有漂白性,能使溴水褪色 | |
| C. | SO2具有还原性,能与Ba(NO3)2溶液反应生成沉淀 | |
| D. | SO2具有漂白性,能使滴加酚酞的NaOH溶液由红色变为无色 |
10.为探究FeCl3溶液中的离子平衡和离子反应,某小组同学进行了如下实验.
(1)配制50mL 1.0mol•L-1的FeCl3溶液,测其pH约为0.7,即c(H+)=0.2mol•L-1.
①用化学用语解释FeCl3溶液呈酸性的原因:Fe3++3H2O?Fe(OH)3+3H+.
②下列实验方案中,能使FeCl3溶液pH升高的是acd(填字母序号).
a.加水稀释 b.加入FeCl3固体 c.滴加浓KSCN溶液 d.加入NaHCO3固体
(2)小组同学利用上述FeCl3溶液探究其与足量锌粉的反应.实验操作及现象如表:
已知:Zn的性质与Al相似,能发生反应:Zn+2NaOH═Na2ZnO2+H2↑
①结合实验现象和平衡移动原理解释出现红褐色沉淀的原因:溶液温度升高,反应过程中出现H2使溶液中c(H+)降低,都会促进Fe3++3H2O?Fe(OH)3+3H+正向移动,出现红褐色Fe(OH)3沉淀.
②用离子方程式解释反应后溶液为浅绿色的原因:2Fe3++Zn═2Fe2++Zn2+.
③分离出黑色固体,经下列实验证实了其中含有的主要物质.
i.黑色固体可以被磁铁吸引;
ii.向黑色固体中加入足量的NaOH溶液,产生气泡;
iii.将ii中剩余固体用蒸馏水洗涤后,加入稀盐酸,产生大量气泡;
iv.向iii反应后的溶液中滴加KSCN溶液,无变化.
a.黑色固体中一定含有的物质是Fe和Zn.
b.小组同学认为上述实验无法确定黑色固体中是否含有Fe3O4,理由是iii中,若存在Fe3O4,稀盐酸与Fe3O4反应产生的Fe3+可与Fe继续反应生成Fe2+,导致在iv中检测不到Fe3+,与没有Fe3O4得到的iv中现象相同.
(3)为进一步探究上述1.0mol•L-1FeCl3溶液中Fe3+和H+氧化性的相对强弱,继续实验并观察到反应开始时现象如表:
小组同学得出结论:在1.0mol•L-1FeCl3溶液中,Fe3+的氧化性比H+更强.
(1)配制50mL 1.0mol•L-1的FeCl3溶液,测其pH约为0.7,即c(H+)=0.2mol•L-1.
①用化学用语解释FeCl3溶液呈酸性的原因:Fe3++3H2O?Fe(OH)3+3H+.
②下列实验方案中,能使FeCl3溶液pH升高的是acd(填字母序号).
a.加水稀释 b.加入FeCl3固体 c.滴加浓KSCN溶液 d.加入NaHCO3固体
(2)小组同学利用上述FeCl3溶液探究其与足量锌粉的反应.实验操作及现象如表:
| 操作 | 现象 |
| 向反应瓶中加入6.5g锌粉,然后加入50mL 1.0mol•L-1的FeCl3溶液,搅拌 | 溶液温度迅速上升,稍后出现红褐色沉淀,同时出现少量气泡;反应一段时间后静置,上层溶液为浅绿色,反应瓶底部有黑色固体 |
| 收集检验反应过程中产生的气体 | 集气管口靠近火焰,有爆鸣声 |
①结合实验现象和平衡移动原理解释出现红褐色沉淀的原因:溶液温度升高,反应过程中出现H2使溶液中c(H+)降低,都会促进Fe3++3H2O?Fe(OH)3+3H+正向移动,出现红褐色Fe(OH)3沉淀.
②用离子方程式解释反应后溶液为浅绿色的原因:2Fe3++Zn═2Fe2++Zn2+.
③分离出黑色固体,经下列实验证实了其中含有的主要物质.
i.黑色固体可以被磁铁吸引;
ii.向黑色固体中加入足量的NaOH溶液,产生气泡;
iii.将ii中剩余固体用蒸馏水洗涤后,加入稀盐酸,产生大量气泡;
iv.向iii反应后的溶液中滴加KSCN溶液,无变化.
a.黑色固体中一定含有的物质是Fe和Zn.
b.小组同学认为上述实验无法确定黑色固体中是否含有Fe3O4,理由是iii中,若存在Fe3O4,稀盐酸与Fe3O4反应产生的Fe3+可与Fe继续反应生成Fe2+,导致在iv中检测不到Fe3+,与没有Fe3O4得到的iv中现象相同.
(3)为进一步探究上述1.0mol•L-1FeCl3溶液中Fe3+和H+氧化性的相对强弱,继续实验并观察到反应开始时现象如表:
| 操作 | 现象 |
| 将5mL 1.0mol•L-1的FeCl3溶液与0.65g锌粉混合 | 溶液温度迅速上升,开始时几乎没有气泡 |
| 将5 mL 0.2 mol•L-1(或pH=0.7)的盐酸与0.65g锌粉混合 | 溶液中立即产生大量气泡 |
20.铅蓄电池是常见的二次电池,电池总反应为:Pb+PbO2+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O.下列说法正确的是( )
| A. | 放电时PbO2发生氧化反应 | |
| B. | 充电时电解质溶液的质量减少 | |
| C. | 放电时的负极反应式为Pb+SO42--2e-=PbSO4 | |
| D. | 充电时的阴极反应式为PbSO4+2H2O-2e-=PbO2+SO42-+4H+ |
7.按照物质的树状分类和交叉分类,氯水应属于( )
①酸 ②能导电 ③胶体 ④混合物 ⑤化合物 ⑥溶液 ⑦电解质.
①酸 ②能导电 ③胶体 ④混合物 ⑤化合物 ⑥溶液 ⑦电解质.
| A. | ①②④⑥⑦ | B. | ①②⑤⑦ | C. | ②④⑥ | D. | ②④⑥⑦ |
4. 已知 X、Y、Z、Q、R、E六种前四周期元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如表.
已知 X、Y、Z、Q、R、E六种前四周期元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如表.
请根据信息回答有关问题:
(1)写出元素Y的原子核外价电子排布图: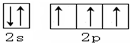 .X的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为3:2.
.X的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为3:2.
(2)X、Y、Z三种元素的第一电离能由高到低的排列为(写元素符号)N>O>C.
(3)X、Z元素分别与氢元素形成的最简单化合物中,沸点较高的为(写化学式)H2O,原因是水分子间可以形成氢键,使沸点升高.
(4)XZ与Y2属于等电子体,写出化合物XZ的结构式:C≡O.
(5)R的一种配合物的化学式为RCl3•6H2O.已知0.01mol RCl3•6H2O在水溶液中用过量硝酸银溶液处理,产生0.02mol AgCl沉淀.此配合物最可能是B.
A.[R(H2O)6]Cl3B.[R(H2O)5Cl]Cl2•H2O
C.[R(H2O)4Cl2]Cl•2H2OD.[R(H2O)3Cl3]•3H2O
(6)向含少量ESO4的水溶液中逐滴滴入氨水,生成蓝色沉淀,反应的离子方程式为:Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+,继续滴加氨水至过量,沉淀溶解,
得到天蓝色溶液,写反应的离子方程式为:Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-.
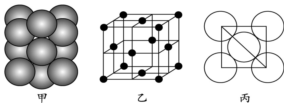
(7)元素E的单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示.
若已知该元素的原子半径为d cm,相对原子质量为M,NA代表阿伏加德罗常数,则该晶体的密度为$\frac{M}{4\sqrt{2}{d}^{3}{N}_{A}}$g•cm-3(用字母表示).
 已知 X、Y、Z、Q、R、E六种前四周期元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如表.
已知 X、Y、Z、Q、R、E六种前四周期元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如表.| 元素 | 结构或性质信息 |
| X | 原子的L层上s电子数等于p电子数 |
| Y | 原子核外的L层有3个未成对电子 |
| Z | 地壳中含量最多的元素 |
| Q | 单质常温常压下是气体,原子的M层上有1个未成对的p电子 |
| R | 核电荷数是Y与Q的核电荷数之和 |
| E | N能层上只有一个电子,K、L、M层均排满电子 |
(1)写出元素Y的原子核外价电子排布图:
 .X的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为3:2.
.X的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为3:2.(2)X、Y、Z三种元素的第一电离能由高到低的排列为(写元素符号)N>O>C.
(3)X、Z元素分别与氢元素形成的最简单化合物中,沸点较高的为(写化学式)H2O,原因是水分子间可以形成氢键,使沸点升高.
(4)XZ与Y2属于等电子体,写出化合物XZ的结构式:C≡O.
(5)R的一种配合物的化学式为RCl3•6H2O.已知0.01mol RCl3•6H2O在水溶液中用过量硝酸银溶液处理,产生0.02mol AgCl沉淀.此配合物最可能是B.
A.[R(H2O)6]Cl3B.[R(H2O)5Cl]Cl2•H2O
C.[R(H2O)4Cl2]Cl•2H2OD.[R(H2O)3Cl3]•3H2O
(6)向含少量ESO4的水溶液中逐滴滴入氨水,生成蓝色沉淀,反应的离子方程式为:Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+,继续滴加氨水至过量,沉淀溶解,
得到天蓝色溶液,写反应的离子方程式为:Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-.
(7)元素E的单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示.
若已知该元素的原子半径为d cm,相对原子质量为M,NA代表阿伏加德罗常数,则该晶体的密度为$\frac{M}{4\sqrt{2}{d}^{3}{N}_{A}}$g•cm-3(用字母表示).
 +3Br2→
+3Br2→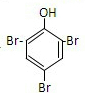 +3HBr
+3HBr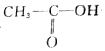 +H-O-CH2CH3$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O
+H-O-CH2CH3$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O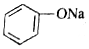 +CO2+H2O→C6H5OH+NaHCO3.
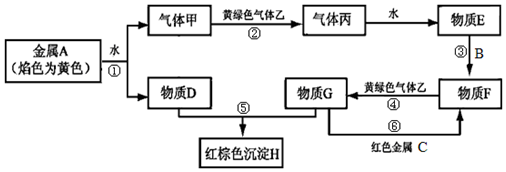
+CO2+H2O→C6H5OH+NaHCO3.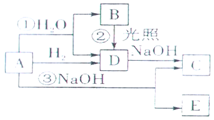 A是黄绿色气体单质,如图所示,
A是黄绿色气体单质,如图所示,