2.“结晶玫瑰”具有强烈的玫瑰香气,是一种很好的定香剂.其化学名称为“乙酸三氯甲基苯甲酯”,通常用三氯甲基苯基甲醇和醋酸酐为原料制备:
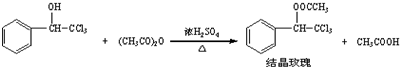
已知:
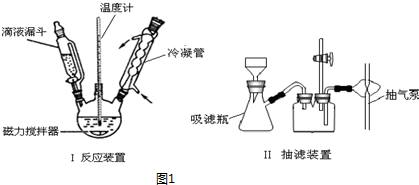
操作步骤和装置(图1)如下:
$\stackrel{加料}{→}$$→_{温度在110℃}^{加热3小时,控制}$$→_{入冰水中}^{反应液倒}$$\stackrel{抽滤}{→}$粗产品$\stackrel{重结晶}{→}$产品
请根据以上信息,回答下列问题:
(1)加料时,应先加入三氯甲基苯基甲醇和醋酸酐,然后慢慢加入浓硫酸并搅拌(或开启磁力搅拌器).待混合均匀后,最适宜的加热方式为油浴加热(填“水浴加热”,“油浴加热”,“砂浴加热”).
(2)用图II抽滤装置操作时,布氏漏斗的漏斗管插入单孔橡胶塞与吸滤瓶相接.橡胶塞插入吸滤瓶内的部分不得超过塞子高度的$\frac{2}{3}$;向漏斗中加入溶液,溶液量不应超过漏斗容量的$\frac{2}{3}$;当吸滤瓶中液面快达到支管口位置时,应拔掉吸滤瓶上的橡皮管,从吸滤瓶上口 倒出溶液.
(3)重结晶提纯时,应将粗产品溶解在无水乙醇中(填“水”,“无水乙醇”,“粗产品滤液”).已知70℃时100g 溶剂中溶解a g结晶玫瑰,重结晶操作过程为:按粗产品、溶剂的质量比为1:$\frac{100}{a}$混合,用水浴加热回流溶剂使粗产品充分溶解,然后待晶体完全溶解后停止加热(若溶液沸腾时还未全部溶解,可再加少量溶剂)冷却结晶,抽滤,此重结晶过程中不需要用到的仪器是c.
A.冷凝管 B.烧杯 C.蒸发皿 D.锥形瓶
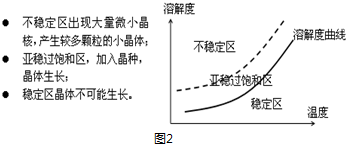
(4)某同学欲在重结晶时获得较大的晶体,查阅资料得到如图2信息:由信息可知,从高温浓溶液中获得较大晶体的操作为加入晶种,缓慢降温.
(5)在物质制备实验中,产品经抽滤、洗涤后,尚需干燥,请列举一种常见的实验室干燥方法.空气中风干、空气中晾干、高温烘干、用滤纸吸干.

已知:
| 三氯甲基苯基甲醇 | 无色液体.不溶于水,溶于乙醇. |
| 醋酸酐 | 无色液体.溶于水形成乙酸,溶于乙醇. |
| 结晶玫瑰 | 白色至微黄色晶体.不溶于水,溶于乙醇.熔点:88℃ |
| 醋酸 | 无色的吸湿性液体,易溶于水、乙醇. |
$\stackrel{加料}{→}$$→_{温度在110℃}^{加热3小时,控制}$$→_{入冰水中}^{反应液倒}$$\stackrel{抽滤}{→}$粗产品$\stackrel{重结晶}{→}$产品

请根据以上信息,回答下列问题:
(1)加料时,应先加入三氯甲基苯基甲醇和醋酸酐,然后慢慢加入浓硫酸并搅拌(或开启磁力搅拌器).待混合均匀后,最适宜的加热方式为油浴加热(填“水浴加热”,“油浴加热”,“砂浴加热”).
(2)用图II抽滤装置操作时,布氏漏斗的漏斗管插入单孔橡胶塞与吸滤瓶相接.橡胶塞插入吸滤瓶内的部分不得超过塞子高度的$\frac{2}{3}$;向漏斗中加入溶液,溶液量不应超过漏斗容量的$\frac{2}{3}$;当吸滤瓶中液面快达到支管口位置时,应拔掉吸滤瓶上的橡皮管,从吸滤瓶上口 倒出溶液.
(3)重结晶提纯时,应将粗产品溶解在无水乙醇中(填“水”,“无水乙醇”,“粗产品滤液”).已知70℃时100g 溶剂中溶解a g结晶玫瑰,重结晶操作过程为:按粗产品、溶剂的质量比为1:$\frac{100}{a}$混合,用水浴加热回流溶剂使粗产品充分溶解,然后待晶体完全溶解后停止加热(若溶液沸腾时还未全部溶解,可再加少量溶剂)冷却结晶,抽滤,此重结晶过程中不需要用到的仪器是c.
A.冷凝管 B.烧杯 C.蒸发皿 D.锥形瓶

(4)某同学欲在重结晶时获得较大的晶体,查阅资料得到如图2信息:由信息可知,从高温浓溶液中获得较大晶体的操作为加入晶种,缓慢降温.
(5)在物质制备实验中,产品经抽滤、洗涤后,尚需干燥,请列举一种常见的实验室干燥方法.空气中风干、空气中晾干、高温烘干、用滤纸吸干.
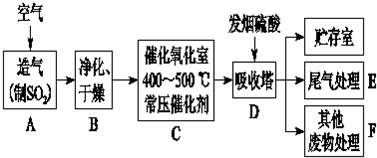
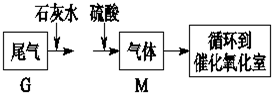
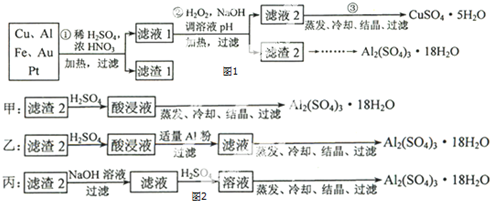
18.孔雀石的主要成分为Cu2(OH)2CO3还含少量二价铁和三价铁的氧化物及硅的氧化物.如图是实验室以孔雀石为原料制备CuSO4•5H2O晶体的流程图: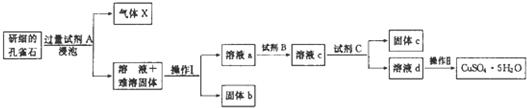
(1)试剂A的化学式是H2SO4;操作I的名称是过滤;
(2)操作Ⅱ的名称是蒸发浓缩、冷却结晶、过滤、洗涤、干燥;用到的仪器有:酒精灯、玻璃棒、蒸发皿、坩埚钳和三角架.
(3)使用试剂B的目的是将溶液中的Fe2+转化为Fe3+,试剂B最好选用B(填选项序号).
A.酸性KMnO4溶液 B.双氧水 C.浓硝酸 D.氯水
写出相应反应的离子方式:2Fe2++2H++H2O2=2Fe3++2H2O.
(4)已知
试剂C的使用是为了调节溶液的pH,使Fe3+转化为沉淀予以分离.试剂C宜选用D(填选项序号);
A.稀硫酸 B.NaOH溶液 C.氨水 D.CuCO3
为完全除去溶液c中的Fe3+而又不使Cu2+沉淀,则应调节溶液pH的范围为3.7~4.8.
(5)溶液c中含有的两种金属阳离子,若用色谱分析法检验,固定相是附着在滤纸上的水,滤纸的作用是惰性支持物.在流动相中分配较少的离子是Cu2+、氨熏后的颜色是深蓝色,其氨熏时的离子方程式为Cu2++4NH3•H20═[Cu(NH3)4]2++4H2O.

(1)试剂A的化学式是H2SO4;操作I的名称是过滤;
(2)操作Ⅱ的名称是蒸发浓缩、冷却结晶、过滤、洗涤、干燥;用到的仪器有:酒精灯、玻璃棒、蒸发皿、坩埚钳和三角架.
(3)使用试剂B的目的是将溶液中的Fe2+转化为Fe3+,试剂B最好选用B(填选项序号).
A.酸性KMnO4溶液 B.双氧水 C.浓硝酸 D.氯水
写出相应反应的离子方式:2Fe2++2H++H2O2=2Fe3++2H2O.
(4)已知
| 物质 | Fe(OH)3 | Cu(OH)2 |
| 开始沉淀时的pH | 2.3 | 4.8 |
| 完全沉淀时的pH | 3.7 | 6.7 |
A.稀硫酸 B.NaOH溶液 C.氨水 D.CuCO3
为完全除去溶液c中的Fe3+而又不使Cu2+沉淀,则应调节溶液pH的范围为3.7~4.8.
(5)溶液c中含有的两种金属阳离子,若用色谱分析法检验,固定相是附着在滤纸上的水,滤纸的作用是惰性支持物.在流动相中分配较少的离子是Cu2+、氨熏后的颜色是深蓝色,其氨熏时的离子方程式为Cu2++4NH3•H20═[Cu(NH3)4]2++4H2O.
17.下列有关电负性的说法中正确的是( )
| A. | 主族元素的电负性越大,元素原子的第一电离能一定越大 | |
| B. | 在元素周期表中,元素电负性从左到右越来越小 | |
| C. | 在形成化合物时,电负性越小的元素越容易显正价 | |
| D. | 金属元素的电负性一定小于非金属元素的电负性 |
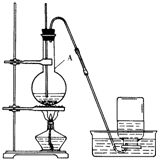
16.醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:

可能用到的有关数据如下:
合成反应:在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓硫酸.b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃.
分离提纯:反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙.最终通过蒸馏得到纯净环己烯10g.
回答下列问题:
(1)装置b的名称是直形冷凝器.
(2)加入碎瓷片的作用是防止暴沸;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加 B.冷却后补加
C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为
(4)分液漏斗在使用前须清洗干净并检漏;在本实验分离过程中,产物应该从分液漏斗的上口倒出(填“上口倒出”或“下口放出”).
(5)分离提纯过程中加入无水氯化钙的目的是干燥.
(6)在环己烯粗产物蒸馏过程中,不可能用到的仪器有CD(填正确答案标号).
A.圆底烧瓶 B.温度计 C.吸滤瓶
D.球形冷凝管 E.接收器
(7)本实验所得到的环己烯产率是C(填正确答案标号).
A.41% B.50%C.61% D.70%
0 159645 159653 159659 159663 159669 159671 159675 159681 159683 159689 159695 159699 159701 159705 159711 159713 159719 159723 159725 159729 159731 159735 159737 159739 159740 159741 159743 159744 159745 159747 159749 159753 159755 159759 159761 159765 159771 159773 159779 159783 159785 159789 159795 159801 159803 159809 159813 159815 159821 159825 159831 159839 203614

可能用到的有关数据如下:
| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.961 8 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.810 2 | 83 | 难溶于水 |
分离提纯:反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙.最终通过蒸馏得到纯净环己烯10g.
回答下列问题:
(1)装置b的名称是直形冷凝器.
(2)加入碎瓷片的作用是防止暴沸;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加 B.冷却后补加
C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为

(4)分液漏斗在使用前须清洗干净并检漏;在本实验分离过程中,产物应该从分液漏斗的上口倒出(填“上口倒出”或“下口放出”).
(5)分离提纯过程中加入无水氯化钙的目的是干燥.
(6)在环己烯粗产物蒸馏过程中,不可能用到的仪器有CD(填正确答案标号).
A.圆底烧瓶 B.温度计 C.吸滤瓶
D.球形冷凝管 E.接收器
(7)本实验所得到的环己烯产率是C(填正确答案标号).
A.41% B.50%C.61% D.70%
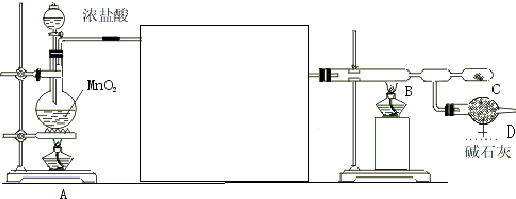
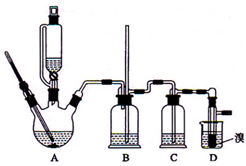 实验室制备1,2-二溴乙烷的反应原理是先用乙醇制备出乙烯,再将乙烯通入溴水中发生如下反应:CH2=CH2+Br2→BrCH2CH2Br.可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示.回答下列问题:
实验室制备1,2-二溴乙烷的反应原理是先用乙醇制备出乙烯,再将乙烯通入溴水中发生如下反应:CH2=CH2+Br2→BrCH2CH2Br.可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示.回答下列问题: