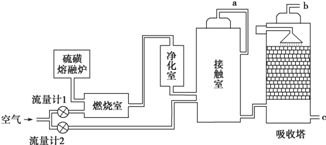
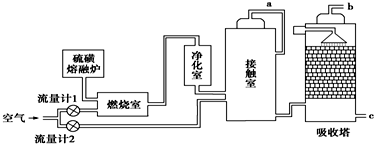
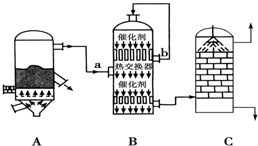
5.目前,我国采用“接触法”制硫酸.有关接触法制硫酸的下列说法中,正确的是( )
| A. | 二氧化硫的接触氧化在合成塔中发生 | |
| B. | 吸收塔得到的硫酸浓度为98% | |
| C. | 煅烧含硫48%的黄铁矿时,若FeS2损失了2%,则S损失4% | |
| D. | 接触室中适宜条件是V2O5作催化剂、高温、常压 | |
| E. | 接触室中采取高温是为了提高催化剂的活性和提高SO2的转化率 |
1.下列说法不符合生产实际的是( )
| A. | 硫酸工业的尾气中含有少量SO2,可用石灰水吸收,然后再用硫酸处理 | |
| B. | 工业上,常采用铁触媒催化剂,在400~500℃和10~30 MPa的条件下合成氨 | |
| C. | 造气中产生的CO,可在催化剂作用下,与水蒸气反应生成CO2和H2. | |
| D. | 在硫酸生产中,SO2催化氧化选择1~10 MPa、400~500℃条件下进行 |
12.亚磷酸(H3PO3)是二元酸,0.1000mol/L的H3PO3溶液pH=1.6.下列判断错误的是( )
| A. | HPO32-既能电离也能水解 | |
| B. | Na2HPO3溶液一定呈碱性 | |
| C. | H3PO3具有还原性 | |
| D. | H3PO3的溶液中加入过量NaOH,生成Na3PO3 |
11.为探究铁钉和钢钉在碱性溶液中遇到高锰酸钾时是否存在电化学腐蚀,进行下图所示实验.下列推断正确的是( )
0 155389 155397 155403 155407 155413 155415 155419 155425 155427 155433 155439 155443 155445 155449 155455 155457 155463 155467 155469 155473 155475 155479 155481 155483 155484 155485 155487 155488 155489 155491 155493 155497 155499 155503 155505 155509 155515 155517 155523 155527 155529 155533 155539 155545 155547 155553 155557 155559 155565 155569 155575 155583 203614

| A. | 钢钉表面有白色沉淀 | B. | 实验2中的高锰酸钾溶液先变色 | ||
| C. | 负极的电极反应为:Fe-3e-→Fe3+ | D. | 铁钉表面有红褐色物质生成 |