题目内容
3.制备:目前,我国采用“接触法”制硫酸,设备如图所示: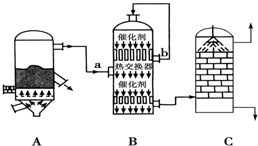
(1)图中设备A的名称是沸腾炉,B设备气流a、b温度较高的是b(填“a”或“b”).
(2)CuFeS2是黄铁矿的另一部分,煅烧时,CuFeS2转化为CuO、Fe2O3和SO2,该反应的化学方程式为:4CuFeS2+13O2$\frac{\underline{\;高温\;}}{\;}$4CuO+2Fe2O3+8SO2.
分析 (1)依据接触法制硫酸的工业流程和设备反应分析判断;二氧化硫氧化生成三氧化硫为放热反应分析判断;
(2)根据已知信息,确定出反应物和生成物,然后配平化学方程式.
解答 解:(1)A设备是硫铁矿与氧气在高温下煅烧反应在沸腾炉中进行;二氧化硫氧化生成三氧化硫为放热反应,所以b处温度高于a,
故答案为:沸腾炉; b;
(2)根据题意可知,高温煅烧时CuFeS2时,反应物为CuFeS2和O2,生成物为CuO、Fe2O3 和SO2,再根据化合价升降法配平氧化还原反应方程式,
故答案为:4CuFeS2+13O2 $\frac{\underline{\;高温\;}}{\;}$ 4CuO+2Fe2O3+8SO2.
点评 本题考查了工业合成硫酸的流程,涉及氧化还原方程式书写,题目较简单.

练习册系列答案
相关题目
5.下列离子方程式正确的是( )
| A. | 向含有Fe203的悬浊液中通入HI:Fe203+6H+═2Fe3++3H20 | |
| B. | 1 mol/L NaAl02溶液和1.5 mol/L HC1溶液等体积混合:6AlO2-+9H++3H2O═5A1(OH)3+Al3+ | |
| C. | 向Ca( Cl0)2溶液中通入S02:Ca2++2ClO-+S02+H20═CaSO3+2HC1O | |
| D. | 向0.1 mol/LpH=l的NaHA溶液中加入NaOH溶液:HA-+OH-═H2O+A2- |
6.市场上有一种加酶洗衣粉,即在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣物的汗渍、血迹以及人体排放的蛋白质油渍等遇到它,皆能水解而除去.下列衣料中不能用加酶洗衣粉洗涤的是( )
①棉织品 ②毛织品 ③腈纶织品 ④蚕丝织品 ⑤涤纶织品 ⑥尼龙织品.
①棉织品 ②毛织品 ③腈纶织品 ④蚕丝织品 ⑤涤纶织品 ⑥尼龙织品.
| A. | ①②③ | B. | ②④ | C. | ③④⑤ | D. | ③⑤⑥ |
3.短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为16,Y的原子半径比X的大,X与W同主族,Z是地壳中含量最高的金属元素,下列说法不正确的是( )
| A. | 原子半径的大小顺序:r(W)>r(Z)>r(Y) | |
| B. | 元素X、Y能形成多种化合物 | |
| C. | 元素W的简单气态氢化物的热稳定性比X的弱 | |
| D. | Y、W最高价氧化物所对应的水化物均能溶解Z的氢氧化物 |
10.在25℃时,向10mL0.01mol•L-1NaX溶液中逐滴加入0.01mol•L-1的盐酸溶液,滴定过程中溶液中HX、X-浓度所占分数(φ)随pH的变化曲线如图所示,据此判断下列说法中正确的是( )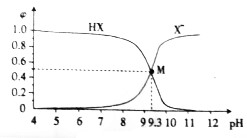

| A. | 25℃时,$\frac{c(HX)}{c({X}^{-})•c({H}^{+})}$=109.3 | |
| B. | M点溶液中存在:c(X-)+c(OH-)=c(H+)+c(Na+) | |
| C. | 滴加盐酸的过程中,水的电离程度先减小后增大 | |
| D. | 常温下,等浓度等体积的HX和NaX溶液混合后,溶液显酸性 |
13.下列说法中正确的是( )
| A. | 所有的电子在同一区域里运动 | |
| B. | 能量高的电子在离核近的区域运动,能量低的电子在离核远的区域运动 | |
| C. | 处于最低能量的原子叫基态原子 | |
| D. | 同一原子中,1s、2s、3s所能容纳的电子数越来越多 |

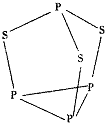 三硫化四磷是黄绿色针状结晶,其结构如图所示,不溶于冷水,溶于叠氮酸、二硫化碳、苯等有机溶剂.在沸腾的NaOH稀溶液中会迅速水解.回答下列问题:
三硫化四磷是黄绿色针状结晶,其结构如图所示,不溶于冷水,溶于叠氮酸、二硫化碳、苯等有机溶剂.在沸腾的NaOH稀溶液中会迅速水解.回答下列问题: (不考虑空间构型).
(不考虑空间构型).